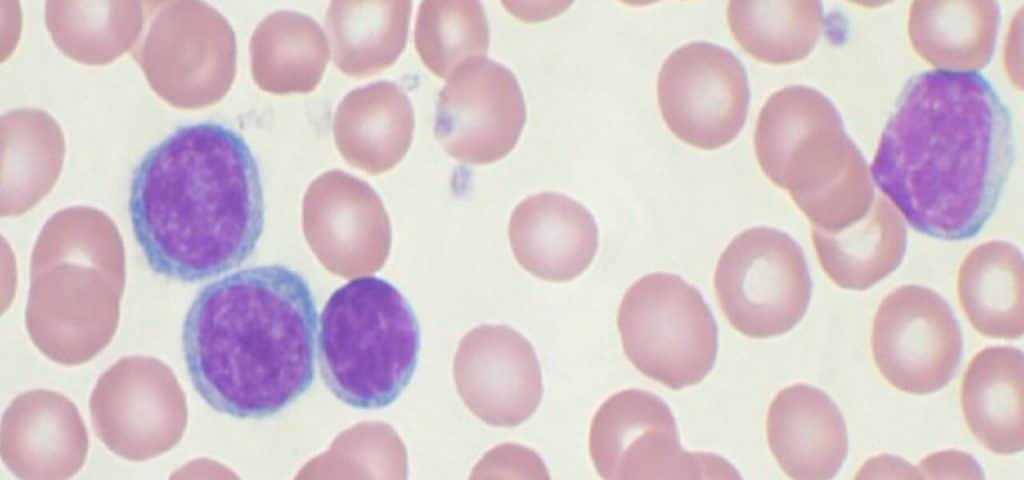
La leucemia linfoblastica acuta (ALL), è un tumore che coinvolge i globuli bianchi noti come linfociti, ed è purtroppo il cancro infantile più comune che interessa il 25% di tutte le diagnosi di cancro, e la sua aggressività lo fa diventare una delle principali cause di morte per cancro infantile. Mentre i tassi di guarigione sono migliorati grazie alla chemioterapia, i trattamenti contro il cancro sono tossici.
I sopravvissuti affrontano un aumentato rischio di malattie cardiache, malattie polmonari, difetti neurocognitivi e un aumentato rischio di sviluppare un cancro secondario nel corso della loro vita.
Una nuova ricerca ha scoperto bambini nati con una predisposizione genetica a produrre più linfocitali, in particolare in relazione ad altri tipi di globuli bianchi, sono a più alto rischio di sviluppo della ALL di tutti. Questa scoperta potrebbe aiutare nello sviluppo di modelli di rischio per i neonati che potrebbero portare a strategie di intervento precoce.
Lo studio è stato pubblicato sulla rivista scientifica Journal of Human Genetics.
Leucemia linfoblastica acuta (ALL): ecco cosa dice la ricerca
“Spero che la nostra ricerca sarà in grado di aiutare a identificare i bambini alla nascita che hanno il più alto rischio di leucemia”, ha dichiarato l’autore corrispondente Adam de Smith, assistente professore presso il Center for Genetic Epidemiology presso la Keck School of Medicine della USC e un membro dell’USC Norris Comprehensive Center. “Un obiettivo ideale sarebbe se gli screening neonatali in futuro potessero incorporare lo screening per la pre-leucemia”.
Gli studi genetici passati hanno identificato oltre una dozzina di posizioni sul genoma associate alla leucemia linfoblastica acuta infantile. Notando che questi punti corrispondevano a posti sul genoma associati a variazioni nei tratti delle cellule del sangue, come la conta dei globuli bianchi, il team dell’USC è stato ispirato a indagare su una connessione tra la sovrapproduzione di linfociti e il rischio di sviluppare la leucemia linfoblastica acuta.
Lo studio ha scoperto che i bambini geneticamente predisposti alla produzione di elevate quantità di linfociti hanno un rischio aumentato del 20% o più di sviluppare la leucemia liinfoblastica acuta. Lo studio ha anche fatto luce sull’importanza del numero di linfociti in proporzione ad altre cellule del sangue chiave.

“Il nostro è stato il primo studio a cercare variazioni genetiche associate al rapporto tra linfociti e alcune altre cellule del sangue: il rapporto tra linfociti e monociti, il rapporto tra linfociti e neutrofili e il rapporto tra linfociti e piastrine“, ha spiegato De Smith. “Sembra che non sia solo la propensione genetica a produrre un gran numero di linfociti, ma è anche il modo in cui quei numeri si riferiscono ad altri tipi di cellule del sangue”.
Attingendo ai dati della Biobanca britannica da oltre 400.000 individui, i ricercatori hanno condotto uno studio di associazione dell’intero genoma (GWAS) in due fasi sui tratti delle cellule del sangue, seguito dall’analisi in 2.666 casi di leucemia linfoblastica acuta e più di 60.000 controlli.
I dati della biobanca britannica provengono da adulti di origine europea, ma negli Stati Uniti i bambini latini in particolare hanno un rischio maggiore di sviluppare ALL rispetto ai bambini non latini. In futuro, de Smith spera di concentrare la ricerca sui tratti delle cellule del sangue in modo specifico sulle popolazioni pediatriche e latine.
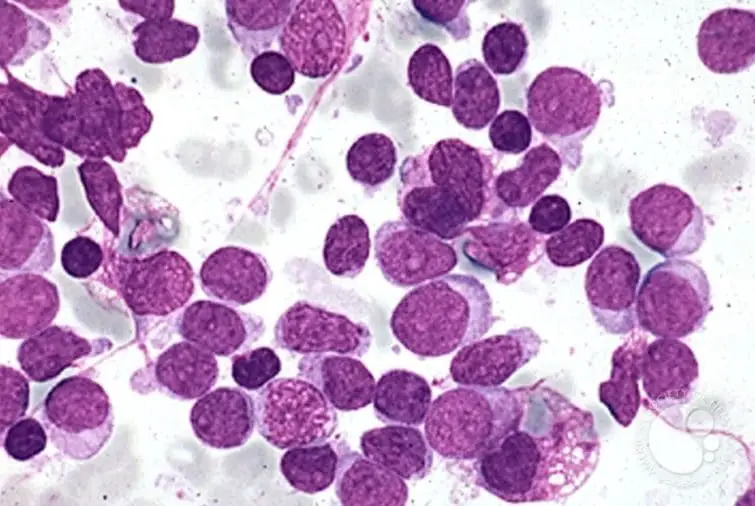
ALL si manifesta quando il DNA nelle cellule del midollo osseo muta. Normalmente le cellule crescono e muoiono a una velocità predeterminata, ma con ALL, le mutazioni genetiche istruiscono le cellule del midollo osseo a continuare a crescere e a dividersi. La produzione di cellule del sangue diventa fuori controllo e il midollo osseo produce cellule immature che si sviluppano in globuli bianchi leucemici chiamati linfoblasti. Queste cellule anormali non sono in grado di combattere le infezioni e spiazzano i globuli bianchi sani, i globuli rossi e le piastrine.
Si ritiene che la malattia sia il risultato di due eventi. Fino a un bambino su venti nasce con una mutazione genetica iniziale nota come clone pre-leucemico. Nella maggior parte dei casi, queste cellule pre-leucemiche non si trasformano mai in leucemia. Ma, per i bambini che sviluppano ALL, una seconda mutazione è innescata da eventi biologici. Una teoria prevalente è che se il sistema immunitario di un bambino non si sviluppa correttamente, possono verificarsi queste mutazioni di eventi secondari, che portano alla leucemia.
Lo studio USC delinea due ipotesi di come la sovrapproduzione di linfociti potrebbe svolgere un ruolo negli eventi che portano alla leucemia. I bambini geneticamente predisposti alla sovrapproduzione di linfociti hanno un maggiore pool di cellule pre-leucemiche e, di conseguenza, maggiori possibilità che si verifichi una mutazione secondaria. Un’ipotesi separata, ma non si esclude a vicenda, è che la sovrapproduzione di linfociti potrebbe determinare il motivo per cui il sistema immunitario non risponde normalmente all’infezione nei primi anni di vita.
Le teorie dei ricercatori corrispondono alla prevalente teoria dell'”infezione ritardata” della leucemia infantile e alla ricerca attuale sulla prevenzione dell’insorgenza della malattia. Se i bambini non sono sufficientemente esposti a infezioni e microbi da neonati, il loro sistema immunitario potrebbe non essere attivato correttamente. A tal fine, i ricercatori stanno sviluppando probiotici e altri potenziali interventi per prevenire le mutazioni secondarie che portano a ALL.
In futuro, De Smith prevede che un punteggio di rischio possa essere assegnato ai neonati in base a fattori di rischio genetici, tra cui la sovrapproduzione di linfociti, nonché rischi non genetici come nascere con un peso alla nascita elevato o attraverso un taglio cesareo pianificato. I bambini con punteggi ad alto rischio per ALL potrebbero ricevere terapie di intervento precoce.
In linea con questa linea di indagine, De Smith sarà coinvolto nella conduzione del più grande studio fino ad oggi utilizzando cellule del sangue cordonale neonate per studiare i cloni pre-leucemici in utero. Rilevare la presenza di queste cellule potrebbe anche far parte dello screening neonatale di routine per il rischio ALL e, in definitiva, delle misure preventive.