Un team di scienziati dell’Università di Huddersfield sta studiando come combattere il cancro usando farmaci “autoassemblati” e, sebbene la ricerca sia nelle sue primissime fasi, hanno già ottenuto buoni risultati.(1)
È importante considerare che uno degli aspetti più ostico delle terapie contro il cancro è la notevole varietà di tumori diversi che possono essere diagnosticati, ognuno dei quali richiede potenzialmente una soluzione diversa perché, sfortunatamente, lo stesso farmaco non è idoneo per tutti.
Inoltre, un altro importante problema di molti farmaci attuali è la loro scarsa selettività nei confronti dei tumori che causa problemi come la normale tossicità dei tessuti, gravi effetti collaterali e lo sviluppo di resistenza ai farmaci.
Lo studio è stato pubblicato sulla rivista scientifica Nature Comunications.
Farmaci autoassemblati: ecco cosa dice la ricerca
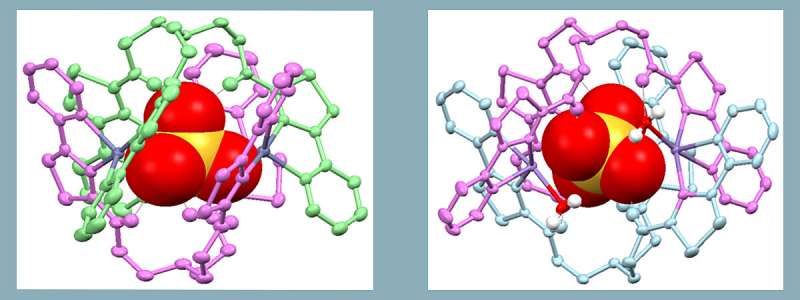
L’autoassemblaggio è la capacità di istruire sistemi chimici con informazioni specifiche in modo che nell’ambiente corretto generino spontaneamente composti biologicamente attivi. Usando questo processo molti composti differenti possono essere formati rapidamente e facilmente con i diversi farmaci autoassemblati che possiedono differenti proprietà chemioterapiche.
“In futuro, potrebbe essere possibile prendere di mira molti tumori attraverso questo approccio con i giusti farmaci ‘autoassemblati’ in modo tale da essere selettivi per un cancro specifico“, ha spiegato il professor Craig Rice.
il professor Roger Phillips, il dottor Simon Allison e il professor Craig Rice hanno dimostrato sistemi chimici che si autoassemblano in capsule molecolari altamente tossiche nei confronti delle cellule tumorali umane di una gamma di diversi tipi di tumore. Ancora più importante, hanno mostrato una selettività del cancro senza precedenti in laboratorio, che in alcuni casi è molte migliaia di volte più tossica per le cellule tumorali rispetto alle cellule sane e normali.
In ultima analisi, se si ottengono risultati simili in sistemi di test più complessi, inclusi i pazienti, e una volta considerati sicuri dopo accurati test, i farmaci autoassemblati potrebbero offrire la possibilità di poter trattare i tumori senza i effetti collaterali severi comunemente associati ai farmaci chemioterapici.
“La scoperta e lo sviluppo di farmaci antitumorali possono richiedere molto tempo e denaro, poiché un particolare farmaco è efficace solo contro un numero relativamente piccolo di tumori con specifiche proprietà condivise“, ha spiegato il professor Rice, che dirige il Dipartimento di scienze chimiche dell’Università ed è anche il Direttore del Centro di Modellistica Strutturale, Molecolare e Dinamica della Scuola di Scienze Applicate.
“In futuro, potrebbe essere possibile prendere di mira molti tumori attraverso questo approccio con il corretto farmaco ‘autoassemblato’ in modo tale da essere selettivo per un cancro specifico“, ha affermato.
La ricerca potrebbe anche aprire la strada al targeting dei tumori difficili da trattare per i quali i farmaci chemioterapici comunemente usati hanno scarso o nessun effetto. Gli studi pubblicati mostrano che il nuovo potenziale farmaco può essere assemblato con zinco, rame o manganese, con i tre ioni metallici che conferiscono proprietà chemioterapiche significativamente diverse attraverso meccanismi diversi a seconda dello ione metallico utilizzato.
“È questo che consente la generazione di diversi sistemi chimici, ciascuno dei quali può avere specificità per diversi tipi di cancro“, ha affermato lo scienziato.
Durante lo studio, sono stati generati due diversi composti utilizzando zinco e manganese. Mentre questi due composti “sembrano” molto simili, il composto di zinco ha dimostrato un’eccellente attività antitumorale e selettività verso una serie di tumori in laboratorio, mentre il composto di manganese era relativamente molto più tossico, il che significa che c’era più attività antitumorale a un concentrazione più bassa, con selettività simile rispetto ai farmaci attualmente testati.
Studi futuri verificheranno se questo può essere utile per i tumori per i quali non sono attualmente disponibili trattamenti efficaci.
Il professor Rice ha aggiunto che questi studi rappresentano i primissimi giorni della scoperta di farmaci e, sebbene i risultati iniziali siano stati molto promettenti, ci saranno molti ostacoli da superare prima che si realizzi il pieno potenziale clinico di questa nuova scoperta.
Farmaci autoassemblati: l’importanza di generare farmaci mirati contro i tumori
Il cancro è la seconda causa di morte nel mondo. Il numero di decessi e incidenze aumenta ogni anno. I farmaci antitumorali a base di metallo sono stati utilizzati clinicamente in tutto il mondo, ma soffrono di scarsa selettività, gravi effetti collaterali e resistenza ai farmaci. Lo sviluppo di farmaci mirati al tumore è la base per un trattamento preciso del cancro.
Recentemente, il professor Hongke Liu dell’Università Normale di Nanchino, il professor Jing Zhao e l’accademico Zijian Guo dell’Università di Nanchino hanno ottenuto risultati rivoluzionari nello sviluppo di farmaci antitumorali. Hanno proposto una strategia di “letalità catalizzata bio-ortogonalmente” (BCL) e hanno pubblicato i loro risultati in National Science Review (NSR).
La strategia BCL utilizza i tumori come fabbriche di produzione per generare un farmaco Ru-rhein altamente potenziale mirato al tumore, che può uccidere selettivamente le cellule cancerose e i tumori nei topi portatori di tumore, mentre nessuna tossicità si è verificata sulle cellule sane. La strategia BCL genera farmaci mirati da composti non tossici all’interno del tumore, non solo evitando la decomposizione e l’inattivazione del farmaco durante il trasporto e lo stoccaggio, ma anche riducendo i gravi effetti collaterali causati dall’interazione con molecole biologicamente attive durante il trattamento.
Il contenuto di rame nelle cellule tumorali è molto più alto di quello nelle cellule normali. Il farmaco bersaglio Ru-reina è generato da due composti non tossici Ru-N3 e reina-alchino all’interno del tumore con una resa superiore all’80%, utilizzando le reazioni bioortogonali catalizzate dal rame endogene. Tuttavia, le reazioni sopra menzionate difficilmente si verificano nei tessuti normali.
Pertanto, il targeting tumorale e la selettività della Ru-reina sono realizzati dalla strategia BCL. La ru-reina mostra un’elevata attività antitumorale, specialmente nei confronti della cellula tumorale polmonare A549, tossica quasi quanto il cisplatino, mentre non è tossica per l’HLF normale delle cellule polmonari e potrebbe essere utilizzata come farmaco candidato per lo sviluppo clinico (Figura 2). La ru-reina colpisce i mitocondri delle cellule tumorali e provoca la morte cellulare autofagica attraverso la via mitocondriale.
Un modello murino stato utilizzato per convalidare la strategia BCL. Rispetto al gruppo di controllo, la crescita tumorale dei topi portatori di tumore iniettati con Ru-N3 e rhein-alkyn è stata significativamente inibita e altri organi erano quasi intatti (Figura 3). La generalità della strategia BCL è stata dimostrata nella generazione di osmio e metallofarmaci a base di iridio all’interno delle cellule cancerogene.
Il metodo BCL fornisce una strategia generale per il trattamento preciso delle malattie e rivela anche che il tumore può fornire specie di rame che catalizzano in modo efficiente reazioni ortogonali. Questa ricerca è stata finanziata dalla National Natural Science Foundation of China.