Gli antibiotici purtroppo se utilizzati spesso, finiscono per non essere più efficenti, perché il nostro corpo sviluppa una resistenza ai farmaci, ed ecco perché dobbiamo cercarne sempre di nuovi. Ma una sorprendente strategia di difesa cellulare potrebbe ispirare una nuova categoria di antibiotici.
Di fronte a invasori batterici, alcune cellule umane dispensano una sostanza sorprendente: il sapone. Queste cellule, che non fanno parte del sistema immunitario, liberano una proteina simile a un detergente che dissolve i pezzi delle membrane interne dei batteri, uccidendo gli infiltrati, secondo i ricercatori che oggi lo hanno pubblicato su Science.
Le cellule immunitarie “professionali”, come gli anticorpi o i globuli bianchi, ricevono molta attenzione, ma “tutte le cellule sono dotate di una certa capacità di combattere le infezioni”, afferma John MacMicking, immunologo alla Yale University.
Negli esseri umani, queste difese cellulari ordinarie sono state spesso trascurate, afferma MacMicking, anche se fanno parte di “un antico e primordiale sistema di difesa” e potrebbero fare la differenza nello sviluppo di trattamenti per nuove infezioni.
Spesso, le cellule non immunitarie si affidano a un avvertimento delle loro controparti professionali per combattere le infezioni. Dopo aver rilevato gli estranei, le cellule immunitarie specializzate rilasciano un segnale di allarme chiamato interferone gamma. Quel segnale stimola altre cellule, comprese le cellule epiteliali che rivestono la gola e l’intestino e sono spesso prese di mira da agenti patogeni, a passare all’azione.
MacMicking e colleghi hanno cercato le basi molecolari di tale azione infettando le versioni di laboratorio delle cellule epiteliali umane con i batteri della Salmonella, che possono sfruttare l’interno ricco di sostanze nutritive delle cellule. Quindi, il team ha esaminato oltre 19.000 geni umani, alla ricerca di quelli che avessero maturato una certa protezione dall’infezione.
Antibiotici mirati e specializzati
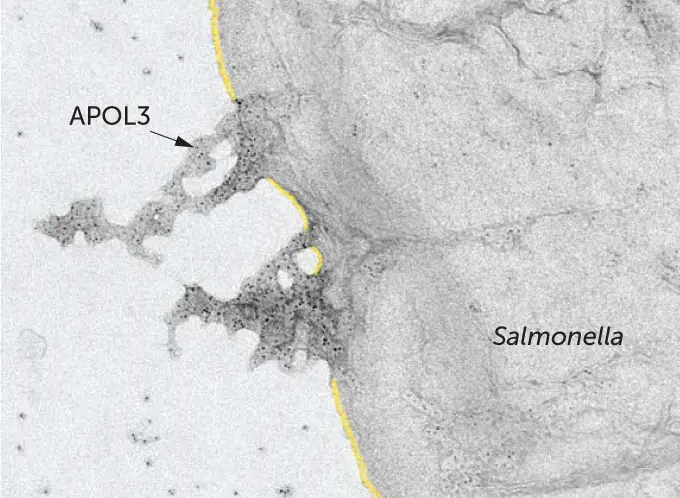
Un gene, che contiene le istruzioni per una proteina chiamata APOL3, si è distinto. Quando questo gene è stato disattivato, le cellule epiteliali hanno ceduto a un’infezione da Salmonella, anche se avvertite dall’interferone gamma. Zoomando sulle molecole di APOL3 in azione all’interno delle cellule ospiti con un microscopio ad alta potenza, i ricercatori hanno scoperto che la proteina invadeva i batteri a sciami e in qualche modo li uccideva.
I microbi della salmonella sono molto resistenti, protetti da una membrana esterna e interna, una caratteristica condivisa da molte diverse forme di batteri. Questo doppio strato rende questi batteri difficili da uccidere, ma ulteriori indagini hanno rivelato come l’APOL3 e un’altra molecola, GBP1, lavorino insieme per riuscirci.
GBP1 in qualche modo allenta la membrana esterna dei batteri, aprendo le porte all’APOL3 che dispensa la sua morte per dissoluzione nella membrana lipidica interna. APOL3 ha sia parti che amano l’acqua che che amano i lipidi, permettendogli di legarsi alla membrana interna e dissolverla nel fluido intracellulare, come il sapone che lava via il grasso, grazie ai tensioattivi.
“Siamo rimasti un po’ sorpresi di trovare un’attività simile a un detergente all’interno delle cellule umane”, afferma MacMicking, dato che una tale molecola potrebbe dissolvere anche le membrane ospiti. Ma i ricercatori hanno scoperto che l’APOL3 prende di mira specificamente i lipidi presenti nei batteri e la sua attività è bloccata dal colesterolo, un componente comune delle membrane cellulari dei mammiferi, lasciando inalterati i tessuti umani.
“Tutto in questi risultati è fantastico”, afferma Jessica Brinkworth, un’immunologa evoluzionista dell’Università dell’Illinois Urbana-Champaign che non è stata coinvolta nello studio. Molte infezioni iniziano in queste cellule epiteliali e capire come reagiscono è fondamentale per lo sviluppo di trattamenti futuri, afferma.
“La scoperta davvero interessante è come l’APOL3 è in grado di distinguere tra membrane batteriche e membrane dell’ospite”, afferma. L’evoluzione ha trovato un modo così elegante per controllare questo potente strumento “è una cosa bellissima”.
La cosa sensazionale è che quindi sarà possibile diminuire la resistenza agli antibiotici, non utilizzando più come principio attivo di base una muffa, e per di più non saranno possibili cure mirate e non ad ampio spettro, riducendo gli effetti collaterali.