La malattia del sangue nota come anemia falciforme è una malattia ereditaria che causa dolore grave e debilitante. Ora, quasi 75 anni dopo la scoperta, i ricercatori stanno sviluppando terapie geniche per curarlo.
Oggi è chiaro che i nostri geni non solo causano molte malattie, ma hanno anche potenziali cure. Ma non è sempre stato così. Fu solo nel 1949 che gli scienziati scoprirono per la prima volta il colpevole molecolare di una malattia: le sue radici nel codice genetico.
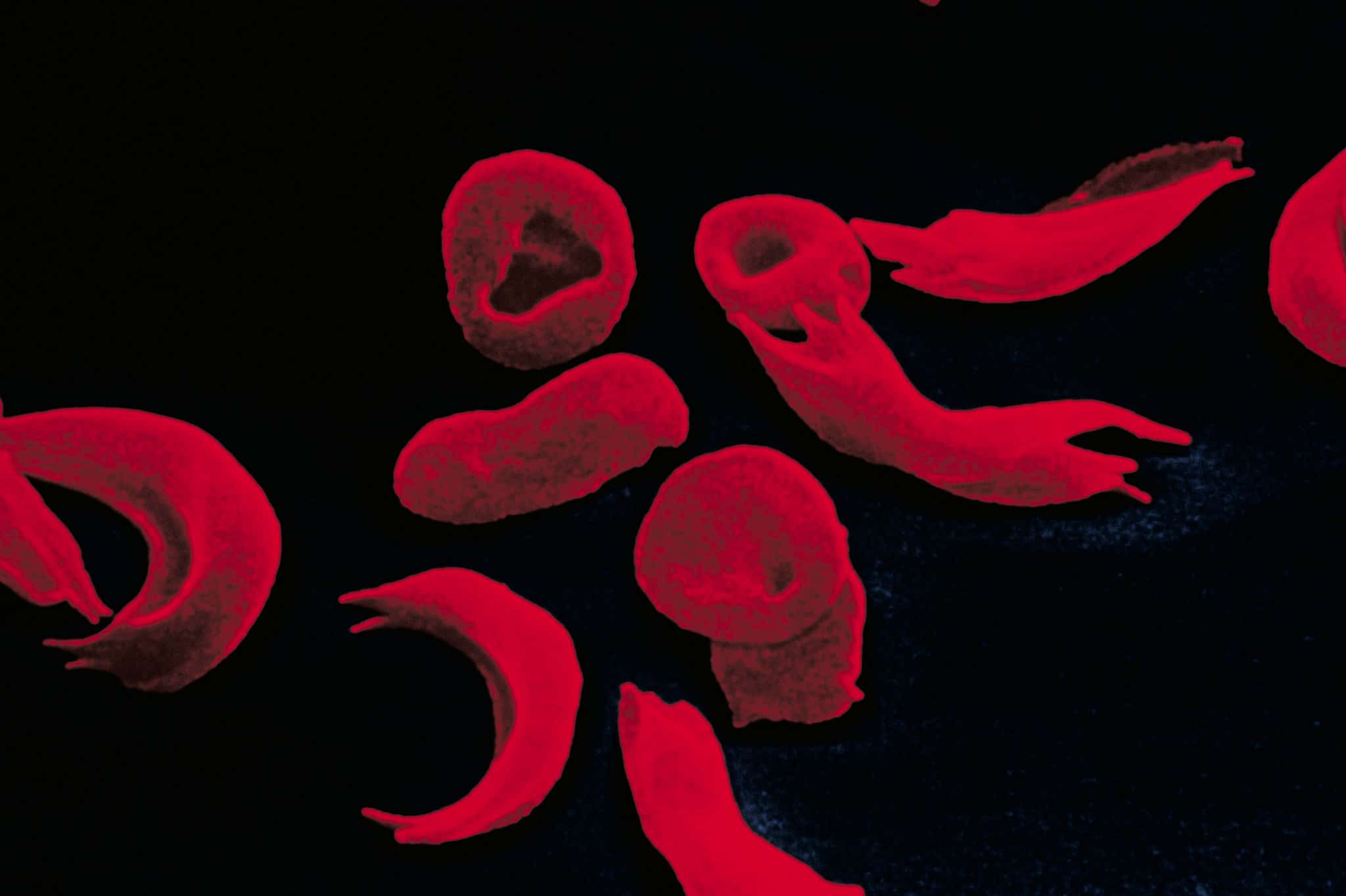
L’anemia falciforme è il risultato di un cambiamento in una proteina chiave dell’emoglobina, che aiuta a trasportare l’ossigeno nei globuli rossi. L’emoglobina normalmente consente ai “globuli rossi di essere molto flosci e flessibili e di scivolare e scivolare facilmente attraverso i vasi sanguigni”, afferma la pediatra Erica Esrick.
Ma una mutazione in un singolo gene, il gene HBB, fa accumulare l’emoglobina in lunghe stringhe all’interno dei globuli, conferendo loro una forma rigida, a falce. Invece di essere “morbidi”, i globuli rossi rigidi rimangono bloccati all’interno dei vasi sanguigni, bloccando il flusso sanguigno.
L’anemia falciforme colpisce milioni di persone in tutto il mondo, in particolare quelle i cui antenati provengono dall’Africa subsahariana, parti del Medio Oriente e del sud-est asiatico. Negli Stati Uniti, ad esempio, circa 100.000 persone convivono con la malattia, la maggior parte delle quali nere o latine. Le persone con anemia falciforme hanno un’aspettativa di vita ridotta, vivendo in media solo fino alla fine dei 40 anni, in gran parte a causa di ictus o danni agli organi causati dai vasi sanguigni ostruiti.
Esrick, del Boston Children’s Hospital e della Harvard Medical School, e altri stanno cercando di combattere la malattia attraverso la terapia genica. Le terapie geniche cercano di manipolare le informazioni stesse della vita sostituendo, inattivando o riparando i geni mancanti o rotti e quindi curando i pazienti.
Ma il viaggio verso la manciata di terapie geniche approvate di oggi, anche per malattie come la sindrome da immunodeficienza combinata grave o SCID, alcuni tumori del sangue e l’atrofia muscolare spinale, è stato complesso. I primi studi clinici negli anni ’90 non erano efficaci e gli anni 2000 hanno portato conseguenze indesiderate e talvolta mortali, inclusa una malattia simile alla leucemia.
Nonostante le sfide della terapia genica, molti ricercatori ritengono che l’anemia falciforme sia un buon bersaglio perché i percorsi molecolari sono ben compresi e diretti. Inoltre, ogni copia del gene non ha bisogno di essere riparata per avere un effetto. Gli individui che ereditano il gene mutato da un solo genitore, ad esempio, non sviluppano l’anemia falciforme.
Anemia falciforme: il probabile metodo
Esrick sta conducendo una sperimentazione clinica con la quale testa una terapia genica che tenta di incoraggiare il corpo a produrre più di un tipo sano di emoglobina prodotta da feti e bambini piccoli, ma non adulti, chiamata emoglobina fetale. Il DNA per la produzione di una breve stringa di materiale genetico chiamato microRNA viene fornito da un virus nelle cellule del midollo osseo di un paziente.
Il virus, chiamato vettore, inserisce permanentemente il DNA nel modello genetico della cellula. Il microRNA interferisce quindi con la produzione di una proteina che impedisce la produzione di emoglobina fetale. Una volta che quella proteina viene bloccata, la produzione di emoglobina fetale si riattiva. Come aprire un rubinetto, un flusso costante di emoglobina sana può fluire nel flusso sanguigno, compensando la forma difettosa.
I dati preliminari pubblicati nel gennaio 2021 hanno mostrato che il trattamento ha aiutato sei pazienti con anemia falciforme a produrre emoglobina fetale, hanno riferito Esrick e colleghi sul New England Journal of Medicine. Durante il periodo di follow-up, che andava da diversi mesi a più di due anni, i sintomi dei pazienti sono stati ridotti o eliminati. Il team ha ampliato lo studio per includere più pazienti e testare ulteriormente il trattamento.
Gli scienziati stanno testando anche altri modi per affrontare l’anemia falciforme attraverso la terapia genica. Una società di biotecnologie chiamata bluebird bio sta testando un approccio che fornisce una copia funzionale del gene HBB ai pazienti. Un altro team si sta preparando per iniziare una sperimentazione che modificherà quel gene direttamente utilizzando CRISPR/Cas9.
La scrittrice dello staff di Science News Erin Garcia de Jesús ha parlato con Esrick della sperimentazione clinica in corso sull’emoglobina fetale, inclusi gli ostacoli e la speranza. La conversazione è stata modificata per lunghezza e chiarezza.
Garcia de Jesús: Quali strumenti abbiamo attualmente per trattare l’anemia falciforme?
Esrick: L’unico trattamento curativo è un trapianto di midollo osseo. Il midollo osseo è come la fabbrica dei globuli. Se riesci a ottenere il midollo osseo da qualcuno che non ha l’anemia falciforme, allora puoi far crescere i tuoi globuli rossi sani che non falciano. Ma questa è una procedura importante, ed è davvero standard solo se hai quello che viene chiamato un fratello abbinato, un fratello o una sorella senza anemia falciforme le cui proteine chiave dei globuli bianchi corrispondono alle tue.
Meno del 20% delle persone con anemia falciforme ha un fratello abbinato disponibile. Se è disponibile un fratello abbinato, allora questa è un’opzione di trattamento potenziale davvero buona, ma è comunque una procedura rischiosa. Si presenta con un rischio iniziale di mortalità e molti potenziali effetti collaterali, come la malattia del trapianto contro l’ospite e un rischio più elevato di infezione a causa dei farmaci immunosoppressori.
Poi ci sono i farmaci per il trattamento dell’anemia falciforme. La più consolidata e di lunga durata si chiama idrossiurea. Aumenta l’emoglobina fetale. In molte persone aumenta di molto l’emoglobina fetale; ecco perché funziona così bene. È disponibile dagli anni ’90 e si è spostato gradualmente verso età sempre più giovani.
Ora è una raccomandazione molto chiara che essenzialmente ogni bambino con anemia falciforme dovrebbe prenderlo. Ma non tutti hanno accesso a cure ematologiche specializzate, ed è un farmaco che deve essere assunto quotidianamente. Alcune persone hanno effetti negativi e non possono prenderlo. Inoltre, non funziona per tutti.
Garcia de Jesús: Quante persone ci sono nella prova della tua squadra e quali risultati hai visto finora?
Esrick: Nove pazienti sono stati curati. Prevediamo che il 10° paziente sarà presto curato. I dati preliminari dei primi sei pazienti sono stati pubblicati circa un anno fa. I dati aggiuntivi dei pazienti successivi sono stati in gran parte abbastanza simili, ad eccezione di un paziente la cui risposta emoglobinica fetale purtroppo non era così robusta.
Garcia de Jesús: Com’è il processo per i partecipanti alla prova?
Esrick: I pazienti devono raccogliere le loro cellule, le cellule vivono nel midollo osseo e danno origine ai globuli, il che richiede un ricovero ospedaliero di tre giorni e talvolta deve essere ripetuto alcune volte. È attraverso IV (fluidi intravenosi), in pratica. Quindi le cellule vengono portate in laboratorio.
Quando riceviamo la parola dal laboratorio, “OK, abbiamo un buon prodotto” il che significa che il virus ha portato il DNA in un numero sufficiente di cellule, il paziente torna e viene ricoverato in ospedale per circa un mese. È un ricovero in ospedale lungo e arduo perché hanno bisogno di ricevere la chemioterapia.
Il motivo per cui hanno bisogno della chemioterapia è perché le cellule del midollo osseo che non sono state raccolte devono essere quasi spazzate via per dare il vantaggio alle cellule che vengono restituite anche attraverso IV per aprire un’auto produzione.
La chemioterapia comporta molti degli effetti collaterali e dei rischi associati alla terapia genica, compresi i rischi acuti a breve termine come la perdita dell’udito e la nausea. E include anche alcuni dei rischi a lungo termine, tra cui l’infertilità e il rischio di tumori del sangue.
Garcia de Jesús: Perché scegliere la terapia genica rispetto a un trapianto di midollo osseo se entrambi richiedono la chemioterapia?
Esrick: Con la terapia genica, non ci sono problemi con l’immunosoppressione, perché sono le tue stesse cellule. Le persone che ricevono un trapianto da un’altra persona devono assumere farmaci immunosoppressori per un periodo di mesi dopo il trapianto. Esiste il rischio di rigetto del trapianto a causa della mancata corrispondenza tra il donatore e il ricevente.
L’altro rischio in un trapianto di midollo osseo da un’altra persona è la malattia del trapianto contro l’ospite, in cui l’innesto e le cellule donate respingono il ricevente. Ciò può causare malattie gravi. Con la terapia genica, questo non è affatto un rischio.
Garcia de Jesús: L’anno scorso, uno studio clinico condotto da una società chiamata bluebird bio ha annunciato che un partecipante allo studio ha sviluppato la leucemia. Il cancro è ovviamente una grande preoccupazione e ha contrastato i precedenti studi di terapia genica. Cosa sappiamo finora a riguardo?
Esrick: Questo era, ovviamente, di grande preoccupazione per il campo. In realtà era il secondo caso di leucemia in quel processo. Il primo è stato pubblicato un paio di anni fa come case report. Se c’è mai un caso di leucemia o di qualsiasi preleucemia in uno studio di terapia genica, ci chiediamo sempre: è stato causato dal fatto che il vettore ha bloccato un gene in un punto pericoloso? Non sembra che sia così.
Nel primo paziente del bio trial bluebird che ha sviluppato la leucemia, le cellule leucemiche non avevano nemmeno il gene trasferito al loro interno. Quindi, il pensiero era che probabilmente fosse solo un esempio di chemioterapia che causa la leucemia, che sappiamo può accadere in una piccola percentuale di persone che ricevono la chemioterapia.
Ma il secondo caso, nel febbraio 2021, ha davvero alzato bandiera rossa. Perché è successo due volte in uno studio su soli 40 pazienti? Non è ancora del tutto chiaro. Ci sono alcuni studi che suggeriscono che le persone con anemia falciforme possono avere un aumentato rischio di leucemia. Ma la Food and Drug Administration ha sospeso il bio-processo bluebird mentre venivano svolte alcune indagini. Quando è diventato abbastanza chiaro che non era direttamente correlato al vettore, il processo è stato autorizzato a riaprire.
Il nostro studio, che ha molte somiglianze con il bio trial bluebird, non è stato sospeso dalla FDA ma è stato sospeso dal nostro finanziatore, il National Heart, Lung and Blood Institute mentre esaminavano i dati. Quella presa è stata recentemente revocata.
Ma sai quando qualcosa del genere accade sul campo, è un grosso problema. Ho chiamato tutti i pazienti che avevamo trattato nel nostro studio per farglielo sapere. I casi bio di bluebird si sono verificati in pazienti che erano stati trattati tre e cinque anni prima. Il paziente trattato più a lungo nel nostro studio è stato quasi tre anni e mezzo fa e l’ultimo trattato è stato circa otto o nove mesi fa. Spero di non vedere segnali preoccupanti per un nuovo sviluppo del genere, ma è troppo presto per dirlo.
Garcia de Jesús: Quali sono alcune delle maggiori sfide che l’anemia falciforme ha dovuto superare?
Esrick: Per molto tempo non ci sono state nuove terapie. Queste tecnologie hanno richiesto molto tempo perché si basano su scoperte scientifiche di base su cui si stava lavorando. Ma anche la popolazione di pazienti con anemia falciforme è una popolazione che è stata storicamente sottoservita e senza molto potere.
Negli Stati Uniti, sono principalmente pazienti neri e latini e, in generale, quelle popolazioni hanno sofferto di disuguaglianze sanitarie. Penso che se ci fosse stata una malattia che avesse causato questo grado di morbilità, mortalità e dolore in altre parti della popolazione, sarebbe stata più rapida.
Garcia de Jesús: Cosa ti dà speranza? Cosa trovi eccitante?
Esrick: Mi ritrovo a farmi in quattro per assicurarmi di imbattermi in “Abbiamo una cura!” Ma detto questo, è davvero eccitante che questo sia un trattamento che è teoricamente possibile per tutti senza la necessità di trovare una corrispondenza midollo osseo. Questa è un’enorme differenza rispetto ai classici trapianti di midollo osseo.
La velocità con cui vengono sviluppati nuovi trattamenti [terapia genica] è sorprendente. Penso che l’orizzonte sia molto luminoso in termini di una o forse molte di queste terapie che sono davvero efficaci e sicure. Ho parlato con così tanti pazienti e famiglie che hanno contattato interessati al nostro studio o ad altri studi. C’è un enorme bisogno insoddisfatto. Il fatto che molti di questi nuovi trattamenti vengano sviluppati è un incoraggiamento per queste famiglie.