Un nuovo sistema di somministrazione di farmaci basato sulla nanotecnologia del DNA o nanotubi di DNA, creato da un team guidato da un ingegnere della Johns Hopkins, potrebbe migliorare i trattamenti e i tassi di sopravvivenza mirando meglio al glioblastoma.
Il glioblastoma è ampiamente considerato il cancro al cervello più aggressivo. Anche con le terapie a disposizione, i tassi di sopravvivenza dei pazienti sono bassi, con la maggior parte che vive in media 15-18 mesi dopo la diagnosi. A causa delle caratteristiche estremamente diverse dei tumori del glioblastoma e della loro posizione nel corpo, nel cervello sensibile e ben protetto, il trattamento di questa malattia è impegnativo.
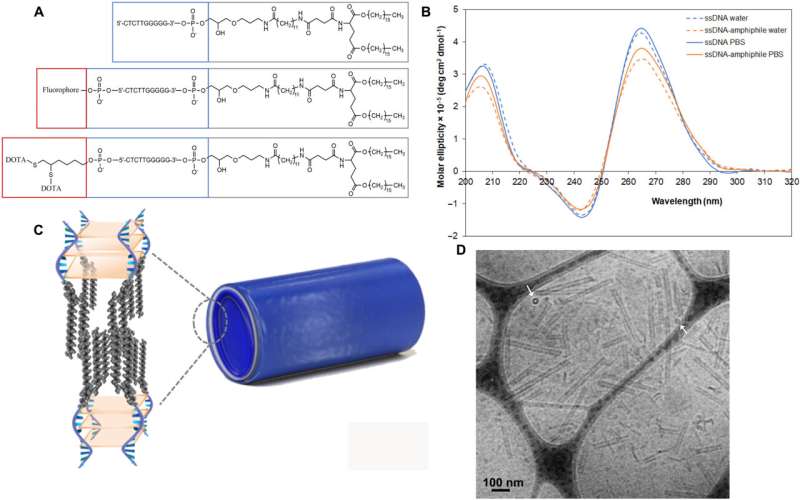
“Uno dei maggiori ostacoli alla somministrazione di trattamenti attraverso il flusso sanguigno è attraversare la barriera emato-encefalica che non solo protegge il cervello dalle tossine nel flusso sanguigno, ma può anche bloccare grandi molecole come le terapie. Il mio team sta usando la nanotecnologia DNA per creare i nanotubi di DNA a filamento singolo (ssDNA) che possono attraversare la BBB, prendendo di mira i tumori cerebrali“, ha affermato Efie Kokkoli, professore di ingegneria chimica e biomolecolare presso la Whiting School of Engineering e membro principale dell’Institute for NanoBioTechnology.
I risultati della ricerca sono stati pubblicati sulla rivista scientifica Science Advances.
Nanotubi di DNA: ecco come funzionano
La nanotecnologia del DNA consente ai ricercatori di utilizzare il DNA sintetico per vari scopi tecnologici. Kokkoli e il suo gruppo hanno utilizzato ssDNA sintetico e altre molecole per progettare un nanotubo autoassemblante in grado di trasportare sostanze terapeutiche. Il DNA sintetico consente inoltre ai ricercatori di personalizzare il proprio design per colpire cellule specifiche.
“Quindi non solo i nanotubi di DNA sono un pacco, ma sono anche il corriere, che trasporta il farmaco al suo obiettivo“, ha spiegato Kokkoli.
Kokkoli, con i colleghi dell’Università del Minnesota e della Johns Hopkins, ha utilizzato modelli murini per testare l’ accuratezza dei nanotubi di DNA nel prendere di mira il glioblastoma.
I ricercatori hanno iniettato nanotubi in entrambi i lati degli emisferi cerebrali dei topi: un lato era sano e uno era carico di tumori del glioblastoma. I ricercatori hanno osservato che i tumori hanno trattenuto i nanotubi, ma erano assenti dal lato sano del cervello, fornendo prove che ci sono poche possibilità che le nuove terapie danneggino le cellule sane.
Il team ha anche iniettato nanotubi in una vena sulla coda dei topi e ha notato gli stessi risultati, indicando che i nanotubi di DNA hanno viaggiato con successo attraverso il corpo dei roditori e hanno attraversato la BBB.
La rimozione chirurgica completa dei tumori del glioblastoma non è possibile poiché tracce di cellule di glioblastoma possono essere lasciate indietro, causando la recidiva. Ecco perché è standard includere i trattamenti chemioterapici dopo l’intervento chirurgico.
Come parte del loro studio, il team di Kokkoli ha valutato i nanotubi come veicolo di consegna per la doxorubicina, un farmaco chemioterapico. Usando nuovamente modelli murini, hanno iniettato cellule di glioblastoma su un lato del cervello per simulare le cellule tumorali residue rimanenti dopo la resezione del tumore.
Dopo l’iniezione, è stata impiantata una minuscola pompa per infusione per fornire diversi trattamenti nel cervello dei soggetti del test. Alcuni topi hanno ricevuto nanotubi vuoti, mentre altri hanno ricevuto doxorubicina liberamente nel cervello o attraverso i nanotubi di DNA.
I trattamenti si sono interrotti dopo due settimane e i topi sono stati monitorati per circa un mese e mezzo. I topi che hanno ricevuto la doxorubicina tramite i nanotubi hanno mostrato un aumento della sopravvivenza: la metà era ancora viva alla fine dello studio.
Ancora più importante, i topi che hanno ricevuto doxorubicina libera dai nanotubi hanno mostrato segni di tossicità nel fegato e nella milza. Al contrario, non ci sono stati risultati significativi nei tessuti della milza e del fegato di topi trattati con nanotubi vuoti e quelli che hanno rilasciato doxorubicina.
“I nostri risultati hanno mostrato che i nanotubi di DNA sono uno strumento promettente per colpire i tumori del glioblastoma e fornire terapie ai tumori cerebrali“, ha specificato Kokkoli.
Il glioblastoma è il tumore cerebrale più comune e più aggressivo. Con un’incidenza da 2 a 5 casi ogni 100.000 persone in Nord America ed Europa, rappresenta oltre il 50% dei tumori cerebrali maligni primari, ma rimane ancora una malattia rara. Il numero di nuovi casi di glioblastoma all’anno può quindi essere stimato intorno ai 250.000 nel mondo, con una sovraincidenza nelle popolazioni caucasiche e un leggero aumento previsto negli anni a venire a causa dell’invecchiamento della popolazione.
Si tratta anche del tumore cerebrale più aggressivo con una sopravvivenza media di quattordici a sedici mesi e un tasso di sopravvivenza globale a cinque anni inferiore al 10% con l’attuale standard di cura. Circa 200.000 persone muoiono ogni anno a causa di un glioblastoma nel mondo, di cui quasi 15.000 in Europa e 9.000 negli Stati Uniti.
L’attuale standard di cura per il glioblastoma consiste nella resezione della quantità massima di tumore (la chirurgia è possibile nel 50-70% dei pazienti, a seconda dell’area geografica), o una semplice biopsia (per i tumori non resecabili), con l’eventuale aggiunta di un trattamento chemioterapico locale negli Stati Uniti e in Giappone, seguito dall’implementazione del “protocollo Stupp“: radioterapia seguita da chemioterapia adiuvante – Temozolomide (Temodal® di Merck) per sei mesi.
L’efficacia di questo trattamento di prima linea varia in base allo stato biologico dei pazienti per i geni EGFRvIII e MGMT, alla loro età, e alle loro condizioni generali, tuttavia consente in media un guadagno di sopravvivenza di poco più di un anno, perché purtroppo non impedisce la ricaduta quasi sistematica.
I trattamenti di seconda linea sono più variabili . Mentre le seconde resezioni sono rare, tranne che negli Stati Uniti, la chemioterapia di seconda linea viene spesso prescritta utilizzando un prodotto citostatico della famiglia delle nutro-urea, come Lomustine (BMS / Prostrakan) o Carmustine (BMS BiCNU®), in combinazione con l’anti -bevacizumab angiogenico (Avastin® di Roche). Questo trattamento di seconda linea consente una vita migliore senza sintomi ma non migliora significativamente il tempo di sopravvivenza globale.
Per tutte queste ragioni, il trattamento del glioblastoma attraverso i tubi di DNA si sono dimostrati una terapia della medicina biotecnologica particolarmente efficace che merita di essere approfondita.