I malati di cancro sembravano trarre beneficio dalle cellule killer naturali ottenute da donatori in un metodo sperimentale di cura del cancro che coinvolgeva un esercito aggressivo di combattenti del sistema immunitario dotati della capacità di colpire le cellule maligne e distruggerle.
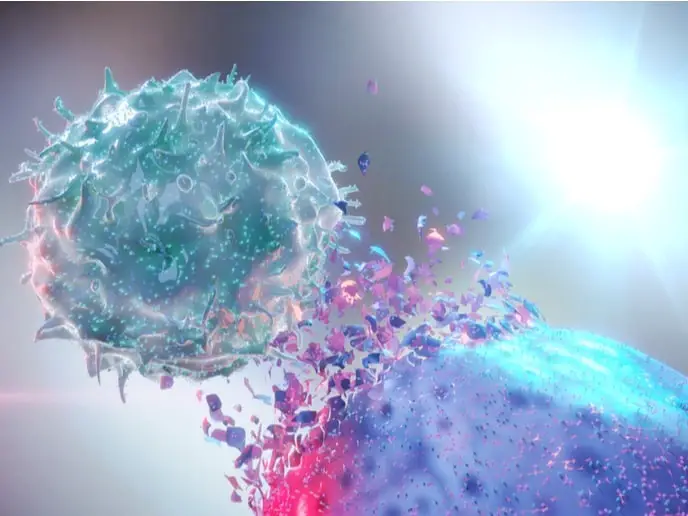
Le cellule killer naturali sono state pretrattate con nicotinamide, un composto ampiamente noto alla maggior parte delle persone come niacina o vitamina B 3 . È una sostanza con un’affinità speciale per le cellule killer naturali, migliorando la loro capacità di annientare i tumori.
Una volta attivati in laboratorio, questi killer naturali sono pronti per essere scatenati contro obiettivi formidabili. La metodologia in evoluzione si è rivelata promettente in uno studio preliminare volto a forzare la remissione dei tumori del sangue difficili da trattare.
I risultati della ricerca sono stati pubblicati su Science Translational Medicine.
Combo tra vitamina B3 e cellule killer naturali: ecco cosa dice la ricerca
Prima della nuova ricerca, i tentativi di altri team di utilizzare le infusioni di cellule killer naturali come terapia per leucemie, linfomi e altre neoplasie del sangue, non erano sempre efficaci. I medici si sono trovati di fronte a un problema: alcune persone semplicemente non hanno risposto al trattamento sperimentale, che è stato offerto dopo il fallimento della terapia standard.
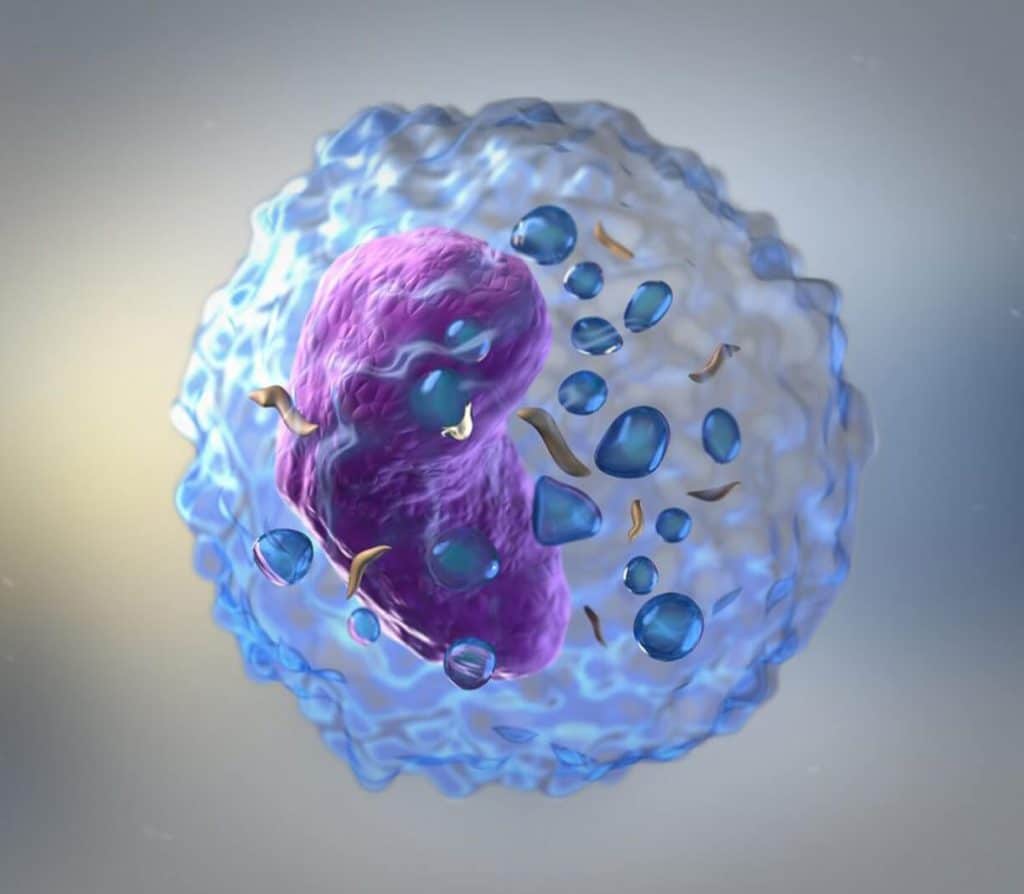
Ora, con una visione unica di questa forma emergente di trattamento del cancro, gli scienziati medici della Divisione di Ematologia, Oncologia e Trapianti dell’Università del Minnesota, hanno ideato un modo per aumentare l’efficacia delle cellule killer naturali, migliorando il loro ruolo come agente terapeutico. . L’approccio innovativo ha potenziato l’impatto delle cellule killer naturali e ha determinato remissioni in pazienti affetti da tumori altrimenti recalcitranti.
“Il trasferimento adottivo di cellule killer naturali allogeniche ha dimostrato il potenziale di indurre remissioni nelle leucemie e nei linfomi recidivanti o refrattari”, scrive il dottor Frank Cichocki e colleghi nella rivista.
“Sono necessarie strategie per migliorare la sopravvivenza e la funzione delle cellule natural killer per migliorare l’efficacia clinica. Abbiamo dimostrato che le cellule natural killer coltivate ex vivo con interleuchina-15—IL-15—e nicotinamide hanno mostrato un’induzione stabile di l-selettina, una molecola di adesione linfocitaria importante per l’homing dei linfonodi.”
La nicotimamide aiuta il corpo a trasformare il cibo in energia ed è chimicamente parte dei coenzimi NAD+ e NADH, che sono fondamentali nelle reazioni di riduzione dell’ossidazione in tutto il corpo. Tra queste attività c’è la produzione di adenosina trifosfato, ATP, che alimenta i processi cellulari e metabolici.
Nel 1937, i ricercatori scoprirono che la malattia sistemica conosciuta come pellegra è causata da una carenza di niacina. Il disturbo è caratterizzato dalle tre D: demenza, diarrea e dermatite. Senza trattamento, che consiste semplicemente nel fornire niacina, la pellegra può essere fatale.
La scelta da parte del team della nicotinamide come potenziatore delle cellule killer naturali mette in luce il comune composto solubile in acqua e dimostra come possa potenziare l’attività antitumorale delle cellule killer naturali. Queste cellule sono linfociti e membri del sistema immunitario innato, la prima risposta del corpo alle malattie invasive. Il compito delle cellule killer naturali è aiutare a controllare il cancro e i microbi invasivi.
Gli scienziati, nel frattempo, che stanno sviluppando la terapia sperimentale, hanno semplicemente potenziato queste cellule per aiutarle ad attaccare il cancro in modo più efficiente. Se ulteriori test dimostreranno l’efficacia di questo metodo – e gli scienziati di Minneapolis saranno convinti di essere sulla strada giusta – allora emergerà un nuovo approccio innovativo per il trattamento dei tumori del sangue.
“Abbiamo condotto il primo studio clinico di fase 1 sull’uomo testando il trasferimento adottivo di cellule natural killer espanse ex vivo con IL-15 e nicotinamide combinati con anticorpi monoclonali in pazienti con linfoma non Hodgkin recidivante o refrattario e mieloma multiplo”, ha affermato Cichocki. in Medicina Traslazionale Scientifica .
Nel piccolo studio preliminare, Cichocki e collaboratori hanno scoperto che la nicotinamide non solo migliora l’attività delle cellule killer naturali, ma aumenta la loro persistenza nel sangue e rafforza la capacità di queste cellule non solo di dare la caccia alle cellule tumorali, ma di distruggerle facilmente.
La combinazione di cellule natural killer potenziate dalla nicotinamide e il trattamento con anticorpi monoclonali si è rivelata sicura in 30 pazienti, di cui 20 con linfoma non Hodgkin recidivante o difficile da trattare. Dei 19 pazienti affetti da linfoma non Hodgkin, 11 hanno dimostrato una risposta completa e tre hanno avuto una risposta parziale entro 28 giorni dal trattamento. Il team ha scoperto che la nicotinamide sembra proteggere le cellule killer naturali dallo stress ossidativo, migliorando al tempo stesso la loro capacità di raggiungere i linfonodi.
“Le alte frequenze di CD62L erano associate a un elevato fattore di trascrizione forkhead box O1, o FOXO1”, ha osservato Cichocki, riferendosi alla molecola homing, CD62L, che guida le cellule killer naturali ai linfonodi. Come fattore di trascrizione, FOXO1 è responsabile della regolazione di un ampio numero di geni coinvolti nel metabolismo, nella progressione del ciclo cellulare e nella morte cellulare programmata.
Nei tumori, FOXO1 agisce come un soppressore delle cellule maligne principalmente a causa dei suoi ruoli che promuovono la morte cellulare programmata – l’apoptosi – e inibiscono la progressione del ciclo cellulare, l’angiogenesi e le metastasi.
“La nicotinamide ha promosso la stabilità di FOXO1 prevenendo la degradazione del proteasoma”, ha aggiunto l’autore principale dello studio Cichocki. “Le cellule natural killer coltivate con nicotinamide hanno mostrato cambiamenti metabolici associati ad un elevato flusso di glucosio e protezione contro lo stress ossidativo.”
Anche le cellule natural killer trattate con nicotinamide in laboratorio hanno dimostrato una maggiore capacità di generare una risposta infiammatoria e tossica contro le cellule tumorali. Cichocki e colleghi hanno concluso che i loro risultati suggeriscono che la nuova strategia di trasferimento dovrebbe essere studiata ulteriormente in studi clinici più ampi.
In un altro studio, i ricercatori del Karolinska Institutet hanno trovato nei campioni di pazienti affetti da linfoma cutaneo un elevato numero delle cosiddette cellule natural killer, un’importante cellula anti-linfoma. Tuttavia, le cellule erano immature e meno attive. Una futura terapia potrebbe essere quella di ripristinare la loro funzione localmente. Lo studio è stato pubblicato su Frontiers in Immunology.
Il linfoma cutaneo è un tipo di cancro della pelle grave, ma meno studiato. Le fasi iniziali della malattia hanno una buona prognosi, ma nelle fasi avanzate la prognosi è sfavorevole. Il trattamento è raramente curativo e vi è un urgente bisogno di nuove opzioni terapeutiche.
Le cellule Natural Killer (NK) sono importanti cellule anti-linfoma. Nello studio i ricercatori hanno trovato un numero elevato di cellule NK in campioni di pelle di pazienti con linfoma cutaneo. Tuttavia, queste cellule erano immature e con attività compromessa. Inoltre, i ricercatori hanno scoperto che strette interazioni cellulari con le cellule del linfoma inducono il fenotipo funzionale compromesso delle cellule NK.
“Questi risultati sono interessanti e suggeriscono che il potenziamento dell’attività delle cellule NK della pelle nel linfoma cutaneo potrebbe essere un potenziale approccio immunoterapeutico”, afferma la ricercatrice principale Hanna Brauner, professoressa associata presso il Dipartimento di Medicina di Solna.
Nella fase successiva gli autori mirano a delineare i fattori necessari per un rigetto efficace del linfoma o per una cura locale. Pertanto, prima e durante il trattamento verrà eseguita un’indagine dettagliata della pelle di pazienti con linfoma cutaneo, comprese le cellule del linfoma , le cellule immunitarie anti-linfoma e altre cellule nel microambiente tissutale.
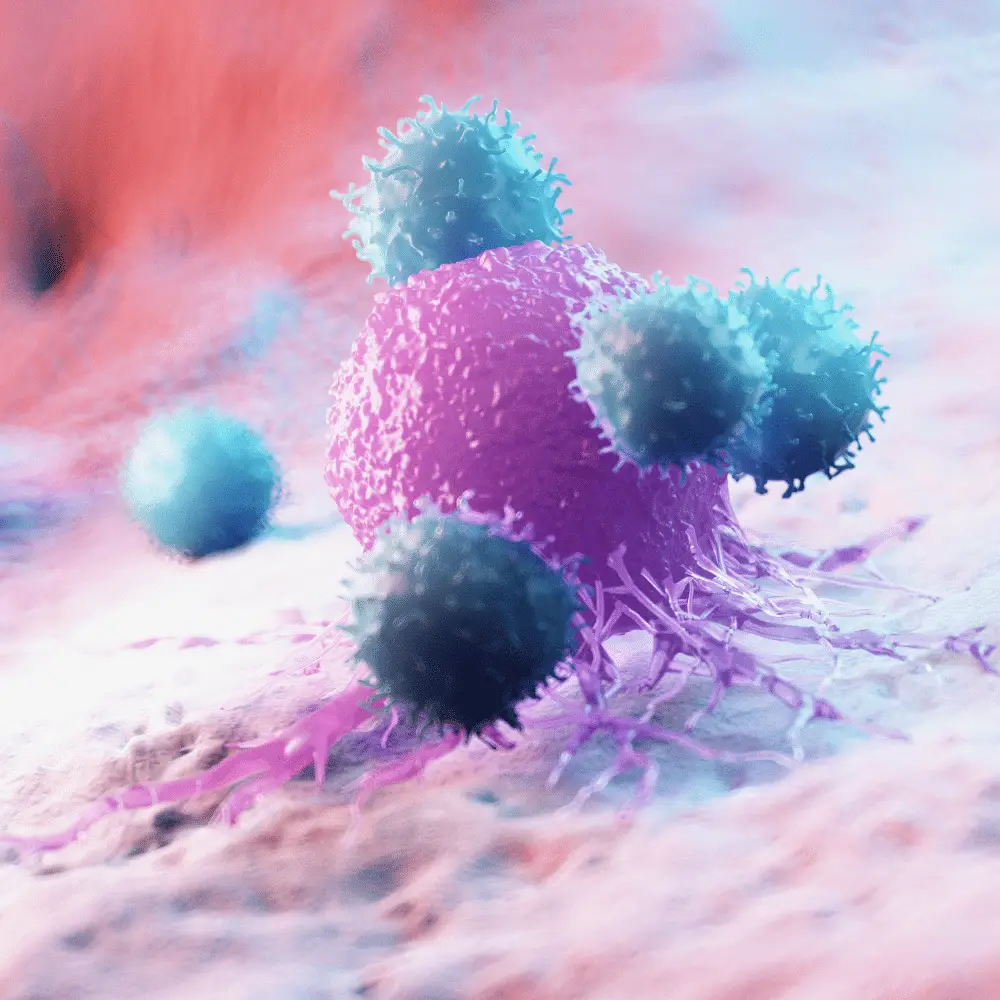
Si spera che le nuove conoscenze acquisite possano essere applicate anche per aumentare la comprensione dei meccanismi fisiopatologici di altri sottotipi di linfoma meno accessibili.
In un ulteriore studio dell’Università di Lund in Svezia, i ricercatori hanno scoperto che i cambiamenti metabolici influenzano il modo in cui si formano le cellule del sangue durante lo sviluppo embrionale. Hanno scoperto un interruttore metabolico precedentemente sconosciuto con un ruolo chiave nel modo in cui si sviluppano diversi tipi di cellule del sangue.
Ciò significa che la formazione delle cellule del sangue può essere indirizzata verso la produzione di cellule killer naturali in laboratorio da utilizzare infine in un nuovo trattamento antitumorale.
Circa 2 miliardi di cellule killer naturali circolano nel nostro corpo e svolgono un ruolo importante nella difesa dell’organismo contro il cancro e le infezioni. Ciò ha portato i ricercatori a credere che le cellule killer naturali possano essere utilizzate nel trattamento immunoterapico per quelle stesse malattie. Pertanto, dobbiamo capire come queste cellule antitumorali vengono inizialmente prodotte a partire dalle cellule staminali del sangue originate nell’embrione.
“Prendendo cellule dal tessuto di un adulto, ad esempio un follicolo pilifero o una cellula della pelle, possiamo riprogrammarle in uno stato simil-embrionale, le cosiddette cellule iPS, cellule staminali pluripotenti indotte. A causa dello stato embrionale, queste cellule possono poi si sviluppano in diversi tipi di cellule del corpo, comprese le cellule del sangue “, afferma Niels-Bjarne Woods, professore associato all’Università di Lund e autore corrispondente dello studio.
Nel nostro sistema per generare cellule del sangue dalle cellule iPS, il team di ricerca ha trovato un interruttore metabolico che può attivare la generazione di specifici tipi di cellule del sangue e di conseguenza aumentare la produzione di cellule killer naturali.
“Nelle nostre cellule ci sono mitocondri che funzionano come centrali elettriche, dove le reazioni chimiche forniscono energia alle cellule. Nutrendo le cellule con sostanze diverse potremmo influenzare la produzione di energia e influenzare quali tipi di cellule del sangue si sviluppano. Abbiamo eseguito gli studi in prima in laboratorio, e poi hanno confermato il risultato sugli animali, ottenendo risultati simili”, afferma Niels-Bjarne Woods.
L’aumento dell’attività nei mitocondri ha portato a livelli sostanzialmente più elevati di cellule killer naturali. Ciò dimostra che il metabolismo è un importante regolatore dello sviluppo del sangue durante la fase embrionale.
“Utilizzando fattori metabolici, abbiamo identificato come controllare la produzione di cellule del sangue specifiche dalle cellule iPS. Abbiamo intenzione di modificare le cellule killer naturali per colpire e distruggere tumori specifici. Il trapianto di cellule killer naturali geneticamente modificate dalle cellule iPS è la prossima grande speranza per terapie antitumorali”, conclude Niels-Bjarne Woods. “Abbiamo appena reso la produzione di cellule killer naturali più on-demand.”
Le cellule natural killer non uccidono solo le cellule tumorali o le cellule infettate da virus, ma mediano anche un compromesso tra la guarigione delle ferite e la difesa batterica nelle ferite della pelle. Se il processo di guarigione viene accelerato, la difesa immunitaria viene indebolita, hanno dimostrato ora i ricercatori dell’Università di Zurigo. Ciò è rilevante nel trattamento delle lesioni cutanee e nella lotta ai germi resistenti agli antibiotici.
Le cellule natural killer sono un tipo specifico di cellule immunitarie. Riconoscono le cellule anormali del corpo come le cellule tumorali o le cellule infette da virus e le eliminano. Un gruppo di ricerca internazionale guidato da Christian Stockmann, professore all’Istituto di anatomia dell’Università di Zurigo (UZH), ha ora scoperto che le cellule killer hanno un’altra funzione sorprendente: gestiscono la guarigione delle ferite nella pelle.
“Siamo riusciti a modificare geneticamente queste cellule nei topi per accelerare la crescita dei vasi sanguigni e far sì che le ferite della pelle si chiudano più rapidamente. Tuttavia, questo ha l’effetto di indebolire la difesa immunitaria, aumentando così la suscettibilità alle infezioni batteriche”, spiega Stockmann.
La ricerca biomedica si è concentrata fortemente sulla ricerca di modi per influenzare i processi di guarigione delle ferite. Soprattutto, i ricercatori hanno cercato metodi per stimolare e accelerare la formazione di nuovi vasi sanguigni, direttamente o indirettamente, influenzando la risposta immunitaria . Tuttavia Stockmann consiglia cautela in questo caso: “I nostri risultati mostrano che potrebbe esserci un aumento del rischio di infezione associato a tali approcci.”
Un’altra questione aperta è la misura in cui le cellule killer naturali influenzano non solo la velocità ma anche la qualità della guarigione delle ferite, ad esempio la composizione del tessuto connettivo o la rigenerazione dei follicoli piliferi, delle ghiandole e di altri componenti della pelle. “La domanda più interessante è come possiamo accelerare la guarigione delle ferite rafforzando allo stesso tempo la difesa immunitaria contro le infezioni”, afferma Stockmann.
L’immunologo e anatomista vede anche un ulteriore potenziale nelle cellule killer. I moderni trattamenti contro il cancro utilizzano già agenti terapeutici che attivano e stimolano le cellule killer in modo che uccidano le cellule tumorali in modo più aggressivo. “I nostri dati suggeriscono che questi tipi di agenti possono essere efficaci anche contro le infezioni batteriche, qualcosa che dovrebbe sicuramente essere esplorato ulteriormente alla luce del numero crescente di batteri resistenti agli antibiotici”, afferma Stockmann.
Le cellule natural killer comunicano continuamente con altre cellule di difesa e influenzano la loro attività. Per fare questo, secernono sostanze messaggere note come citochine. Nel loro studio i ricercatori si sono resi conto che le cellule killer si infiltrano anche nelle lesioni cutanee con livelli di ossigeno molto bassi (ipossia). In tali tessuti, le cellule killer modificano la loro espressione genetica per adattarsi alla mancanza di ossigeno. I fattori di trascrizione inducibili dall’ipossia (HIF) sono responsabili di questo adattamento. Nei topi, se manca uno di questi fattori chiamato HIF-1α, il rilascio di alcune citochine viene compromesso.
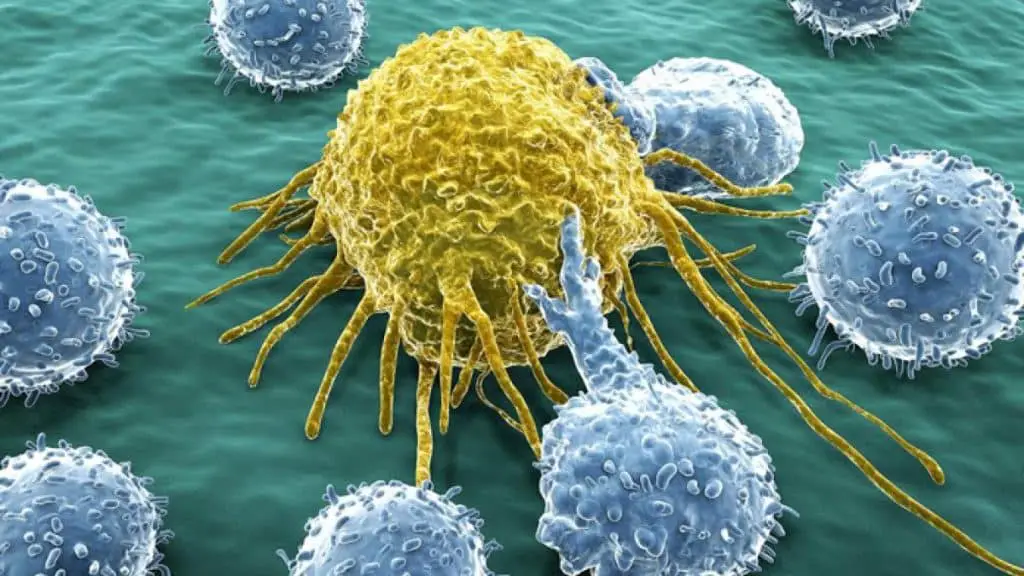
In risposta, i vasi sanguigni crescono più rapidamente nella pelle, accelerando così la guarigione delle ferite. Allo stesso tempo, però, la lotta contro le infezioni batteriche è limitata. L’equilibrio pende quindi a favore della guarigione delle ferite, ma con un rischio di infezione più elevato.
Le cellule T effettrici e killer sono tipi di cellule immunitarie. Il loro compito è attaccare agenti patogeni e tumori. Queste cellule possono anche inseguire cellule normali causando malattie autoimmuni. Ma, se sfruttati correttamente, possono distruggere le cellule tumorali che resistono al trattamento.
Gli scienziati del St. Jude volevano capire come vengono controllate queste cellule T. Hanno esaminato i potenziatori , sequenze di DNA che, quando legate a determinate proteine, determinano il modo in cui i geni vengono attivati o disattivati.
Gli scienziati hanno scoperto che i potenziatori di un gene chiamato Foxp3 funzionano in coppia per tenere sotto controllo le cellule T effettrici e killer. Gli esaltatori che lavorano insieme sono essenziali.
“Questi potenziatori vanno insieme come le mani sinistra e destra”, ha detto Yong Feng, Ph.D., del St. Jude Immunology. “Lavorano insieme in modi diversi per frenare le cellule T effettrici e killer, svolgendo un ruolo fondamentale nel modo in cui il sistema immunitario si assicura di attaccare solo il bersaglio giusto.”