Una ricerca dell‘Università di Melbourne ha scoperto come le cellule immunitarie retiniche cambiano durante il diabete, il che può portare a nuovi trattamenti che possono essere utilizzati fin da una fase iniziale della malattia, ben prima di qualsiasi perdita della vista.
Il nuovo studio potrebbe costituire la base per lo sviluppo di terapie che cambiano la vita e che limitano l’impatto della malattia oculare diabetica, una condizione che potrebbe potenzialmente colpire circa 1,7 milioni di australiani, affetti da diabete di tipo 1 e di tipo 2.
I risultati della ricerca sono stati pubblicati sulla rivista scientifica PNAS.
Cellule immunitarie retiniche: qualche accenno sulla ricerca
“Fino a poco tempo fa, si pensava che le cellule immunitarie del sistema nervoso esistessero tranquillamente, rispondendo solo quando si verificavano lesioni o malattie. La nostra scoperta amplia la nostra conoscenza di ciò che fanno queste cellule e mostra un meccanismo molto insolito mediante il quale i vasi sanguigni sono regolati. Per la prima volta, le cellule immunitarie sono state implicate nel controllo dei vasi sanguigni e del flusso sanguigno”, ha affermato la co-autrice, la professoressa Erica Fletcher.
Secondo Diabetes Australia, quasi tutti i soggetti con diabete di tipo 1 e oltre il 60% di quelli con diabete di tipo 2 svilupperanno una qualche forma di malattia oculare diabetica entro 20 anni dalla diagnosi. Con altre 280 persone che sviluppano la malattia ogni giorno, la svolta ha importanti implicazioni.
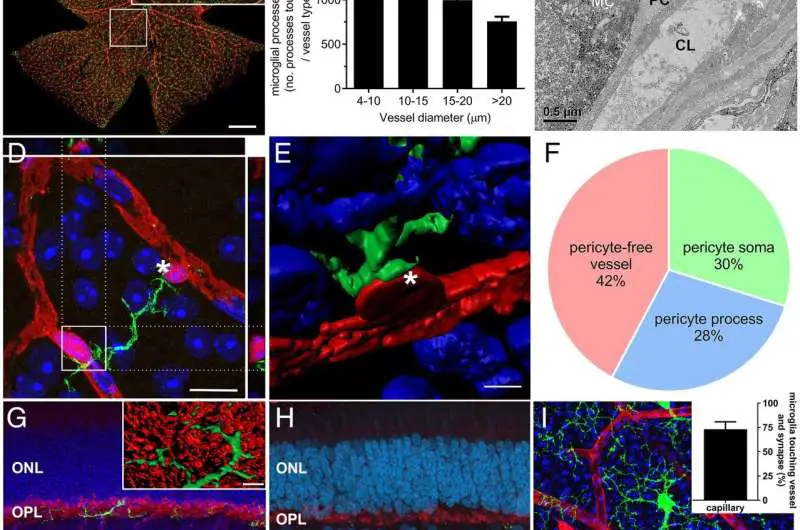
Il team di ricerca ha scoperto che un tipo specifico di cellula immunitaria, chiamata microglia, contatta sia i vasi sanguigni che i neuroni nella retina ed è in grado di modificare il flusso sanguigno per soddisfare le esigenze dei neuroni.
La Professoressa Fletcher e il coautore, il dott. Andrew Jobling, hanno identificato il segnale chimico attraverso il quale le cellule immunitarie comunicano con i vasi sanguigni e hanno dimostrato che la regolazione delle cellule immunitarie dei vasi sanguigni è anormale nel diabete, una malattia nota per colpire i vasi sanguigni nel occhio. Gli studi hanno utilizzato modelli animali preclinici e una serie di metodi di imaging che hanno permesso ai ricercatori di vedere le cellule immunitarie retiniche in un occhio vivente.
“Abbiamo anche isolato le cellule immunitarie retiniche da gruppi di animali normali e diabetici e analizzato il loro genoma per identificare come queste cellule comunicano con i vasi sanguigni. Infine, abbiamo utilizzato una serie di strumenti farmacologici per esaminare come i vasi sanguigni cambiano in risposta all’attivazione del sistema immunitario retinico“, ha spiegato il dottor Jobling.
Fletcher ha affermato che i risultati evidenziano un nuovo modo di controllare e potenzialmente prevenire i cambiamenti retinici nel diabete.
“Questa scoperta ha anche implicazioni per la nostra comprensione di altre malattie della retina e del cervello. Sebbene solo in una fase iniziale, questi risultati suggeriscono un nuovo modo per comprendere le malattie vascolari del cervello con implicazioni per la nostra conoscenza dell’ictus e del morbo di Alzheimer“, ha dichiarato la scienziata.
“È importante sottolineare che siamo stati in grado di dimostrare che in una fase iniziale del diabete, prima che ci fossero cambiamenti visibili nella parte posteriore dell’occhio, i vasi sanguigni sono anormalmente stretti, influenzando il modo in cui forniscono i neuroni della retina. Le cellule immunitarie retiniche erano implicate in questa anomalia vascolare precoce, coinvolgendole come un nuovo bersaglio terapeutico per controllare i primi cambiamenti nella retina nel diabete”.
Si spera che i risultati aiutino a sviluppare nuove terapie per ridurre gli effetti delle condizioni vascolari della retina e del cervello. Queste condizioni includono diabete, morbo di Alzheimer e condizioni vascolari come ictus o occlusioni vascolari retiniche.