Circa un quarto delle diagnosi di cancro al seno ricorrenti positivi al recettore degli estrogeni (ER+) perde l’espressione di ER, il che li rende resistenti alla terapia endocrina e in grado di crescere incontrollati. Un team di ricercatori del Baylor College of Medicine ha studiato come queste cellule perdono il loro ER e hanno rilevato un meccanismo che non solo spiega il processo ma offre anche possibilità di superamento esso.
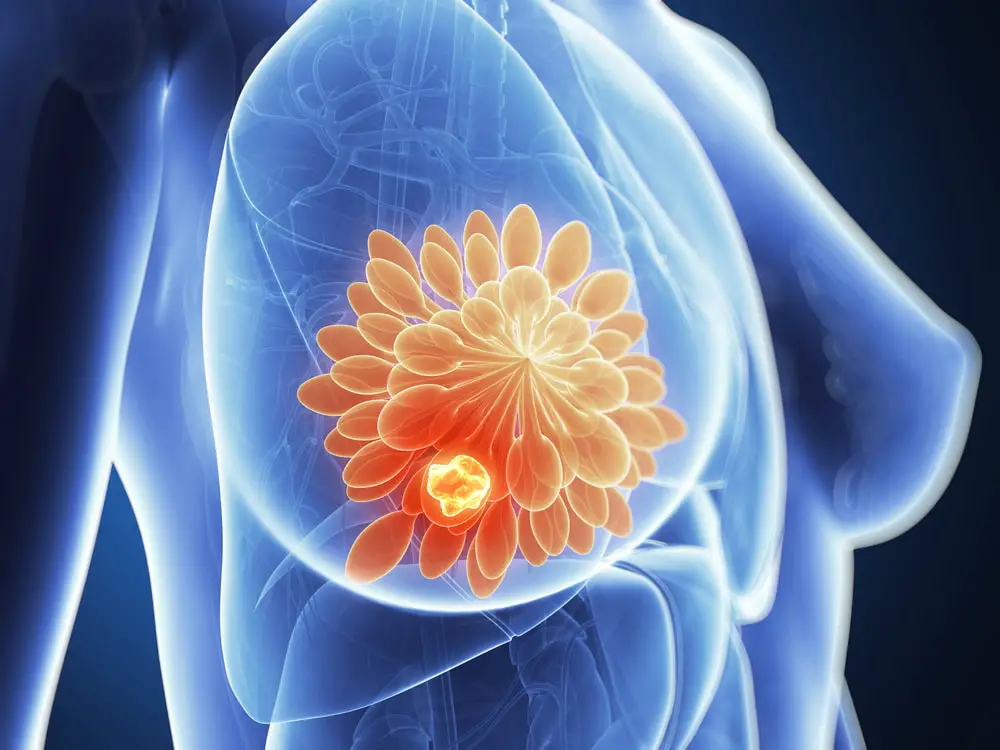
I risultati dello studio sono stati pubblicati negli Atti della National Academy of Sciences.
Cancro al seno: ecco perché le cellule cancerose diventano resistenti ai trattamenti
Precedenti ricerche hanno dimostrato che alti livelli di collagene XII possono innescare la diffusione delle cellule del cancro al seno dal tumore ad altre parti del corpo, in un processo noto come metastasi.

“Per anni, il nostro obiettivo è stato quello di risolvere il complesso puzzle della progressione del cancro al seno per capire come i giocatori interagiscono tra loro per conferire resistenza alla terapia e crescita persistente”, ha affermato l’autore corrispondente Dr. Weei-Chin Lin, professore di medicina —ematologia e oncologia e di biologia molecolare cellulare a Baylor. “Il nostro obiettivo è superare questo ostacolo per ripristinare l’espressione del recettore ER in questi tumori in modo che diventino nuovamente suscettibili alla terapia, offrendo ai pazienti una migliore possibilità di guarigione”.
Due proteine cellulari note come 14-3-3τ e ERα36 sono state precedentemente implicate nello sviluppo della resistenza del cancro al seno alla terapia endocrina .
“Lavorando con un modello murino di cancro al seno umano ER+, siamo stati sorpresi di scoprire che la sovraespressione di 14-3-3τ in questi tumori ha portato tutte le cellule tumorali a diventare ER-negative (ER-)”, ha affermato Lin, un membro del Dan L Duncan Comprehensive Cancer Center. “Ricordo ancora il giorno in cui ho visto i dati. Il cambiamento è stato drammatico: tutti i tumori avevano perso il loro pronto soccorso”.
Studiare il meccanismo nei modelli animali sarebbe laborioso, dispendioso in termini di tempo e costoso, quindi i ricercatori hanno sviluppato un modello alternativo. La prima autrice Lidija A. Wilhelms Garan, una studentessa del Baylor’s Cancer and Cell Biology Graduate Program che lavora nel laboratorio Lin, ha sviluppato un modello sferoide di cellule di cancro al seno umano che imita la progressione da ER+ a ER- e fornisce uno strumento sperimentale molto utile per indagine futura.
“In una paziente, un tumore al seno può richiedere anni per passare da ER+ a ER-, nel nostro modello animale ci vogliono diversi mesi, ma nel nostro modello sferoide passa da ER+ a ER- in 1 o 2 settimane”, ha detto Garan. Nel modello di sferoide di laboratorio il team ha scoperto che una volta che 14-3-3τ è sovraespresso nelle cellule tumorali nelle giuste condizioni, le cellule aumenteranno i loro livelli di ERα36 e questo è seguito dalla perdita di ER.
Nel modello di sferoide di laboratorio il team ha scoperto che una volta che 14-3-3τ è sovraespresso nelle cellule tumorali nelle giuste condizioni, le cellule aumenteranno i loro livelli di ERα36 e questo è seguito dalla perdita di ER.
“Sono necessari anche altri giocatori molecolari, come AKT e GATA3”, ha affermato Garan. “È importante sottolineare che abbiamo anche scoperto che i fattori prodotti dal microambiente tumorale , che include fibroblasti e cellule immunitarie che fanno parte della massa tumorale e dialogano con le cellule tumorali, sono anche essenziali per la progressione da ER+ a ER-“.
“Sapevamo che 14-3-3τ, ERα36, AKT e GATA3 erano gli attori chiave coinvolti nella trasformazione delle cellule di cancro al seno ER+ in cellule ER-. Qui abbiamo determinato come interagiscono funzionalmente tra loro, tracciando una mappa della strada che porta alla perdita di ER”, ha detto Lin. “Sono molto entusiasta del fatto che con il nostro modello di cancro al seno sferoide ora abbiamo uno strumento prezioso per studiare non solo i cambiamenti cellulari coinvolti nella progressione del cancro al seno, ma anche per testare i farmaci per la loro capacità di inibire il processo che porta alla perdita di ER”.
Anche Yang Xiao del Baylor College of Medicine è stato un autore di questo lavoro.
Secondo l’ISTAT: “Ogni anno, in Italia, quasi 55mila donne ricevono la diagnosi di tumore della mammella. Ben 84% di tali donne presenta la malattia in stadio iniziale e il 9% di queste presenta tumori caratterizzati sia dalla sovraespressione della proteina HER2 (HER2+) sia dalla co-espressione dei recettori ormonali. È questa la fetta di pazienti in cui occorre valutare l’opportunità di somministrare per un anno la terapia adiuvante, cioè subito dopo la chirurgia”.
Paolo Marchetti, professore ordinario di Oncologia all’Università La Sapienza di Roma e presidente della Fondazione per la medicina personalizzata, ha dichiarato: “In questa popolazione il trattamento sistemico adiuvante con la chemioterapia, la terapia ormonale e un anno di terapia biologica con l’anticorpo anti-HER2 trastuzumab rappresenta oggi lo standard di cura ed è in grado di ridurre il rischio di recidiva e di morte”.
“Trastuzumab ha infatti migliorato ma non eliminato il rischio che la malattia si ripresenti. Una percentuale di pazienti infatti continua a recidivare con un picco di incidenza a 18-24 mesi dall’intervento chirurgico, anche se alcune presentano recidive tardive anche a 10 anni di follow-up. L’evento più rilevante dal punto di vista clinico, nel carcinoma mammario operato radicalmente, è proprio la comparsa di recidive a distanza, che si associa a un drammatico peggioramento prognostico”, ha continuato l’esperto.
“Le percentuali di guarigione sono ancora lontane dal teorico 100% a cui, idealmente, vogliamo tendere. Neratinib è già stato approvato in Europa ed è rimborsato in diversi paesi, ma non ancora in Italia. È importante che, anche nel nostro Paese, le pazienti possano accedere quanto prima alla terapia adiuvante estesa per ridurre le possibilità di ricaduta e aumentare la sopravvivenza”, ha specificato Marchetti.
Incoraggiante è il risultato dello studio Rome Trial, promosso dall’Istituto Superiore di Sanità, dall’Università La Sapienza di Roma e dalla Fondazione per Medicina Personalizzata: “Il Rome trial è uno studio clinico che si integra perfettamente in quelli che sono i pilastri principali dell’oncologia di precisione. Il primo pilastro fondamentale è quello convenzionale, ovvero il modello istologico, nel quale vengono effettuate delle valutazioni morfologiche sul tessuto, poi integrate dalla ricerca di fattori predittivi di risposta (ovvero specifiche alterazioni genetiche che predicono la risposta a terapie mirate)”.
“Il secondo pilastro, inserito alcuni anni fa, è quello agnostico, indipendente dal tessuto: quindi se, per esempio, un individuo presenta un tumore con instabilità dei microsatelliti, indipendentemente dalla sede della neoplasia che ha questa alterazione, è possibile ricorrere all’immunoterapia”.
“Entrambi questi modelli si basano su un presupposto fondamentale, ovvero si basano sui risultati di studi clinici che dimostrano che quella determinata alterazione del genoma consente di usare uno specifico farmaco a cui segue un vantaggio terapeutico per il paziente. Tutto ciò non ha nulla a che fare con il terzo pilastro, cioè il modello mutazionale”.
“Nell’ambito del modello mutazionale vengono valutate molte più mutazioni, con lo scopo non solo di individuare un maggior numero di possibili bersagli terapeutici da utilizzare nella cura del paziente, ma anche e soprattutto per capire se si sono instaurati meccanismi di resistenza che possono vanificare la risposta a un determinato tipo di trattamento. Motivo per cui diviene particolarmente importante discutere questi risultati nell’ambito di un MTB, come è stato fatto nel Rome Trial”.
L’obiettivo principale dello studio era quello di dimostrare che una profilazione estesa, discussa nell’ambito di un MTB, consente, grazie alla contaminazione dei saperi dei diversi specialisti coinvolti, di fornire al medico curante di quel paziente informazioni sulla possibile utilizzazione di farmaci specifici che dovrebbero essere più efficaci”, ha spiegato Marchetti.
“I dati raccolti finora dimostrano la validità della valutazione multidisciplinare di profilazioni molecolari estese. Ancora non abbiamo i risultati di efficacia che dovrebbero essere disponibili nella primavera del prossimo anno”.
“L’individuazione di alterazioni genetiche germinali, che possono essere ereditate e passare di generazione in generazione, apre un ombrello protettivo che coinvolge tutta la famiglia con screening a cascata sui diversi membri del nucleo familiare e l’avvio di programmi di prevenzione. Dato tanto più importante se si considera che in altre circostanze quello stesso paziente non avrebbe mai scoperto di avere una sindrome ereditaria non rientrando nelle categorie a rischio secondo i criteri standard”, ha concluso l’esperto.