Un team di scienziati della Johns Hopkins University ha sviluppato un nuovo strumento per prevedere quali individui colpiti da una cardiopatia infiammatoria complessa sono a rischio di arresto cardiaco improvviso. il nuovo approccio è il primo a creare modelli del cuore dei pazienti costruiti da più immagini con la potenza dell’apprendimento automatico (imaging multimediale).
Lo studio è stato pubblicato sulla rivista scientifica Science Advances.
Cardiopatia infiammatoria: ecco cosa promette la nuova tecnologia
“Questa nuova e robusta tecnologia personalizzata ha superato le metriche cliniche nella previsione dell’aritmia futura e potrebbe trasformare la gestione dei pazienti con sarcoidosi cardiaca”, ha affermato l’auteice senior Natalia Trayanova, professoressa di ingegneria biomedica della Johns Hopkins e co-direttrice dell‘Alliance for Cardiovascular Diagnostic and Treatment Innovation.
I medici non dispongono attualmente di nuove tecnologie di precisione per valutare quali pazienti con sarcoidosi cardiaca (cardiopatia infiammatoria), una condizione che causa infiammazione e cicatrici che possono innescare battiti cardiaci irregolari, possano avere un’aritmia dall’esito infausto: questa mancanza purtroppo è la conseguenza del decesso di alcuni pazienti e degli continui interventi invasivi per coloro che sopravvivono. Una recente meta-analisi ha spiegato come circa un terzo dei pazienti con CS riceve un trattamento adeguato.
“C’è un urgente bisogno clinico di strumenti predittivi migliori”, ha specificato Trayanova, che è anche professoressa alla Johns Hopkins School of Medicine. “Alcuni pazienti con cardiopatia infiammatoria muoiono, spesso nel pieno della loro vita, mentre altri hanno un defibrillatore impiantato inutilmente e spesso affrontano le complicazioni, tra cui infezioni, malfunzionamento del dispositivo e shock inappropriati, senza ricevere alcun beneficio reale”.
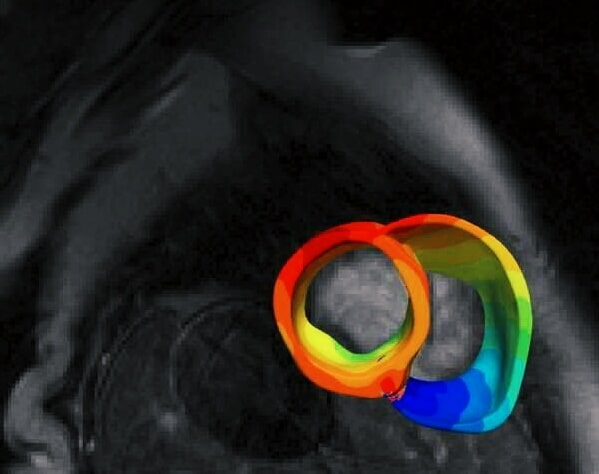
Durante la loro ricerca, gli scienziati della John Hopkins hanno sviluppato modelli digitali tridimensionali del cuore di 45 pazienti affetti da CS trattati al Johns Hopkins Hospital. Per riuscire nell’impresa, si sono serviti di un nuovo approccio che combina i dati di due diversi tipi di scansioni cardiache: risonanza magnetica cardiaca con mezzo di contrasto, che rileva fibrosi o cicatrici, e scansioni PET, che rilevano l’infiammazione.
“Questi modelli cardiaci personalizzati sono i primi nel loro genere ad essere creati con dati provenienti da più modalità di imaging”, ha affermato Trayanova, il cui laboratorio ha sperimentato tecniche per la modellazione meccanicistica del cuore. “Gli effetti combinati di fibrosi e infiammazione non sono mai stati rappresentati in precedenza nei modelli cardiaci”.
Il team ha utilizzato simulazioni al computer per applicare una serie di segnali elettrici in varie posizioni in ciascuno dei modelli e ha raccolto milioni di punti dati che misurano la reazione di ciascun cuore.
Il gruppo di esperti ha sfruttato alcune simulazioni fatte al computer per poter riuscire ad applicare una serie di segnali elettrici in varie posizioni in ciascuno dei modelli e ha raccolto milioni di punti dati che misurano la reazione di ciascun cuore:
“Abbiamo raccolto dati estremamente dimensionali con l’obiettivo di comprendere come le varie caratteristiche delle cicatrici e dell’infiammazione abbiano influenzato il battito cardiaco“, ha affermato Trayanova.
Gli scienziati, in una fase successiva, hanno combinato i dati delle simulazioni meccanicistiche, insieme a dati aggiuntivi del paziente e di imaging, per sviluppare e addestrare un algoritmo per prevedere la probabilità che l’aritmia porti all’arresto cardiaco: “In una malattia complessa come la CS, con cicatrici e infiammazioni, l’apprendimento dei risultati della simulazione meccanicistica ci ha permesso di metterli in relazione con i risultati del mondo reale”, ha aggiunto Julie Shade, autrice principale dello studio e dottore di ricerca.
Lo strumento ha superato significativamente le metriche cliniche standard per la previsione dell’arresto cardiaco nei pazienti con CS. Per migliorare l’algoritmo, gli esperti hanno sviluppato un intenso processo di convalida incrociata, che misura se si possa ottenere la stessa precisione quando vengono rimossi diversi sottoinsiemi di dati, suggerendo come lo strumento potrebbe funzionare sui futuri pazienti. In tutto, il team ha condotto 560 iterazioni di convalida incrociata.
“Siamo stati in grado di stimare l’accuratezza dello strumento per i nuovi pazienti con una confidenza del 95%, il che significa che eravamo relativamente certi che l’algoritmo non sarebbe stato distorto dai dati con cui era stato addestrato e che sarebbe stato quindi accurato se applicato a nuovi pazienti”, ha dichiarato Shade.
Infine, gli scienziati hanno messo a confronto le loro simulazioni con le scansioni delle lesioni nel cuore dei pazienti che erano stati successivamente sottoposti a una procedura per ripristinare i loro battiti cardiaci, scoprendo che le loro intuizioni erano coerenti con i risultati effettivi.
Saranno necessari ampi studi clinici, ma i ricercatori sperano che il loro strumento possa trasformare la gestione dei pazienti con cardiopatia infiammatoria, riducendo il numero di impianti di dispositivi defibrillatori non necessari e garantendo allo stesso tempo la protezione dei pazienti a rischio di morte cardiaca improvvisa.
Secondo Trayanova, l’uso sinergico di modelli personalizzati e apprendimento automatico, che non è mai stato utilizzato in precedenza per affrontare un problema nell’assistenza sanitaria cardiovascolare, potrebbe anche aiutare a risolvere una delle maggiori sfide per l’implementazione dell’intelligenza artificiale nel settore sanitario: la mancanza di dati.
Cardiopatia infiammatoria: cosa succede ai pazienti colpiti da covid19
Un occhio di riguardo meritano i pazienti colpiti da cardiopatia infiammatoria con l’aggravante di essere stati infettati dal covid19. Per ovviare a questo, i cardiologi della John Hopkins University hanno sviluppato un algoritmo che avverte i medici diverse ore prima che i pazienti ricoverati COVID-19 subiscano un arresto cardiaco o coaguli di sangue.(2)
Il predittore COVID-HEART può prevedere l’arresto cardiaco nei pazienti COVID-19 con un tempo medio di preallarme di 18 ore e prevedere la formazione di coaguli di sangue con tre giorni di anticipo. Questa tecnologia è stata sviluppata con i dati di 2.178 pazienti trattati nei cinque ospedali del Johns Hopkins Health System tra il 1 marzo e il 27 settembre.
“È un sistema di allerta precoce per prevedere in tempo reale questi due esiti nei pazienti COVID ricoverati“, ha affermato Trayanova. “Il predittore in continuo aggiornamento può aiutare gli ospedali ad allocare le risorse appropriate e gli interventi adeguati per ottenere i migliori risultati per i pazienti”.
Julie K. Shade, ricercatrice presso il Dipartimento di ingegneria biomedica, ha sviluppato l’algoritmo di apprendimento automatico con più di 100 punti di dati clinici, informazioni demografiche e risultati di laboratorio ottenuti dal registro JH-CROWN che Johns Hopkins ha stabilito per raccogliere dati COVID19 da ogni individuo presente nel sistema ospedaliero.
“Durante l’estate vedrei rapporti aneddotici su Twitter o in pre-stampe di alcune variabili cardiovascolari nei pazienti COVID che i medici avevano trovato che potrebbero essere significativi e li aggiungerei al modello“, ha dichiarato Shade. “Si è evoluto molto quando abbiamo appreso del COVID. Non sapevamo tutto ciò che sarebbe stato importante perché è una malattia così nuova”.
“Ad esempio, il team non aveva previsto che i dati dell’elettrocardiogramma avrebbero giocato un ruolo fondamentale nella previsione della coagulazione del sangue. Ma una volta aggiunti, i dati ECG sono diventati uno degli indicatori più accurati per la condizione”, ha spiegato Trayanova.
Il prossimo passo per i ricercatori sarà quello di sviluppare il metodo migliore per installare la tecnologia negli ospedali per aiutare nella cura dei pazienti COVID-19.
“Lo strumento di previsione di COVID-HEART potrebbe aiutare nel rapido triage dei pazienti COVID-19 in ambito clinico, specialmente quando le risorse sono limitate“, ha affermato Allison Hays, professore associato di medicina presso la Johns Hopkins University School of Medicine e collaboratore clinico del progetto. “Ciò potrebbe avere implicazioni per il trattamento e un monitoraggio più attento dei pazienti COVID-19 per aiutare a prevenire questi scarsi risultati”.
In Italia invece, a fare luce sul problema è stata una ricerca condotta da Marco Metra dell’Università di Brescia, direttore dell’Unità di Cardiologia dell’ASST-Spedali Civili.
“La nostra analisi ha mostrato che i pazienti Covid-19 con concomitante cardiopatia hanno una prognosi estremamente severa, significativamente peggiore di quella già grave dei non cardiopatici con polmonite da Covid-19. Cause principali di mortalità sono state la sindrome da distress respiratorio acuto (Ards), eventi tromboembolici, tra cui l’embolia polmonare, e lo shock settico” spiega Metra .
”
“ Gli studi eseguiti su casistiche cinesi avevano già suggerito la maggiore suscettibilità per polmonite da Covid-19 dei soggetti cardiopatici e la possibilità di un danno cardiaco in corso d’infezione. In questo studio, per la prima volta, sono descritte sia le caratteristiche cliniche che i fattori di rischio per aumentata mortalità di questi pazienti: età, storia d’insufficienza cardiaca, storia d’insufficienza renale, diabete” continua lo scienziato.
“Viene anche confermato il significato prognostico di alcuni semplici parametri laboratoristici quali la creatininemia (parametro del sangue che indica la funzionalità renale , la troponina plasmatica (indice importante per la salute del cuore), la linfopenia (carenza di specifici globuli bianchi”.
Lo studio a coinvolto 99 pazienti colpiti da polmonite con covid19 e con diagnosi pregresse di malattie cardiache: 53 dei soggetti osservati possedevano già problemi cardiaci mentre 46 non avevano una malattia cardiaca concomitante. Tra gli individui cardiopatici coinvolti, il 40% aveva una storia di insufficienza cardiaca, il 36%, una fibrillazione atriale e il 30% una cardiopatia ischemica; 67 anni l’età media con l’81% dei pazienti maschi.
Osservando tutti i casi dello studio, è stato evidenziato che durante il ricovero ospedaliero, il 26% dei pazienti è purtroppo deceduto, il 15% ha avuto eventi tromboembolici, il 19%, una sindrome di stress da respiratorio acuto, il 6 % uno shock settico. Dal confronto tra individui cardiopatici e soggetti sani è emersa la mortalità più alta dei pazienti con cardiopatia, 36% contro il 15% dei non cardiopatici con un tasso di eventi tromboembolici e di shock settico anche questi più elevati: 23 contro 6%, e 11% contro zero.