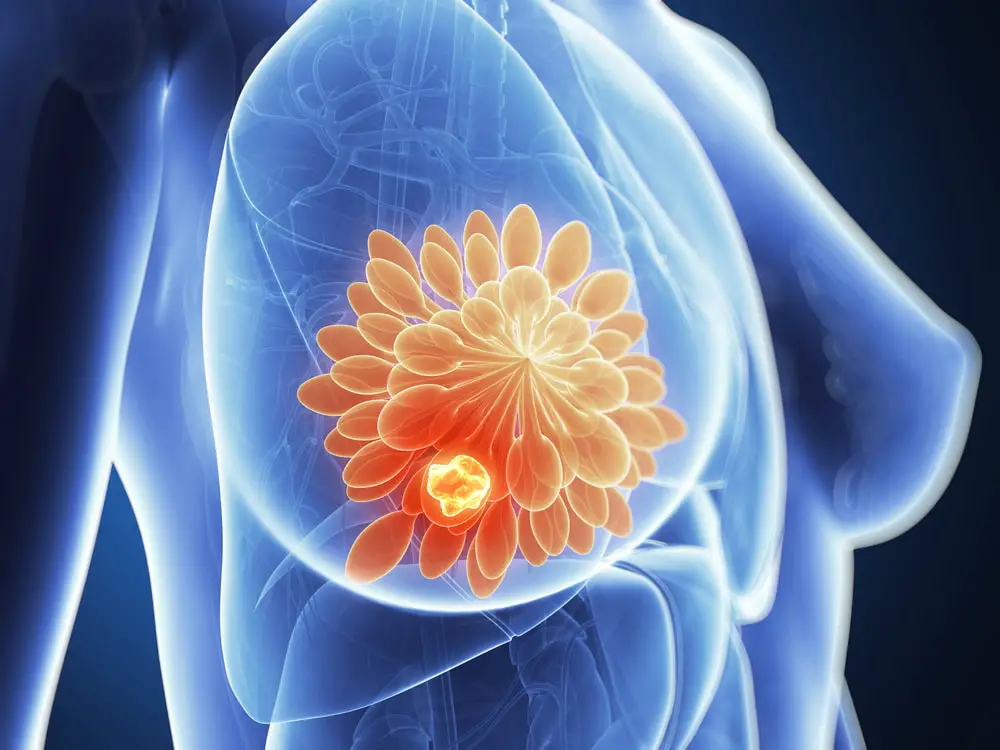
Un farmaco promettente potrebbe portare a un nuovo trattamento per la forma più aggressiva di cancro al seno, che colpisce migliaia di donne ogni anno. Uno studio preclinico condotto dall’Università di Adelaide ha scoperto che il nuovo farmaco inibisce con successo la crescita del cancro al seno triplo negativo senza effetti collaterali tossici.
I risultati della ricerca sono stati pubblicati su Oncogene.
Nuova terapia promettente per il cancro al seno aggressivo
“Si tratta di uno sviluppo entusiasmante nella battaglia contro il cancro al seno triplo negativo, che è la forma più aggressiva della malattia”, ha affermato la professoressa associata Theresa Hickey, esperta di cancro al seno riconosciuta a livello internazionale presso i Dame Roma Mitchell Cancer Research Laboratories dell’Università di Adelaide.
“Attualmente non esiste un trattamento mirato specificamente a questo tipo di cancro al seno, mentre la chemioterapia e, in alcune donne, l’immunoterapia sono le uniche opzioni. I risultati di questo studio mostrano che questo farmaco potrebbe essere la chiave per migliorare i tassi di sopravvivenza “.
Il farmaco è progettato per essere assunto per via orale e agisce prendendo di mira una proteina specifica nel tumore canceroso chiamata CDK9, che accelera la crescita cellulare . Inibendo questa proteina, ferma efficacemente il cancro sul suo cammino.
“Il nostro studio preclinico dimostra che il farmaco è stato in grado di arrestare la moltiplicazione delle cellule tumorali , ma non ha influenzato le cellule normali del tessuto mammario prelevato dalle pazienti. È ancora agli inizi, ma sulla base di queste prove iniziali, riteniamo che inibisca questa proteina potrebbe portare a un trattamento per il cancro al seno triplo negativo e questo nuovo farmaco dovrebbe essere ulteriormente sviluppato”, ha affermato il professore associato Hickey.
Lo studio collaborativo pubblicato su Oncogene ha coinvolto anche il professor Shudong Wang dell’Università dell’Australia Meridionale, che ha sviluppato il farmaco (CDDD11-8) per il trattamento della leucemia mieloide acuta.
“Abbiamo sviluppato CDDD11-8 come inibitore CDK9 potente, selettivo e bioattivo per via orale per la terapia del cancro . Siamo molto entusiasti del suo potenziale terapeutico contro il cancro al seno triplo negativo mostrato dal Professore Associato Hickey,” ha detto il Professore Wang.
In Australia, ogni anno, a circa 2.500 donne viene diagnosticato un cancro al seno triplo negativo. Questo tipo di cancro al seno si verifica più frequentemente nelle donne più giovani. Ha un tasso più elevato di recidiva entro cinque anni e un tasso di mortalità più elevato rispetto ad altri tumori al seno durante questo periodo.
I ricercatori sperano di identificare i biomarcatori che predicono quali tumori al seno tripli negativi risponderanno meglio al farmaco inibitore in modo che questi possano essere utilizzati per selezionare i pazienti per studi futuri.
“Sebbene questo farmaco si stia dimostrando promettente come potenziale trattamento per il cancro al seno triplo negativo, necessita di ulteriori sviluppi prima di poter passare alla sperimentazione umana. Spero che ciò accada entro i prossimi cinque anni, se non prima”, ha affermato il Professore Associato. Succhiotto.
I ricercatori prevedono inoltre di condurre studi futuri per esplorare se questa potenziale terapia potrebbe essere utilizzata per trattare altri tipi di cancro al seno.
“È fondamentale continuare a cercare e valutare a livello preclinico terapie mirate per questa malattia aggressiva e migliorare le prospettive per tutti i pazienti affetti da cancro al seno”, ha affermato il Professore Associato Hickey.
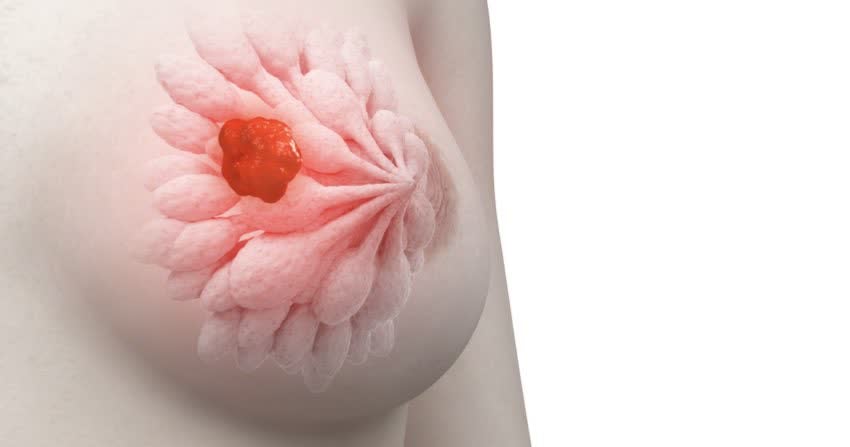
I ricercatori della Cleveland Clinic hanno sviluppato con successo un peptide terapeutico che impedisce alle cellule tumorali aggressive di moltiplicarsi rapidamente. I risultati evidenziano una potenziale nuova strategia per lo sviluppo di trattamenti mirati per il cancro al seno triplo negativo, che attualmente non dispone di opzioni approvate.
I farmaci mirati attaccano direttamente le funzioni delle cellule tumorali, offrendo un approccio più preciso per integrare trattamenti più ampi come la chemioterapia. Un gruppo di ricerca guidato da Ofer Reizes, Ph.D., e Justin Lathia, Ph.D., ha progettato un peptide terapeutico che interrompe i processi molecolari alla base della crescita aggressiva del cancro quando viene somministrato nelle cellule.
Il farmaco ha bloccato la crescita del cancro e ha indotto la morte delle cellule tumorali e ha colpito le cellule cancerose solo nel lavoro preclinico. Lo studio è stato evidenziato in Molecular Cancer Therapeutics .
“È devastante che al momento disponiamo di opzioni così limitate per aiutare le persone affette da cancro al seno triplo negativo “, afferma la dottoressa Reizes, presidentessa di Laura J. Fogarty per la ricerca sul cancro uterino. “Vogliamo che i nostri risultati offrano speranza a questi pazienti e alle loro famiglie e servano da punto di partenza per inserire più trattamenti nella pipeline di sviluppo”.
I peptidi sono proteine corte costituite da aminoacidi che costituiscono i “mattoni” delle proteine più grandi. Le proteine naturali e sintetizzate artificialmente sono comunemente usate per trattare le malattie. Alcuni peptidi vengono utilizzati per integrare le proteine esistenti nel corpo, come l’insulina nelle persone con diabete.
Il peptide in sviluppo, basato su una scoperta della Cleveland Clinic del 2018 , funge da prova di concetto per questo tipo di farmaco per il cancro al seno triplo negativo.
Poiché le cellule del cancro al seno triplo negativo mancano di determinati recettori, i farmaci progettati per trattare altri sottotipi di cancro al seno non funzioneranno. Attualmente non esistono farmaci mirati approvati per il cancro al seno triplo negativo, che costituisce il 15% dei casi di cancro al seno. Per sviluppare nuovi farmaci, i ricercatori dovevano identificare nuovi bersagli efficaci.
Un precedente ricercatore post-dottorato con il team del Dr. Reizes e del Dr. Lathia ha scoperto che Cx26, un tipo di proteina chiamata connessina, forma un complesso molecolare nelle cellule di cancro al seno triplo negativo che le rende più propense a recidivare o diffondersi nel corpo. I ricercatori hanno lavorato per trovare un modo per interrompere quel complesso, che limiterebbe le proprietà cancerose delle cellule.
I primi autori Erin Mulkearns-Hubert, Ph.D., ed Emily Esakov Rhoades, Ph.D., hanno sviluppato un peptide terapeutico. La sequenza del peptide è la stessa della componente Cx26 necessaria alla formazione del complesso. L’obiettivo è saturare il sistema con il peptide e interrompere la capacità delle proteine integrali di legarsi, afferma il dottor Mulkearns-Hubert, ricercatore associato nel laboratorio Lathia.
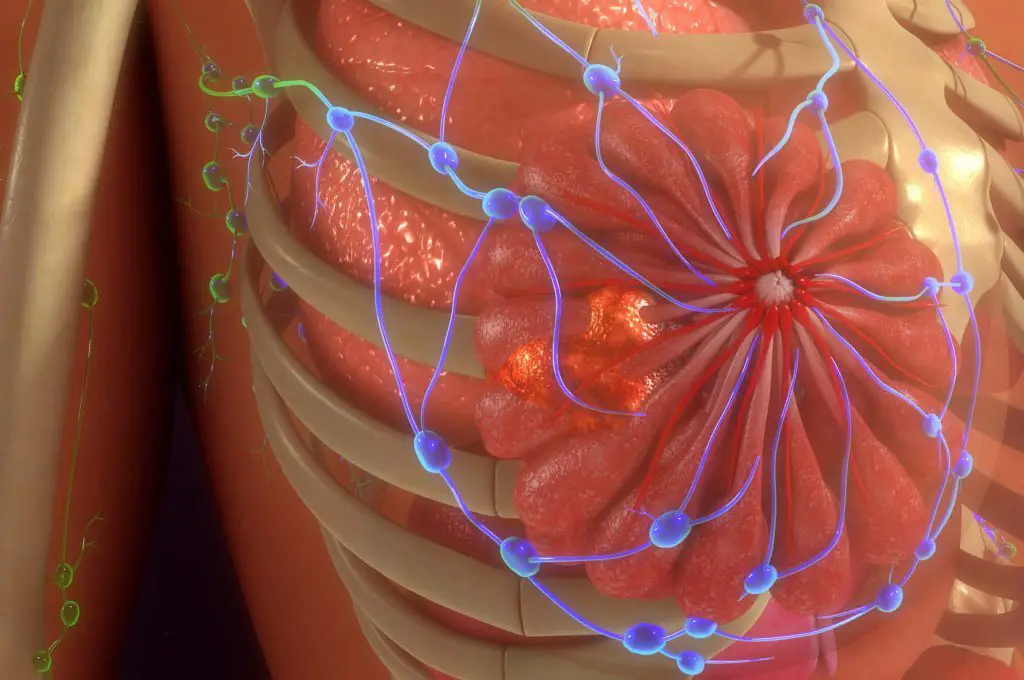
“La progettazione del peptide era in realtà relativamente semplice e ha funzionato magnificamente, rallentando la crescita del tumore nei modelli preclinici”, afferma. “Il cancro al seno triplo negativo rimane un tipo di tumore incredibilmente difficile da trattare, quindi lo sviluppo e la verifica di strategie come quella di questo peptide è fondamentale per andare avanti.”
I ricercatori hanno osservato che il farmaco ha impedito alle cellule staminali tumorali presenti in una capsula di autorinnovarsi, una caratteristica delle cellule tumorali aggressive che supporta la resistenza al trattamento. Il team sta ora lavorando con Cleveland Clinic Innovations per sviluppare il farmaco ed esplorare il potenziale per studi clinici.
I ricercatori del Centro di Regolazione Genomica e dell’Istituto di Oncologia Vall d’Hebron hanno dimostrato che l’inibizione simultanea di due diverse proteine può rappresentare una nuova strategia per affrontare il cancro al seno triplo negativo, la forma di cancro al seno più aggressiva e resistente ai farmaci. I risultati sono stati pubblicati oggi sulla rivista EMBO Molecular Medicine.
Il cancro al seno è il tipo di cancro più comunemente diagnosticato e la quarta causa più comune di morte correlata al cancro nelle donne, con oltre due milioni di casi in tutto il mondo e 685.000 decessi nel 2020.
Circa uno su sette (15%) di questi casi è una forma altamente aggressiva della malattia nota come cancro al seno triplo negativo . La prognosi per il cancro al seno triplo negativo è sfavorevole. La malattia è altamente resistente ai trattamenti esistenti perché le sue cellule non hanno i recettori presi di mira dai farmaci per il cancro al seno.
Recentemente è stato dimostrato che l’enzima LOXL2 guida la crescita del cancro al seno triplo negativo. Un team guidato dalla Dott.ssa Sara Sdelci del Centro di Regolazione Genomica e dalla Dott.ssa Sandra Peiró, insieme ai ricercatori del Gruppo di ricerca traslazionale sul cancro del tratto gastrointestinale superiore dell’Istituto di oncologia Vall d’Hebron, ha effettuato varie analisi per valutare l’idoneità dell’enzima come biomarcatore in grado di prevedere l’esito del trattamento.
Hanno scoperto che l’espressione di LOXL2 poteva solo predire gli esiti dei farmaci che prendono di mira la proteina BRD4, un noto fattore scatenante del cancro. Spinti dall’interesse delle loro scoperte, i ricercatori hanno effettuato ulteriori esperimenti per valutare se LOXL2 e BRD4 potrebbero lavorare insieme per aiutare le cellule del cancro al seno triplo negativo a crescere.
Varie tecniche sperimentali di laboratorio hanno dimostrato che LOXL2 interagisce con una versione di BRD4 all’interno del nucleo. I ricercatori hanno dimostrato che questa interazione modifica l’espressione dei geni e, in definitiva, aiuta le cellule del cancro al seno triplo negativo a crescere. L’inibizione simultanea di entrambe le proteine ha interrotto queste interazioni e ha contribuito a rallentare la crescita del cancro nelle colture cellulari (in vitro) e in tre modelli murini separati (in vivo).
“La nostra indagine approfondita su come le cellule del cancro al seno triplo negativo crescono a livello molecolare ha rivelato un nuovo meccanismo che può essere sfruttato a fini terapeutici. È entusiasmante perché una strategia a doppio attacco che prende di mira entrambe le proteine potrebbe essere combinata con altri trattamenti e trasformare cancro al seno triplo negativo da una malattia con una prognosi molto sfavorevole a una malattia gestibile”, afferma la dottoressa Laura Pascual Reguant, prima autrice dello studio e ricercatrice post-dottorato presso il Centro di Regolazione Genomica di Barcellona.
I risultati hanno importanti implicazioni per una classe sperimentale di farmaci noti come inibitori BET, che si sono mostrati promettenti nella lotta contro il cancro al seno triplo negativo. Gli inibitori BET funzionano compromettendo la funzione di BRD4, ma non sono riusciti a superare la fase di sperimentazione clinica perché le cellule del cancro al seno triplo negativo acquisiscono resistenza. Gli autori dello studio ritengono che il targeting simultaneo sia di BRD4 che di LOXL2 potrebbe aiutare a superare questa resistenza.
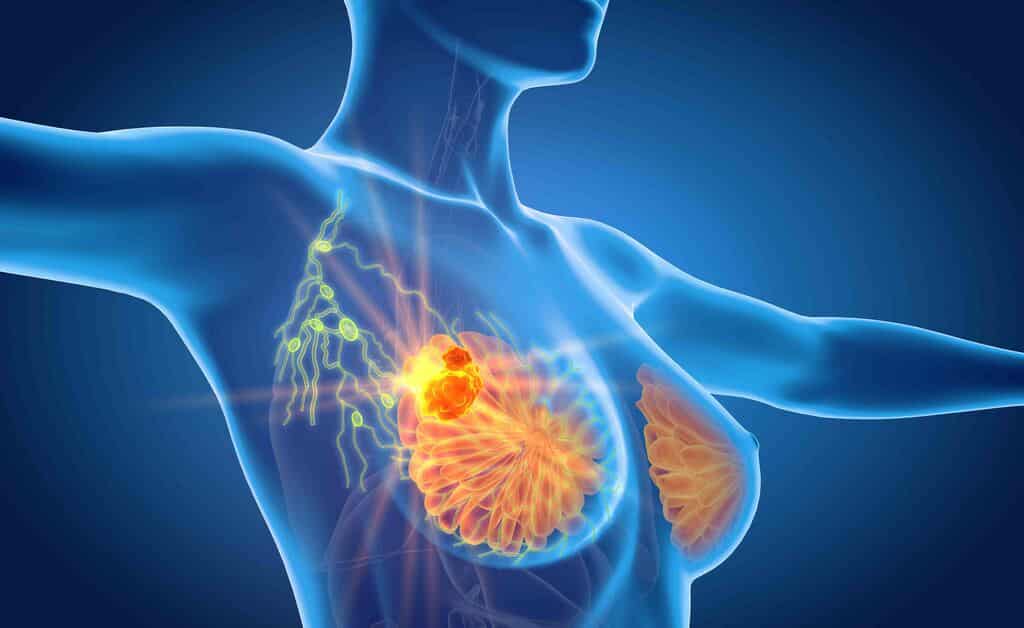
La prossima sfida sarà trovare come colpire in modo sicuro ed efficace entrambe le proteine contemporaneamente. Un modo è combinare gli inibitori esistenti. Diverse versioni di BRD4 sono già prese di mira dagli inibitori del BET in 30 diversi studi clinici, cinque dei quali riguardano il cancro al seno triplo negativo. Esistono anche gli inibitori LOXL2, ma la loro sicurezza ed efficacia nel trattamento del cancro non è stata esplorata. La combinazione di entrambi gli inibitori non è stata testata.
“È necessario fare ancora più lavoro prima che i nostri risultati possano portare benefici ai pazienti, ma qualsiasi progresso nella comprensione dei meccanismi di questa malattia altamente aggressiva è una buona notizia. Mentre continuiamo a far luce su come cresce il cancro al seno triplo negativo, le sfide per la salute che pone potrebbe essere più trattabile di quanto pensassimo inizialmente,” conclude il Dott. Sdelci.