Un team multidisciplinare dell’Università di Alberta sta cercando di capire in che modo il virus del vaiolo delle scimmie (mpox) possa causare sintomi neurologici nelle persone colpite dall’epidemia globale di malattia del vaiolo, dichiarata dall’Organizzazione Mondiale della Sanità nel 2022.
La ricerca è stata pubblicata sulla rivista Proceedings of the National Academy of Sciences.
Come il virus MPOX si infiltra negli astrociti
il team ha utilizzato esperimenti di laboratorio per infettare le cellule cerebrali umane con il virus mpox. Hanno scoperto che il virus MPOX si è infiltrato negli astrociti, un tipo di cellula responsabile della normale funzione cerebrale, innescando una risposta immunitaria estrema.
“Gli astrociti sono le cellule neurali più abbondanti nel cervello”, spiega il primo autore Hajar Miranzadeh Mahabadi, un ricercatore post-dottorato in medicina e titolare di una borsa di studio del Canadian Institutes of Health Research HIV Trials Network. “Abbiamo scoperto che il virus del vaiolo delle scimmie può infettare efficacemente queste cellule e può indurre una sorta di morte delle cellule cerebrali che chiamiamo piroptosi”.
“Stavamo esaminando il potenziale del virus di infettare le cellule cerebrali e vedere quali conseguenze l’infezione potrebbe avere sulle cellule”, afferma il co-investigatore Ryan Noyce, assistente professore di microbiologia medica e immunologia, sottolineando che sono necessari ulteriori studi utilizzando campioni provenienti da pazienti umani, modelli animali e vari ceppi di vaiolo. “I nostri risultati fanno luce sulla possibilità che il virus del vaiolo delle scimmie si infiltri nel cervello e infetti le cellule in alcuni casi.”
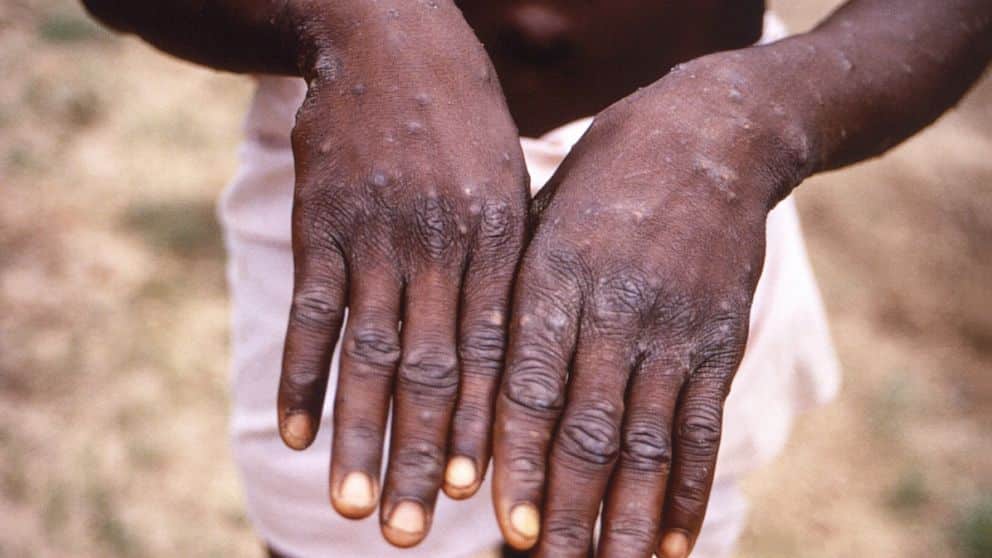
Secondo Health Canada, più di 80.000 persone erano state infettate dal virus del vaiolo al momento in cui è stata dichiarata l’epidemia, e attualmente ci sono circa 1.500 casi confermati in Canada. Il virus si trasmette attraverso la pelle, il contatto sessuale o le goccioline respiratorie e questa epidemia ha colpito principalmente gli uomini che hanno rapporti sessuali con uomini.
I sintomi più comuni includono eruzioni cutanee, febbre e dolori muscolari, ma sono stati osservati sempre più sintomi neurologici come mal di testa, confusione mentale e convulsioni, suggerendo un’infiammazione del tessuto cerebrale.
“L’entità dei casi di virus del vaiolo delle scimmie, in particolare quelli associati a complicazioni neurologiche, ha evidenziato l’urgente necessità di comprendere il potenziale effetto del virus del vaiolo delle scimmie sul sistema nervoso centrale”, afferma Miranzadeh Mahabadi, sottolineando che questo è il primo studio ad esaminare le cellule cerebrali esposte a virus del vaiolo.
Il team di ricerca ha identificato una potenziale strada per il trattamento quando è riuscito a ridurre la morte cellulare nelle cellule infettate dal virus mpox trattandole con dimetilfumarato , un composto approvato in Europa per la psoriasi e utilizzato per trattare la sclerosi multipla negli Stati Uniti e in Canada.
Noyce fa notare che ora ci sono due trattamenti antivirali approvati per la malattia da vaiolo e che in Canada è disponibile anche un vaccino per prevenire la malattia nelle popolazioni vulnerabili.
Miranzadeh Mahabadi prevede di continuare la sua ricerca sul morbo e il cervello e di esaminare perché la malattia sembra essere più grave e ha un tasso di mortalità più elevato tra le persone che hanno anche l’HIV.
Un ampio team internazionale di ricercatori medici ed epidemiologi ha trovato prove che il vaiolo delle scimmie (mpox) circola negli esseri umani dal 2016. Nel loro studio, riportato sulla rivista Science , il gruppo ha utilizzato l’analisi evolutiva bayesiana del virus mpox per dimostrare che la sua genomica la storia include anni di cambiamenti dovuti a infezioni umane.
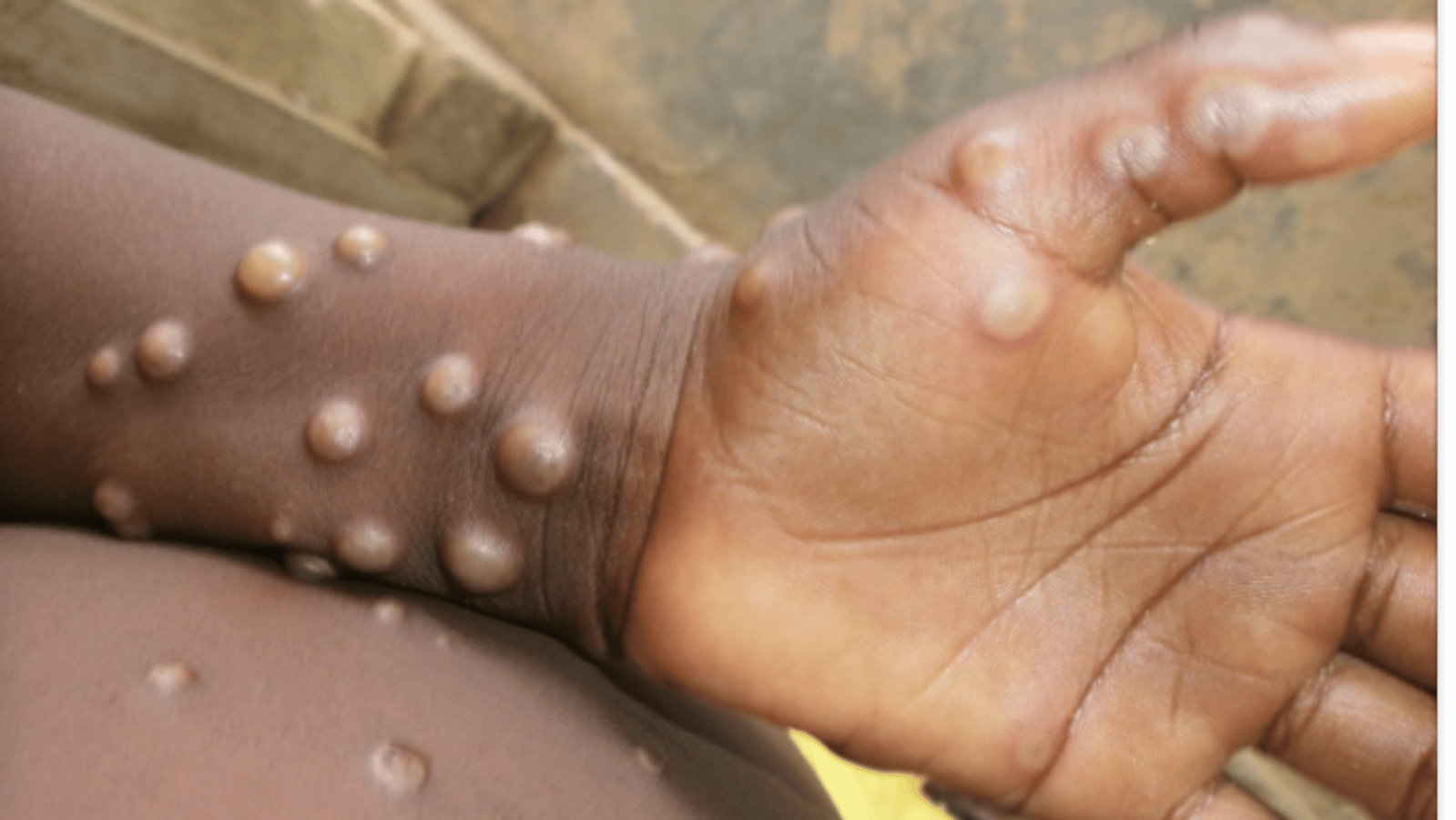
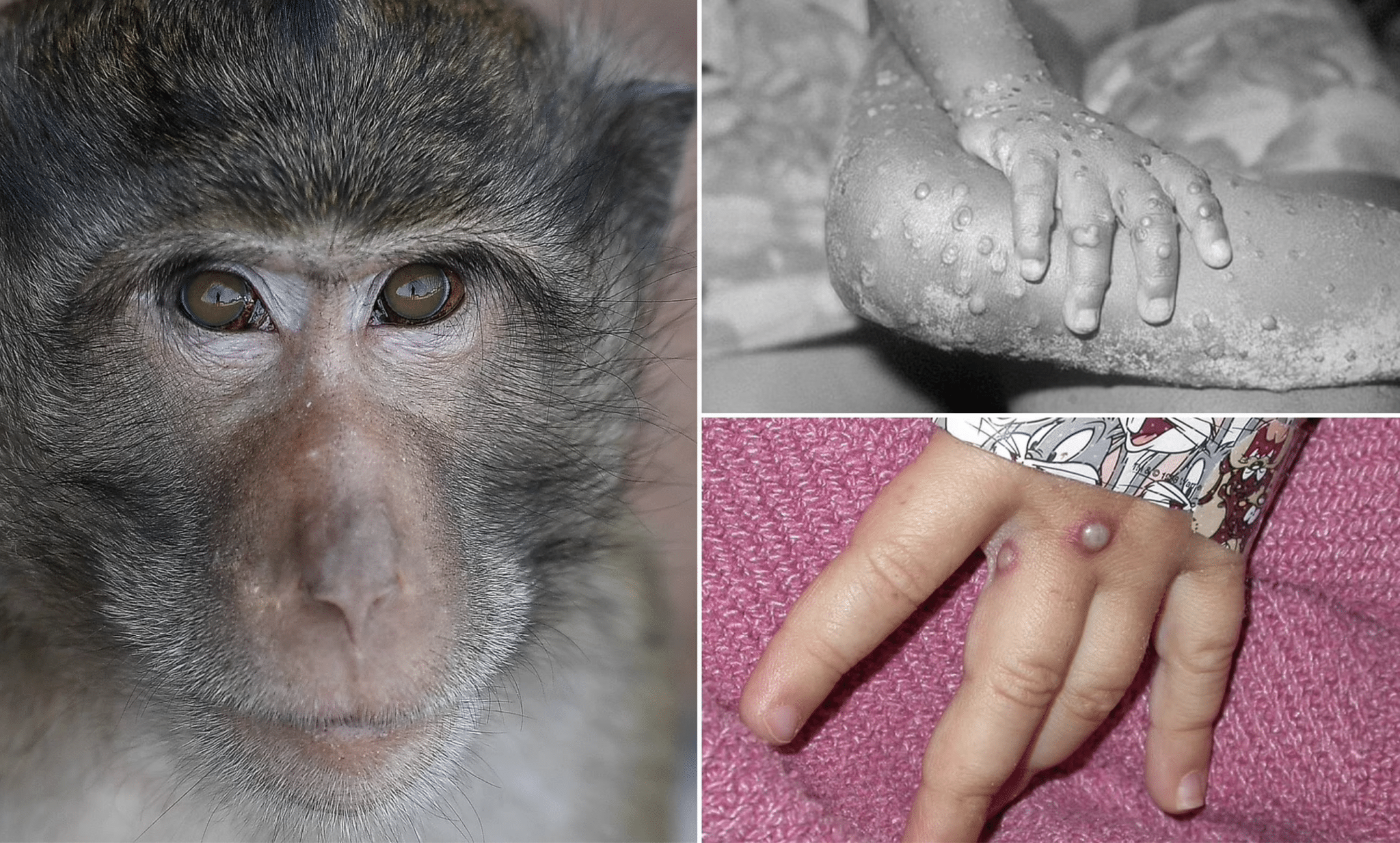
Il Mpox fu identificato per la prima volta negli anni ’50 dopo che una malattia colpì un gruppo di scimmie ricercatrici in Danimarca. Vent’anni dopo, il primo caso fu rilevato in un essere umano in Africa. Nel corso dei decenni successivi, diversi casi della malattia furono osservati negli esseri umani e tutti furono attribuiti alla trasmissione del virus da altri mammiferi.
Poi, nel 2017, si è verificata un’epidemia in Nigeria e nel 2022 si è diffusa in tutto il mondo, dimostrando che il virus si era evoluto per passare da uomo a uomo. In questo nuovo sforzo, il gruppo di ricerca ha esaminato più da vicino il genoma del virus dietro il morbo per saperne di più sulla sua storia evolutiva , in particolare su come si collega alle infezioni umane.
I ricercatori hanno sequenziato il genoma del virus MPOX per saperne di più sulla sua storia evolutiva. Hanno scoperto che il clade IIb era quello che si era diffuso in tutto il mondo. Hanno anche notato che sembrava diverso da altri ceppi visti prima in Africa.
Hanno trovato una mutazione che aveva portato alla produzione di un enzima chiamato APOBEC3, che si è scoperto causare ulteriori mutazioni che alterano le coppie di basi del genoma. Si è scoperto anche che è stato causato da infezioni nell’uomo. Ciò ha permesso al team di tracciare la storia evolutiva del virus quando ha infettato gli esseri umani: hanno trovato tali mutazioni risalenti al 2016 circa, il che suggerisce fortemente che il virus sia trasmissibile tra esseri umani da quell’anno.
Il gruppo di ricerca conclude che esiste una forte probabilità che si verifichino molteplici casi di piccole epidemie di vaiolo che non sono state riconosciute, consentendo al virus di diffondersi sotto il radar. Suggeriscono inoltre che siano istituiti metodi di sorveglianza più forti perché il virus sta ancora mutando rapidamente e potrebbe diventare più mortale.
Gli organoidi della pelle offrono una potente piattaforma per la scoperta di farmaci nella lotta in corso contro il virus precedentemente noto come vaiolo delle scimmie. Un nuovo sistema modello per studiare le infezioni da virus dell’mpox in laboratorio sta fornendo preziose informazioni sui meccanismi di attacco del virus alle cellule della pelle, offrendo un potenziale catalizzatore nella ricerca di farmaci innovativi per combattere questo patogeno emergente.
Un gruppo di ricerca internazionale che comprendeva scienziati KAUST ha dimostrato che la pelle umana coltivata in laboratorio – strutture 3D derivate da cellule staminali chiamate organoidi – può facilitare efficacemente la replicazione attiva del virus mpox, il virus precedentemente noto come virus del vaiolo delle scimmie, che si diffonde rapidamente durante un importante epidemia nel 2022. La ricerca ha portato a pubblicazioni sulle riviste Nature Microbiology e Cell Discovery .
“I ricercatori possono ora utilizzare questo modello per studiare come il virus mpox causa la malattia e per testare nuove terapie”, afferma Intikhab Alam, un bioinformatico che ha contribuito allo studio insieme al collega Roberto Incitti, entrambi del KAUST.
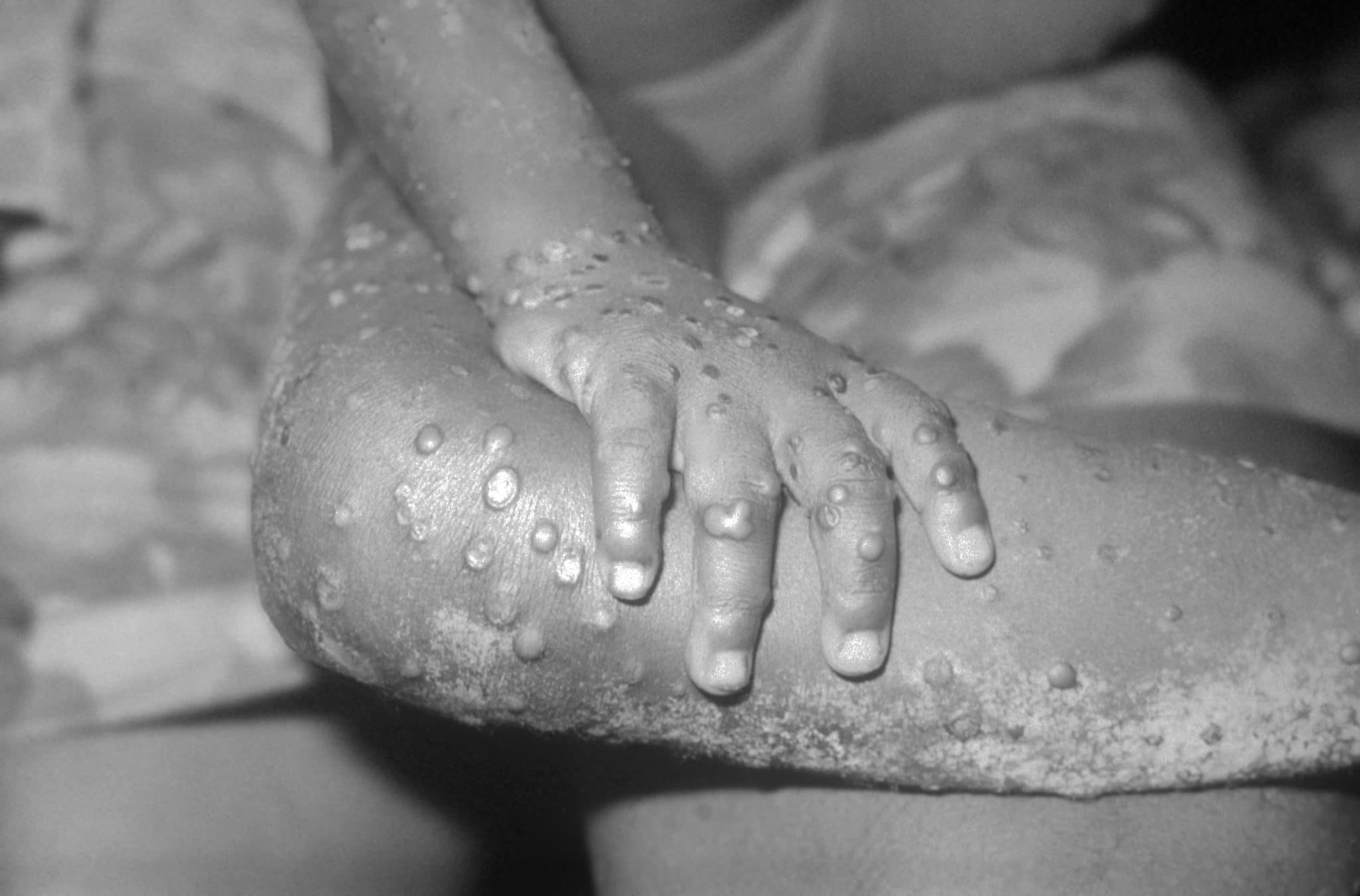
Le persone infettate dal virus mpox sviluppano tipicamente eruzioni cutanee e lesioni cutanee , che spesso portano a cicatrici e deturpazioni, e gli organoidi cutanei coltivati in laboratorio ora aiutano a mostrare il perché.
Alam e Incitti di KAUST hanno collaborato con Qiuwei Abdullah Pan e il suo team dell’Erasmus MC-University Medical Center di Rotterdam per riferire che il virus si insedia all’interno dei cheratinociti, il tipo di cellula predominante nello strato esterno della pelle. Lì, il virus subisce le sue quattro fasi di assemblaggio, un processo che i ricercatori hanno potuto osservare al microscopio ad alta potenza.
Le analisi dell’espressione genica condotte dai ricercatori hanno rivelato che numerosi geni virali si attivano nei giorni successivi all’infezione . Questa attivazione, a sua volta, sembra indurre cambiamenti nelle cellule ospiti, portando ad alterazioni nell’attività di molteplici geni umani associati all’immunità e alla morte cellulare.
Queste alterazioni genetiche probabilmente compromettono la barriera protettiva della pelle, provocando le caratteristiche lesioni osservate nelle persone infette.
Gli effetti osservati potrebbero essere invertiti attraverso l’uso di un farmaco antivirale chiamato tecovirimat. Negli organoidi infetti, questo farmaco si è rivelato altamente efficace nell’arrestare la replicazione del virus e nel contrastare la sovversione delle cellule ospiti.
I risultati confermano il potenziale di inibizione del mpox del tecovirimat, un farmaco approvato per il trattamento delle infezioni legate al virus del vaiolo correlato. Sottolineano inoltre il potenziale del sistema organoide come piattaforma versatile con cui individuare nuove sostanze con proprietà simili.
In particolare, l’impatto della MPOX si estende oltre i problemi legati alla pelle. Nei casi più gravi, il virus può devastare gli organi interni. Lo stesso gruppo di ricerca affiliato a KAUST aveva precedentemente sviluppato un sistema di organoidi renali progettato per studiare le infezioni da mux nei tessuti renali. Altri gruppi hanno studiato le dinamiche dell’mpox all’interno degli organoidi del colon e del cervello.
“Questi studi si completano a vicenda modellando l’infezione in diversi tessuti e con diversi tipi di manifestazioni patologiche”, afferma Incitti.
Collettivamente, gli sforzi nei modelli organoidi – che i ricercatori KAUST e i loro collaboratori stanno ora estendendo anche ad altri sistemi di infezione virale – dovrebbero “aiutare a combattere l’attuale epidemia di mpox e migliorare la preparazione alla pandemia per il futuro”, afferma Incitti.
Un gruppo di ricerca guidato dal professore associato junior Kazuo Takayama (CiRA, Università di Kyoto) e dal professor Kei Sato (Istituto di scienze mediche, Università di Tokyo) ha infettato sperimentalmente cheratinociti umani e organoidi del colon derivati da cellule iPS umane con il virus mpox (MPXV) e caratterizzato la virologia del ceppo MPXV convenzionale e del ceppo epidemico del 2022 (2022 MPXV). I risultati sono stati pubblicati sul Journal of Medical Virology il 6 giugno 2023.
Dal primo caso identificato di mux nella Repubblica Democratica del Congo nel 1970, casi di mux sono stati osservati ripetutamente in Medio Oriente e in Africa. Nel 2022, tuttavia, è emerso un nuovo ceppo di MPXV (2022 MPXV) che si è ora diffuso oltre le tipiche aree colpite e in diverse parti del mondo. MPXV è classificato in tre ceppi, clade I, IIa e IIb. In particolare, 2022 MPXV appartiene al clade IIb ed è noto per essere meno letale del clade I.
Mentre le manifestazioni cliniche della MPOX comprendono rash, febbre, mal di testa e linfoadenopatia, è noto che l’infezione da 2022 MPXV causa un rash, in particolare nelle aree rettale e genitale. Tuttavia, deve ancora essere effettuata un’analisi comparativa approfondita delle caratteristiche virologiche tra i ceppi MPXV. Inoltre, considerando che le presentazioni cliniche di 2022 MPXV differiscono sostanzialmente da quelle degli altri ceppi, è necessaria un’analisi dettagliata di 2022 MPXV.
In questo studio, il gruppo ha infettato cheratinociti umani e organoidi del colon derivati da cellule iPS umane con i tre ceppi noti di MPXV, Clade I, Clade IIa e Clade IIb, e ha valutato la loro infettività e le risposte dell’ospite. È stato scoperto che tutti e tre i ceppi virali infettano i cheratinociti e gli organoidi del colon. In particolare, i cheratinociti hanno mostrato un’efficienza infettiva circa 7-42 volte maggiore rispetto agli organoidi del colon.
I ricercatori hanno anche osservato che l’infezione da MPXV causa disfunzione dei cheratinociti e danni mitocondriali. Inoltre, mentre i cheratinociti infettati con 2022 MPXV mostravano una maggiore espressione di geni associati all’ipossia, gli organoidi del colon derivati da cellule iPS umane infettati con un ceppo di clade I mostravano principalmente disfunzione intestinale.
Sebbene siano già stati sviluppati diversi agenti terapeutici mirati alle proteine virali MPXV , sono ancora in corso sforzi per esaminarne gli effetti antivirali nelle cellule umane. Pertanto, oltre ai farmaci antivirali , questo modello di infezione può essere utilizzato per valutare potenziali agenti terapeutici che agiscono direttamente per prevenire danni alla pelle e al colon.
Inoltre, come nel caso della sindrome respiratoria acuta grave coronavirus 2 (SARS-CoV-2), l’MPXV ha il potenziale per acquisire nuove mutazioni, richiedendo così in futuro un ulteriore sviluppo di farmaci preventivi o antivirali. Il gruppo di ricerca spera che questi risultati portino a una migliore comprensione dell’MPXV e facilitino lo sviluppo di terapie per l’MPXV.
Gli scienziati del National Institute of Allergy and Infectious Diseases (NIAID), parte del National Institutes of Health, hanno rimosso un importante ostacolo alla migliore comprensione del MPOX (precedentemente vaiolo delle scimmie). Hanno sviluppato un modello murino della malattia e lo hanno utilizzato per dimostrare chiare differenze nella virulenza tra i principali gruppi genetici (cladi) del virus mpox (MPXV).
La ricerca, apparsa in Proceedings of the National Academy of Science , è stata condotta da Bernard Moss, MD, Ph.D., capo della sezione di ingegneria genetica del Laboratorio di malattie virali del NIAID.
Storicamente, la vaiolo, una malattia simile al vaiolo, veniva trasmessa solo occasionalmente dai roditori a primati o persone non umane ed è stata osservata principalmente in diversi paesi africani. Il Mpox raramente si diffonde da persona a persona. Questo modello è cambiato nel 2022 con un’epidemia in cui si è verificata la trasmissione da persona a persona in più di 100 località in tutto il mondo.
Ad oggi, durante questa epidemia sono stati diagnosticati più di 80.000 casi di vaiolo. Il sequenziamento del genoma ha rivelato che il ceppo che causa l’attuale epidemia, il clade IIb, differisce da due clade storici; clade I, che ha un tasso di mortalità fino al 10%, e clade IIa, che ha un tasso di mortalità inferiore all’1%. La mortalità del clade IIb MPXV è inferiore a quella di entrambi i clade storici.
I topi da laboratorio consanguinei standard sono resistenti all’infezione da MPXV e l’assenza di un modello animale di piccola taglia ha reso difficile studiare come le differenze genetiche contribuiscono alle differenze osservate nella virulenza . Il dottor Moss e i suoi colleghi hanno identificato un ceppo di topi da laboratorio di origine selvatica (CAST/EiJ) e hanno determinato che questi topi possono essere infettati da MPXV. Come nelle persone, il clade I era il più virulento nei topi CAST, seguito dal clade IIa, quindi dal clade IIb.
Inaspettatamente, il virus del clade IIb era 100 volte meno virulento del virus del clade IIa nei topi e ha portato a una replicazione virale molto ridotta e a una virulenza molto inferiore rispetto a entrambi i clade storici. Nessun topo è morto per infezione del clade IIb, nonostante l’esposizione a dosi estremamente elevate di virus. Insieme, i risultati suggeriscono che il clade IIb sta evolvendo con una virulenza ridotta o si sta adattando ad altre specie, concludono i ricercatori.