Con scoperte a dir poco sorprendenti sui vaccini pneumococcici, gli scienziati hanno dimostrato che il fegato è il sito in cui il sistema immunitario scatena il suo assalto ai batteri pneumococcici dopo la vaccinazione contro gli agenti patogeni potenzialmente letali.
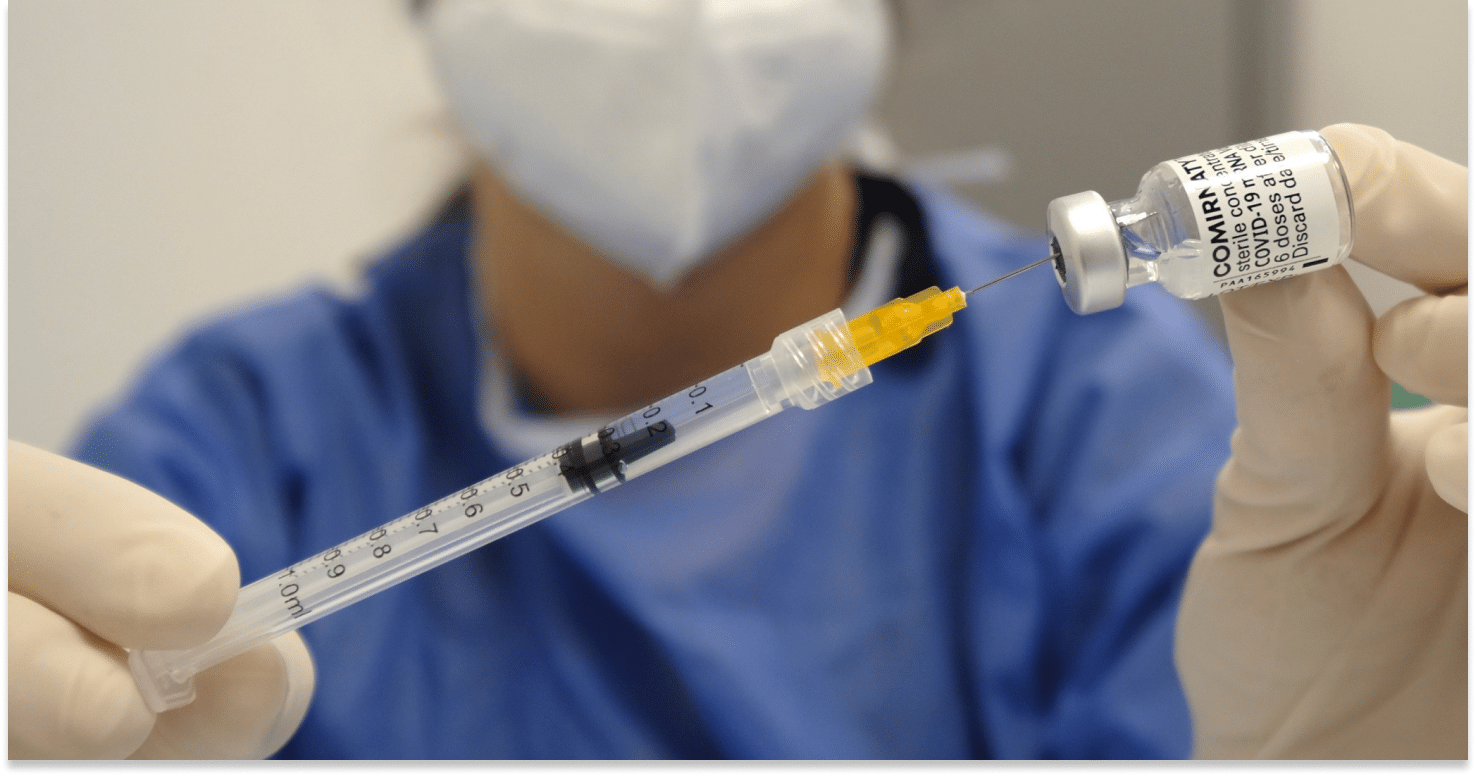
Lo studio è stato pubblicato su Science Translational Medicine.
Nuovi studi sui vaccini pneumococcici
Per anni gli scienziati hanno ipotizzato, teorizzato, suggerito e persino intuito come i batteri pneumococcici vengano distrutti nel corpo dopo essere stati segnalati come una minaccia dalla vaccinazione.
Una nuova ricerca mostra che il sistema immunitario non solo ha un posto speciale in cui gli organismi vengono distrutti, ma che una speciale coppia di cellule è coinvolta in un processo di annientamento “cattura e uccidi”, prevenendo la malattia prima che inizi, il vantaggio chiave della vaccinazione.
Un team globale di vaccinologi in Cina, Stati Uniti e Svizzera ha cercato spiegazioni su come si è svolto l’annientamento, lanciando uno studio approfondito su come due vaccini pneumococcici approvati stimolano la risposta di cattura e uccisione contro lo Streptococcus pneumoniae.
Numerosi ceppi di S. pneumoniae rappresentano una minaccia e i batteri sono noti causa di meningite, polmonite e infezioni del flusso sanguigno. I ricercatori hanno studiato due importanti vaccini pneumococcici: PCV13 e PPV23.
“La vaccinazione ha sostanzialmente ridotto la morbilità e la mortalità delle malattie batteriche”, ha affermato il dottor Juanjuan Wang, autore principale di una serie di esperimenti riportati su Science Translational Medicine . La ricerca ha confermato come è avvenuta l’annientamento batterico e quale dei due vaccini ha innescato la risposta immunitaria più efficiente.
I vaccini rappresentano una delle più grandi conquiste tecnologiche dell’umanità, avendo salvato centinaia di milioni di vite a partire dal vaccino contro il vaiolo di Edward Jenner del 1796 , sviluppato in Inghilterra durante il regno di Giorgio III.
La maggior parte dei vaccini, compreso quello di Jenner, sono stati sviluppati per combattere i virus. E alcuni dei vaccini più conosciuti al mondo hanno avuto un impatto drammatico sulla salute pubblica , combattendo una serie di malattie virali: morbillo, influenza, parotite, poliomielite, SARS-CoV-2 e altre.
I vaccini mirati contro i batteri sono ugualmente efficaci nel contrastare le malattie e nel salvare vite umane da agenti infettivi devastanti. Le vaccinazioni che aiutano l’organismo a respingere le infezioni batteriche includono quelle sviluppate per combattere la difterite, la pertosse e il tetano, insieme ai vaccini contro lo pneumococco. Tuttavia, ciò che era rimasto una questione di ricerca provocatoria e senza risposta era il modo in cui il corpo catturava e uccideva i batteri pneumococcici quando esposto.
Prima della nuova ricerca, gli scienziati avevano sospettato che dopo la vaccinazione il sistema immunitario inducesse le cellule chiave, come i fagociti, a migrare verso i siti di infezione e distruggere i batteri invasori. Ma mentre quello scenario era ampiamente accettato, i meccanismi fondamentali su come avrebbe potuto funzionare erano rimasti sconosciuti. Ora, la collaborazione internazionale ha prodotto una risposta piuttosto sorprendente.
“Segnaliamo che l’immunità indotta dal vaccino contro i batteri invasivi opera principalmente nel fegato”, ha scritto Wang. “In contrasto con il paradigma attuale secondo cui i fagociti migranti eseguono l’immunità indotta dal vaccino contro i patogeni trasmessi per via ematica, abbiamo scoperto che i batteri invasivi vengono catturati e uccisi nel fegato dell’ospite vaccinato attraverso vari meccanismi immunitari che dipendono dalla potenza protettiva del vaccino”.
Wang, un vaccinologo del Centro per la ricerca sulle malattie infettive dell’Università Tsinghua di Pechino, ha sottolineato che i meccanismi di eliminazione degli agenti patogeni indotti dal vaccino – come e dove nel corpo il sistema immunitario si è sbarazzato dei batteri invasivi – erano rimasti in gran parte indefiniti, almeno fino a quando Ora. E ci sono voluti scienziati di tre continenti per trovare la risposta e rivelare dove il sistema immunitario annientava i batteri patogeni.
Passando a un modello murino , sono stati in grado di confrontare gli effetti di due noti vaccini contro lo Streptococcus pneumoniae, PCV13 e PPV23.
Il PCV13 è un cosiddetto vaccino coniugato. PCV sta per vaccino coniugato pneumococcico e il numero 13 indica il numero di ceppi di S. pneumoniae da cui protegge. I vaccini coniugati sono costituiti da due subunità: un antigene debole come unità e un antigene forte come unità di trasporto. Con entrambe le unità, secondo i Centri statunitensi per il controllo e la prevenzione delle malattie, il sistema immunitario ha una risposta più forte all’antigene debole.
L’altro vaccino analizzato nell’indagine era PPV23, che è un vaccino polisaccaridico. Le iniziali stanno per vaccino polisaccaridico pneumococcico, che protegge contro 23 ceppi. Un vaccino polisaccaridico è progettato per stimolare l’immunità esponendo il sistema immunitario agli zuccheri che avvolgono la superficie di quasi due dozzine di ceppi di S. pneumoniae.
Nel corso dei loro esperimenti, il team è stato in grado di dimostrare una sorprendente differenza tra la capacità di cattura e quella di uccisione indotta dai due vaccini. È stata rilevata una maggiore efficacia di cattura e uccisione con la formulazione PCV13. Quel vaccino era associato ad una maggiore cattura di agenti patogeni circolanti da parte delle cellule endoteliali epatiche .
Il PCV13 è stato a lungo considerato più efficace del PPV23 e i colleghi di Wang hanno ora fornito una ragione per questa differenza. I ricercatori hanno scoperto che il PCV13 più potente induce quantità più elevate di anticorpi IgG e che il PCV13 coinvolge in modo più potente anche le cellule di Kupffer e le cellule epiteliali del fegato.
Le cellule di Kupffer sono macrofagi, globuli bianchi fagocitici, che risiedono nel fegato aderendo alle cellule endoteliali dei vasi sanguigni. Le cellule endoteliali sono le cellule epiteliali che rivestono le pareti dei vasi sanguigni. Poiché le cellule di Kupffer sono fagocitiche, nel senso che ingeriscono e distruggono i microrganismi invasivi, il loro ruolo è fondamentale nella dura attività di cattura e uccisione, hanno scoperto Wang e colleghi.
Il team è stato in grado di confermare nella loro ricerca che sia Kupffer che le cellule endoteliali hanno catturato S. pneumoniae nel flusso sanguigno attraverso un meccanismo “simile a una cerniera” prima di distruggerle. Il vaccino PPV23 più debole, al contrario, ha coinvolto solo le cellule di Kupffer e ha indotto quantità inferiori di anticorpi IgG. Gli scienziati hanno segnalato modelli simili di cattura e uccisione a livello epatico con i vaccini contro la Neisseria meningitidis, una delle principali cause di meningite batterica.
“Con alcune modifiche tecniche, i nostri risultati potrebbero essere utilizzati anche per la valutazione di candidati vaccini per agenti patogeni virali che dipendono dalla viremia per la diffusione”, ha concluso Wang, sottolineando che la viremia è la presenza di virus nel flusso sanguigno.
I vaccini pneumococcici sono efficaci, ma sono necessarie nuove strategie per ridurre la meningite
I vaccini pneumococcici coniugati (PCV) si sono rivelati molto efficaci nel ridurre la polmonite e altre infezioni invasive causate dal batterio Streptococcus pneumoniae . Ma i tassi di meningite hanno mostrato pochi cambiamenti, poiché i ceppi di pneumococco non presi di mira dai PCV emergono come cause più importanti di meningite, riporta un articolo pubblicato su The Pediatric Infectious Disease Journal , la rivista ufficiale della Società europea per le malattie infettive pediatriche.
Reshmi Mukerji, MPH, e David E. Briles, Ph.D., dell’Università dell’Alabama a Birmingham analizzano le prove su come la meningite pneumococcica sia cambiata dall’introduzione dei PCV. Per fare progressi nella riduzione dei tassi di meningite in tutto il mondo, i ricercatori ritengono che saranno necessari nuovi vaccini mirati a tutti i ceppi di pneumococco che colonizzano il naso e la gola, indipendentemente dal tipo capsulare.
I vaccini PCV7 e PCV13, mirati rispettivamente a sette e tredici ceppi di batteri pneumococcici, si sono rivelati molto efficaci nel ridurre i tassi di malattia pneumococcica invasiva, tra cui polmonite e infezioni del sangue o sepsi. Ma nonostante l’uso del PCV, i batteri pneumococcici rimangono la principale causa di meningite nei bambini. In tutto il mondo sono stati segnalati tassi di meningite fino a 13 casi ogni 100.000 bambini.

La meningite batterica è un’infezione del cervello e delle membrane del midollo spinale: è difficile da trattare, spesso fatale e causa complicazioni durature nei sopravvissuti. Studi recenti hanno dimostrato che i tassi di meningite pneumococcica nei bambini e negli adulti sono rimasti stabili o sono aumentati, in gran parte a causa di ceppi batterici non presi di mira dai PCV.
“L’uso diffuso dei vaccini ha portato all’emergere di un’ampia varietà di ceppi sostitutivi di tipo non PCV”, scrivono la signora Mukerji e il dottor Briles. Sebbene questa sostituzione del sierotipo sia avvenuta in tutto il mondo, le prove suggeriscono che i tassi sono più alti in Europa e Nord America. Questi ceppi non vaccinali causano meningiti almeno altrettanto gravi quanto i ceppi presi di mira dal PCV7 e dal PCV13.
Molti pneumococchi coperti dal PCV 13 formano capsule che li proteggono dal sistema immunitario del corpo nei polmoni e nel sangue. Tuttavia, i ceppi sostitutivi raramente causano sepsi, suggerendo che le loro capsule non PCV non consentono loro di sopravvivere bene nel flusso sanguigno. I pneumococchi con capsule di tipo non PCV possono raggiungere il cervello direttamente dal naso, dalla gola e dall’orecchio, attraverso i nervi olfattivi e uditivi, piuttosto che attraverso il flusso sanguigno.
Ciò potrebbe verificarsi quando il naso e la gola vengono colonizzati da pneumococchi di tipo capsulare diverso dal PCV, che hanno ampiamente sostituito i batteri presi di mira dagli attuali PCV. Per prevenire tali casi di meningite, sarà necessario sviluppare nuovi vaccini per prevenire o ridurre notevolmente la colonizzazione con questi batteri capsulari, non di tipo vaccinale.
Il problema è che esistono più di 98 diversi tipi capsulari: sarebbe difficile o impossibile individuarli tutti in un unico vaccino. L’alternativa più promettente potrebbe essere costituita da vaccini diretti contro proteine specifiche coinvolte nella formazione e colonizzazione delle capsule pneumococciche. Gli autori delineano un approccio in cui questa strategia potrebbe essere testata prima in studi su piccola scala, prima di studi più ampi per confermarne l’efficacia nella prevenzione della meningite.
“Poiché praticamente tutti i casi di meningite pneumococcica portano a sequele neurologiche permanenti [complicazioni] o alla morte, varrebbe la pena sviluppare un nuovo vaccino in grado di prevenire la meningite pneumococcica indipendentemente dal tipo capsulare”, hanno affermato Mukerji e Briles. concludere. “Un vaccino del genere dovrebbe proteggere dalla colonizzazione da parte della maggior parte, se non di tutti, i pneumococchi.”
Vaccini pneumococcici associati a meno infezioni gravi tra i bambini affetti da anemia falciforme
Una nuova ricerca pubblicata su Blood Advances rivela che dall’introduzione dei vaccini pneumococcici coniugati, PCV7 e PCV13, i tassi di infezione pneumococcica invasiva (IPD) tra i bambini affetti da anemia falciforme (SCD) sono diminuiti in modo significativo. Lo studio esplora l’efficacia dei vaccini esistenti ed emergenti per proteggere i bambini affetti da MCI da infezioni potenzialmente letali.
La SCD è la malattia ereditaria dei globuli rossi più comune negli Stati Uniti e colpisce circa 100.000 persone. Secondo i Centri per il controllo e la prevenzione delle malattie (CDC), la MCI colpisce una su 365 nascite di neri o afroamericani e una su 16.300 nascite di ispanoamericani.
I bambini affetti da MCI sviluppano tipicamente una disfunzione splenica entro i primi sei mesi o un anno di vita. La milza svolge un ruolo vitale nel proteggere il corpo umano dalle infezioni e i bambini affetti da morte improvvisa corrono un rischio maggiore di sviluppare malattie gravi e potenzialmente letali. Quelli con questa condizione vengono trattati con la profilassi con penicillina per ridurre il rischio di morte correlata all’infezione.
Prima del trattamento con penicillina, ogni anno un bambino su dieci di età inferiore ai cinque anni sviluppava IPD, una grave infezione. Ciò rappresentava il 32% di tutte le cause di morte per gli individui con anemia falciforme di età inferiore ai 20 anni nello studio cooperativo sull’anemia falciforme. Tuttavia, con l’aumento della resistenza agli antibiotici negli ultimi decenni, i ricercatori hanno dovuto ricorrere a nuovi metodi, come la vaccinazione, per proteggere questa popolazione vulnerabile.
“Negli anni 2000, quando gli pneumococchi stavano sviluppando resistenza agli antibiotici , furono introdotti i vaccini coniugati PCV7/PCV13 ,” ha spiegato Thomas Adamkiewicz, MD, MSc, ematologo pediatrico presso la Morehouse School of Medicine. “Poiché questi vaccini sono stati sviluppati per colpire i sierotipi batterici attualmente non coperti. Abbiamo esaminato l’impatto della copertura attuale e potenziale dei vaccini più recenti.”
I ricercatori hanno analizzato i dati raccolti in 25 anni dal Georgia Emerging Infections Program, parte della rete di sorveglianza attiva batterica dei Centri per il controllo e la prevenzione delle malattie (CDC), che identifica tutti gli IPD che si verificano nell’area metropolitana di Atlanta dal 1994.
I ricercatori del Georgia Emerging Infections Program, del Children’s Health care di Atlanta e della Emory University hanno collaborato a questo studio. Hanno identificato 104 episodi di IPD in 3.707 bambini di età inferiore a 10 anni con varianti HbSS e HbSC di SCD.
Secondo i dati dei ricercatori, dopo il 2002, l’87% dei bambini affetti da MCI ha ricevuto una o più dosi di vaccino PCV7 o PCV13 nella prima decade di vita. Il dottor Adamkiewicz e il suo team hanno scoperto che tra il 1994-1999 e il 2010-2018, i tassi di IPD sono diminuiti dell’87% nei bambini dalla nascita ai quattro anni affetti da HbSS, la forma più grave di MCI, e dell’80% in quelli di età compresa tra i cinque e i quattro anni. nove.
Hanno inoltre identificato che tra i bambini con HbSS e IPD, i tassi di mortalità sono diminuiti dal 14% al 3% dopo il 2002, e i tassi di meningite sono diminuiti dal 16% all’8%. Gli scienziati hanno inoltre osservato che la resistenza alla penicillina era più diffusa tra questa popolazione prima dell’approvazione del vaccino PCV7.
Dopo il 2000, sono emersi ceppi di IPD con sierotipi non coperti dai vaccini esistenti contro PCV7 e PVC13 che hanno causato la maggior parte delle IPD. Il vecchio vaccino pneumococcico polisaccaridico 23-valente (PPSV23) si è rivelato efficace contro i ceppi pneumococcici con sierotipi diversi dal PCV13, entro tre anni dalla vaccinazione.
I ricercatori hanno identificato che dall’autorizzazione del PCV7, i tassi di IPD nei bambini affetti da MCI dai cinque anni in su sono diminuiti in modo significativo. Inoltre, dall’approvazione e introduzione del vaccino PCV13, non è stata registrata alcuna infezione da IPD correlata al ceppo PCV13, nonostante alcuni bambini affetti da MCI non abbiano ricevuto il regime vaccinale completo raccomandato.
Questi risultati suggeriscono che l’immunità di gregge, introdotta da questi vaccini nella popolazione generale , sta aiutando a proteggere anche i bambini affetti da MCI dalle infezioni.
Il Dott. Adamkiewicz sottolinea che poiché i ceppi batterici con sierotipi non coperti dall’attuale vaccino sono predominanti, i bambini affetti da MCI possono trarre beneficio dalla ricezione di vaccini recentemente approvati come PCV15 e PCV20, che coprono rispettivamente il 16% e il 51% dei ceppi IPD non coperti da PCV13.
“Una grande domanda è il ruolo della profilassi con penicillina nei bambini affetti da MCI che ricevono nuovi vaccini”, ha affermato il dottor Adamkiewicz. “Abbiamo bisogno di molti più dati per formulare raccomandazioni.”
I dati di questo studio sono limitati a una regione degli Stati Uniti, ma i suoi risultati potrebbero offrire spunti sull’impatto che tali vaccini avrebbero sugli individui affetti da MCI in Africa, dove risiede la maggior parte dei bambini affetti da MCI.
Sebbene circa due terzi dei bambini nella popolazione generale abbiano ricevuto il vaccino PCV13, la mortalità nei bambini affetti da anemia falciforme rimane elevata, suggerendo la necessità di una più ampia diffusione delle misure preventive, compresi i vaccini.
Nel 2020, alla luce di questa esigenza, è stato istituito l’ASH Consortium on Newborn Screening in Africa (CONSA), una rete internazionale che cerca di dimostrare i benefici dello screening neonatale e degli interventi precoci per i bambini affetti da anemia falciforme nell’Africa sub-sahariana.
Sebbene l’IPD rimanga un rischio mortale per i bambini affetti da MCI, questo studio sottolinea la necessità di vaccini mirati ad ampi ceppi di batteri pneumococcici e di ulteriori ricerche per continuare a far progredire i trattamenti di profilassi disponibili per questa popolazione.