Grazie ai progressi nello sviluppo di cuori sintetici brevettati simili a quelli umani creati per la prima volta nello Stato del Michigan, i ricercatori possono studiare lo sviluppo del cuore umano e le malattie cardiache congenite su modelli altamente accurati. Ciò sta facilitando lo sviluppo di nuove terapie e farmaci per il trattamento di una varietà di malattie cardiache giusto in tempo per l’osservanza dell’American Heart Month a febbraio

Mini cuore: un organoide cardiaco complesso
Simili per dimensioni e sviluppo ai cuori fetali umani, questi mini organoidi cardiaci stanno diventando sempre più complessi e realistici. Il team di ricerca della MSU che ha creato i mini cuori ha pubblicato per la prima volta le sue scoperte nel 2020. Sono rapidamente diventati leader mondiali in questo campo e i loro ultimi progressi sono stati pubblicati su Nature Communications e Stem Cell Reports .
Aitor Aguirre, professore associato di ingegneria biomedica e capo della divisione di biologia delle cellule staminali e dello sviluppo presso l’Istituto di scienza e ingegneria quantitativa della salute della MSU, ha spiegato che l’introduzione di modelli realistici è essenziale per la scoperta di soluzioni efficaci e clinicamente traducibili per le malattie cardiovascolari . Si stima che circa 21 milioni di decessi ogni anno siano legati a questa condizione, compresi disturbi del cuore e dei vasi sanguigni. E quel numero è in crescita.
“Sebbene si ritenga che il 90% delle malattie cardiovascolari siano prevenibili, esse sono diventate la principale causa di morte nel mondo sviluppato”, ha affermato Aguirre. “Grazie ai progressi nelle tecnologie delle cellule staminali e nella bioingegneria, possiamo coltivare e studiare i cuori umani. Ciò rivoluzionerà gli approcci medici al trattamento e alla prevenzione delle malattie cardiache e delle condizioni congenite aiutandoci a comprendere i meccanismi della malattia.

“In futuro, prevediamo che meno pazienti avranno bisogno di cure e, per coloro che ne avranno bisogno, lo sviluppo di nuovi farmaci richiederà meno tempo”, ha aggiunto. “Soprattutto per i difetti congeniti, la prevenzione è la soluzione migliore. Ecco perché i mini organoidi cardiaci possono davvero cambiare il modo in cui affrontiamo l’assistenza sanitaria.”
Ad esempio, Aguirre ha spiegato che le aziende farmaceutiche ritireranno i farmaci dal mercato se si scoprirà che causano cardiotossicità. Essere in grado di prevedere la tossicità in anticipo potrebbe far risparmiare denaro, tempo e ridurre il rischio di fallimento del farmaco.
I mini organoidi cardiaci sono sviluppati con cellule staminali pluripotenti donate da adulti. La loro complessità cellulare e la rilevanza fisiologica consentono lo studio dello sviluppo e delle malattie del cuore umano in una piastra a un livello mai visto prima.
“Abbiamo creato un modello utilizzando questi organoidi per studiare gli effetti del diabete materno in ogni fase dello sviluppo nel cuore del feto”, ha detto Aguirre. “Questa è la definizione di medicina di precisione. Possiamo usare la scienza per rendere la pratica clinica più precisa.”
Utilizzo di un modello di mini cuore per sviluppare nuove terapie
I ricercatori della Michigan State University che hanno creato il primo modello di cuore umano in miniatura con tipi primari di cellule cardiache, tessuto vascolare e una struttura di camere funzionante hanno fatto un altro passo avanti: sviluppare nuove terapie per le malattie cardiache congenite.
Lo studio , “Organoidi cardiaci umani autoassemblanti per la modellazione dello sviluppo cardiaco e delle malattie cardiache congenite “, è stato pubblicato su Nature Communications e scritto per la prima volta da Yonatan Lewis-Israeli, uno studente laureato in ingegneria biomedica. Descrive in dettaglio come il modello cardiaco può essere utilizzato per studiare i difetti cardiaci congeniti umani, o CHD, aprendo così strade per lo sviluppo di trattamenti e strategie di prevenzione.
“La cosa più interessante di questa pubblicazione è che abbiamo utilizzato il nostro modello di organoidi cardiaci precedentemente stabilito per studiare e ricapitolare, per la prima volta, gli effetti del diabete della madre sullo sviluppo del cuore embrionale, che è una delle principali cause di malattia coronarica “, ha affermato Aitor Aguirre, autore senior dello studio e assistente professore di ingegneria biomedica presso l’Institute for Quantitative Health Science and Engineering della MSU.
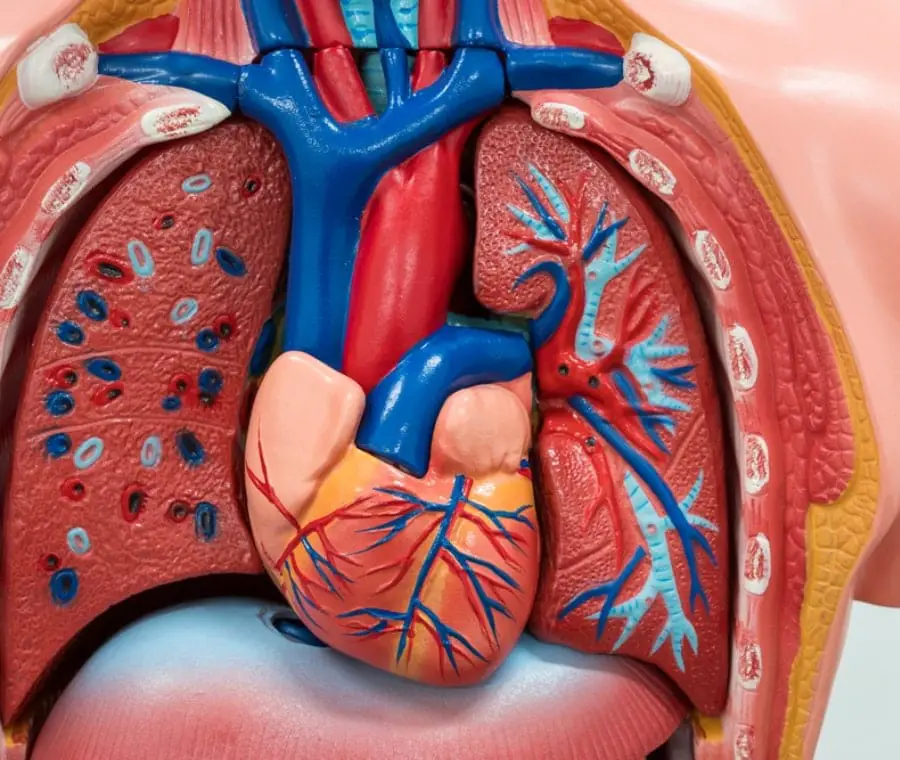
“Si tratta di un grande passo avanti verso la prevenzione della malattia coronarica e lo sviluppo di terapie per curarla. Normalmente non abbiamo accesso a cuori umani embrionali per ragioni etiche, quindi la nostra conoscenza diretta è molto limitata e proviene principalmente dai topi. Con i nostri mini-cuori, questo non è più un limite”, ha affermato. “Abbiamo accesso a tutti i cuori di cui abbiamo bisogno.”
Il team utilizza cellule staminali umane pluripotenti , simili alle cellule che compongono l’embrione iniziale, e le induce a diventare cuori manipolando segnali chimici e fisici. I “mini-cuori” di dimensioni fetali rappresentano un grande passo avanti nell’ingegneria dei tessuti con cellule staminali che può aiutare nella ricerca sulle malattie e nello sviluppo di nuove terapie mediche.
“Utilizziamo quindi questi mini-cuori per modellare una delle cause più frequenti di malattie cardiache congenite nei bambini, il diabete della madre”, ha detto Aguirre. “Quando la madre è diabetica, i bambini hanno un rischio 12 volte maggiore di avere CHD (circa l’1% per la popolazione normale), fino a circa il 12%. Con questo modello aggiornato di CHD indotta dal diabete, possiamo ora esplorare potenziali trattamenti per prevenire e curare la malattia in un modello umano.”
Tale ricerca era precedentemente limitata a soggetti animali come i topi, che non sono in grado di modellare i disturbi umani.
“Creare modelli di organi umani in vitro è un sogno della medicina attuale e questo costituisce un passo nella giusta direzione”, ha detto Aguirre. “Questi modelli possono essere utilizzati per studiare la biologia della salute e delle malattie , consentendo così lo sviluppo di nuove terapie e farmaci per trattare una varietà di malattie. Inoltre, questa tecnologia continuerà ad evolversi e un giorno potremmo far crescere questi costrutti abbastanza da poter essere utilizzati per i trapianti.”
Organoidi auto-organizzanti del cuore umano
Il biologo Sasha Mendjan dell’Accademia austriaca delle scienze di Vienna e il suo team hanno utilizzato cellule staminali umane pluripotenti per coltivare modelli di cuore delle dimensioni di un seme di sesamo, chiamati cardioidi, che si auto-organizzano spontaneamente per sviluppare una camera cava senza la necessità di impalcature sperimentali.
In precedenza, gli scienziati avevano costruito organoidi cardiaci 3D tramite l’ingegneria dei tessuti , un approccio che generalmente prevede l’assemblaggio di cellule e impalcature, come costruire una casa con mattoni e malta. Ma questi organoidi ingegnerizzati non hanno le stesse risposte fisiologiche ai danni del cuore umano e quindi spesso non riescono a fungere da buoni modelli di malattia.
“L’ingegneria dei tessuti è molto utile per molte cose, ad esempio se si desidera effettuare misurazioni sulla contrazione”, afferma Mendjan. Ma in natura gli organi non sono costruiti in questo modo. Nell’embrione gli organi si sviluppano spontaneamente attraverso un processo chiamato auto-organizzazione . Durante lo sviluppo, gli elementi costitutivi cellulari interagiscono tra loro, muovendosi e cambiando forma man mano che la struttura di un organo emerge e cresce.
“L’auto-organizzazione è il modo in cui la natura fa sì che i cristalli di fiocchi di neve o gli uccelli si comportino in uno stormo. Questo è difficile da progettare perché sembra che non ci sia un piano, ma ne esce comunque qualcosa di molto ordinato e robusto”, dice. “L’auto-organizzazione degli organi è molto più dinamica e succedono molte cose che non comprendiamo. Pensiamo che questa ‘magia nascosta’ dello sviluppo, ciò che non conosciamo ancora, sia la ragione per cui attualmente le malattie non sono modellati molto bene.”
Mendjan e il suo team volevano imitare lo sviluppo attraverso l’auto-organizzazione in un piatto. Hanno indotto le cellule staminali ad auto-organizzarsi attivando tutte e sei le vie di segnalazione conosciute coinvolte nello sviluppo del cuore embrionale in un ordine specifico. Man mano che le cellule si differenziavano, cominciavano a formare strati separati, simili alla struttura della parete cardiaca. Dopo una settimana di sviluppo, questi organoidi si sono auto-organizzati in una struttura 3D che aveva una cavità chiusa, una traiettoria di crescita spontanea simile a quella del cuore umano. Inoltre, il team ha scoperto che il tessuto simile a una parete dei cardioidi si contraeva ritmicamente per spremere il liquido all’interno della cavità.
“Non è che stiamo usando qualcosa di diverso rispetto ad altri ricercatori, ma stiamo semplicemente usando tutti i segnali conosciuti”, dice Mendjan. Aggiunge che non tutti i percorsi sono necessari per indirizzare le cellule staminali a diventare cellule cardiache. “Così hanno pensato: ‘Okay, non sono realmente necessari in vitro.’ Ma si scopre che tutti questi percorsi sono necessari. Sono importanti per far sì che le cellule si auto-organizzino in un organo.”
Il team ha anche testato il modo in cui i cardioidi rispondono ai danni ai tessuti. Hanno usato una barra d’acciaio fredda per congelare parti dei mini-cuori e hanno ucciso molte cellule nel sito. La morte cellulare è comunemente osservata dopo lesioni come un infarto. Immediatamente, il team ha visto i fibroblasti cardiaci – un tipo di cellula responsabile della guarigione delle ferite – iniziare a migrare verso i siti della lesione e produrre proteine per riparare il danno.
“Vogliamo elaborare modelli di cuore umano che si sviluppino in modo più naturale e siano quindi predittivi delle malattie”, afferma Mendjan. “In questo modo, le aziende saranno più aperte a includere più farmaci negli studi clinici perché sono molto più certe dell’esito dello studio.”
Il team ha in programma di coltivare organoidi cardiaci con camere multiple come quello visto in un vero cuore umano. Molte malattie cardiache congenite si verificano quando iniziano a formarsi altre camere, quindi il modello multicamera aiuterebbe i medici a comprendere meglio come si sviluppano i difetti nei feti.
I mini-cuori sono simili ai cuori umani
Vanessa Solvang è una studentessa magistrale in biotecnologie e ha scelto di specializzarsi in biologia cellulare e molecolare. Trascorre molto del suo tempo coltivando e studiando i mini-cuori presso il Laboratorio Centro della NTNU (Laboratoriesenteret).
Qui crescono mini-cuori, mini-cervelli, mini-polmoni e mini-occhi, che i ricercatori utilizzano per studiare malattie e possibili metodi di cura.
Vanessa e molti altri utilizzano nei loro studi un metodo per creare mini-cuori che inizia recuperando cellule della pelle da persone che hanno un difetto cardiaco.
“Effettuiamo una biopsia cutanea da pazienti con vari difetti cardiaci . Dalle cellule della pelle coltiviamo fibroblasti. Si tratta di un tipo di cellula da cui poi coltiviamo cellule staminali, che è il punto di partenza per l’ulteriore produzione di cellule cardiache”, afferma Vanessa. Solvang.

Le cellule staminali sono le cellule primarie del corpo. Nel feto, nel grembo materno, le cellule staminali si sviluppano gradualmente in diversi tipi di cellule. Ad esempio, alcuni diventano cellule polmonari e formano i polmoni, alcuni diventano cellule cartilaginee e formano nasi e orecchie, e alcuni diventano cellule cardiache e costruiscono un cuore.La stessa cosa accade in laboratorio, ma in piccole piastre Petri e sotto il controllo e la supervisione umana.”È incredibile come sia possibile utilizzare le cellule staminali per ogni genere di cose!” dice Solvang.
Vanessa Solvang fa parte del team che guida le cellule staminali a diventare cellule cardiache. Le piccole cellule cardiache pulsanti hanno bisogno di nutrimento e cure continue per vivere e pulsare. Poiché il materiale da costruzione di queste cellule proviene da persone con un difetto cardiaco, le cellule portano con sé queste informazioni nei loro geni.
Ed è proprio questo ciò che interessa studiare ai ricercatori: cercheranno di comprendere il difetto cardiaco e il suo materiale genetico e studiare il decorso della malattia. L’obiettivo è trovare metodi di trattamento e forse, a lungo termine, essere in grado di prevenire le malattie cardiache ereditarie.
“La conoscenza è la chiave per trovare soluzioni”, afferma Solvang.
Nota che in alcuni casi è altrettanto importante studiare le cellule cardiache sane per comprendere meglio la loro funzionalità e le risposte ai vari stimoli.
Gli studenti ricercatori stanno coltivando qualcosa chiamato organoidi cardiaci. Queste sono cellule cardiache che insieme formano strutture come il cuore di un essere umano vivente.
“Il vantaggio degli organoidi cardiaci è che sono simili al tessuto cardiaco umano. Ci rende più facile studiare e capire come funziona un cuore umano e possiamo studiare il decorso di una malattia. È anche concepibile che con Grazie a queste conoscenze saremo in grado di trovare trattamenti per varie malattie cardiache”, afferma Solvang.
La ricerca in corso sui mini-cuori è una collaborazione tra la Clinica di Cardiologia e la Clinica pediatrica dell’Ospedale St. Olav e il gruppo di ricerca di genetica medica presso il Dipartimento di Medicina Clinica e Molecolare della NTNU.
Solvang fa parte dei gruppi di ricerca guidati dal professor Magnar Bjørås. È uno dei leader del progetto coinvolti nel lavoro sul test del coronavirus della NTNU.
Oltre a coltivare cellule cardiache, Vanessa Solvang crea protocolli.
“L’obiettivo principale della mia tesi di master è stabilire un protocollo robusto per la produzione di organoidi cardiaci da cellule staminali umane. Ciò comporta il test di diverse sostanze chimiche – sia di che tipo che in quali concentrazioni – necessarie per indirizzare le cellule staminali a diventare cellule cardiache , ” lei dice.
Il suo lavoro prevede anche la ricerca della tecnica migliore per assemblare le cellule in strutture 3D, come mostrato nel video.
Solvang presenterà la sua tesi di master a maggio e, nonostante la pandemia di coronavirus, scopre che i suoi studi sono andati bene.
“Il coronavirus non ha influenzato il mio corso di studi. Ho lavorato principalmente in laboratorio, in un ambiente sicuro e con ottimi controlli delle infezioni. E l’ambiente qui è fantastico”, afferma.
Gli scienziati sviluppano il primo mini modello di cuore umano funzionante
I ricercatori della Michigan State University hanno creato per la prima volta in laboratorio un modello in miniatura di cuore umano, completo di tutti i tipi di cellule cardiache primarie e di una struttura funzionante di camere e tessuto vascolare.
Negli Stati Uniti, le malattie cardiache sono la prima causa di morte. “Questi minicuori costituiscono modelli incredibilmente potenti in cui studiare tutti i tipi di disturbi cardiaci con un grado di precisione mai visto prima”, ha affermato Aitor Aguirre, autore senior dello studio e assistente professore di ingegneria biomedica presso l’Institute for Quantitative Health Science and Engineering della MSU.
Questo studio, “Generazione di organoidi cardiaci che modellano lo sviluppo cardiaco umano precoce in condizioni definite”, appare sul server di pubblicazione preliminare bioRxiv.
Gli organoidi del cuore umano , o in breve hHO, sono stati creati tramite una nuova struttura di cellule staminali che imita gli ambienti di sviluppo embrionale e fetale.
“Gli organoidi – che significa ‘somiglianti a un organo’ – sono costrutti cellulari tridimensionali autoassemblanti che ricapitolano le proprietà e la struttura degli organi in misura significativa”, ha detto Yonatan Israeli, uno studente laureato dell’Aguirre Lab e primo autore dello studio.
L’innovazione utilizza un processo di bioingegneria che utilizza cellule staminali pluripotenti indotte – cellule adulte di un paziente per innescare lo sviluppo di un cuore di tipo embrionale in una capsula – generando un mini cuore funzionale dopo poche settimane. Le cellule staminali sono ottenute da adulti consenzienti e quindi prive di preoccupazioni etiche.
“Questo processo consente alle cellule staminali di svilupparsi, sostanzialmente come farebbero in un embrione, nei vari tipi e strutture cellulari presenti nel cuore”, ha detto Aguirre. “Diamo istruzioni alle cellule e loro sanno cosa devono fare quando tutte le condizioni appropriate sono soddisfatte.”
Poiché gli organoidi seguivano il naturale processo di sviluppo embrionale cardiaco, i ricercatori hanno studiato, in tempo reale, la crescita naturale di un vero cuore fetale umano.
Questa tecnologia consente la creazione di numerosi hHO contemporaneamente con relativa facilità, in contrasto con gli approcci di ingegneria tissutale esistenti che sono costosi, ad alta intensità di manodopera e non facilmente scalabili.
Uno dei problemi principali che deve affrontare lo studio dello sviluppo del cuore fetale e dei difetti cardiaci congeniti è l’accesso a un cuore in via di sviluppo. I ricercatori si sono limitati all’uso di modelli di mammiferi, di resti fetali donati e di ricerche sulle cellule in vitro per approssimare la funzione e lo sviluppo.
“Ora possiamo avere il meglio di entrambi i mondi, un modello umano preciso per studiare queste malattie – un piccolo cuore umano – senza utilizzare materiale fetale o violare i principi etici. Ciò costituisce un grande passo avanti”, ha affermato Aguirre.
Qual è il prossimo? Per Aguirre il processo è duplice. In primo luogo, l’ organoide cardiaco rappresenta uno sguardo senza precedenti su come si sviluppa un cuore fetale.
“In laboratorio, stiamo attualmente utilizzando organoidi cardiaci per modellare le malattie cardiache congenite, il difetto congenito più comune negli esseri umani che colpisce quasi l’1% della popolazione neonatale”, ha detto Aguirre. “Con i nostri organoidi cardiaci possiamo studiare l’origine delle malattie cardiache congenite e trovare modi per fermarle”.
E in secondo luogo, sebbene l’hHO sia complesso, è lungi dall’essere perfetto. Per il team, il miglioramento dell’organoide finale è un’altra strada chiave della ricerca futura. “Gli organoidi sono piccoli modelli del cuore fetale con caratteristiche funzionali e strutturali rappresentative”, ha detto Israeli. “Tuttavia, non sono ancora perfetti come il cuore umano. Questo è qualcosa su cui stiamo lavorando.”
Aguirre e il suo team sono entusiasti dell’ampia applicabilità di questi cuori in miniatura. Consentono una capacità senza precedenti di studiare molte altre malattie cardiovascolari, dalla cardiotossicità indotta dalla chemioterapia agli effetti del diabete, durante la gravidanza, sullo sviluppo del cuore fetale.