Gli scienziati dell’Università della California di San Francisco e del Gladstone Institute hanno identificato due farmaci antitumorali, il letrozolo e irinotecan, che mostrano una promettente capacità di invertire i cambiamenti cerebrali associati alla malattia di Alzheimer, offrendo la potenziale possibilità di rallentare o persino invertire i suoi sintomi.

Letrozolo e irinotecan farmaci antitumorali riprogrammano il cervello
Lo studio ha confrontato la firma dell’espressione genica caratteristica del morbo di Alzheimer con quella indotta da 1.300 farmaci già approvati, individuando una combinazione di questi due farmaci oncologici come potenziale trattamento per la forma più comune di demenza. Inizialmente, i ricercatori hanno analizzato come la malattia di Alzheimer alterasse l’espressione genica nelle singole cellule del cervello umano.
Successivamente, hanno esaminato farmaci già approvati dalla Food and Drug Administration (FDA) che potessero indurre alterazioni opposte nell’espressione genica. Nello specifico, la ricerca si è concentrata su farmaci capaci di invertire le modificazioni nell’espressione genetica sia nei neuroni che nelle cellule gliali, entrambi tipi cellulari danneggiati o alterati nell’Alzheimer.
A supporto di questa scoperta, i ricercatori hanno analizzato milioni di cartelle cliniche elettroniche, rivelando che i pazienti che assumevano alcuni di questi farmaci per altre patologie mostravano una minore probabilità di sviluppare il morbo di Alzheimer. La fase successiva ha coinvolto la sperimentazione di una combinazione dei due principali farmaci identificati, entrambi usati in oncologia, su un modello murino di Alzheimer. I risultati sono stati incoraggianti: si è osservata una riduzione della degenerazione cerebrale nei topi e persino il ripristino della loro capacità di memorizzare.
“Il morbo di Alzheimer provoca cambiamenti complessi nel cervello, rendendolo difficile da studiare e curare, ma i nostri strumenti computazionali hanno aperto la possibilità di affrontare direttamente la complessità,” ha dichiarato Marina Sirota, Ph.D., direttrice ad interim dell’UCSF Bakar Computational Health Sciences Institute, professoressa di pediatria e co-autrice senior dello studio. “Siamo entusiasti che il nostro approccio computazionale ci abbia condotto a una potenziale terapia combinata per l’Alzheimer basata su farmaci esistenti approvati dalla FDA.” Questa ricerca rappresenta un passo significativo verso nuove strategie terapeutiche per una delle malattie neurodegenerative più complesse.
Morbo di Alzheimer: la sfida di una malattia complessa
Il morbo di Alzheimer affligge circa 7 milioni di persone negli Stati Uniti, causando un inesorabile declino delle capacità cognitive, dell’apprendimento e della memoria. Nonostante decenni di ricerca intensiva, sono stati approvati dalla FDA solo due farmaci, nessuno dei quali è in grado di rallentare significativamente questo progressivo deterioramento.

Il Dr. Yadong Huang, ricercatore senior e direttore del Center for Translational Advancement presso Gladstone, nonché professore di neurologia e patologia presso l’UCSF e coautore senior dello studio, ha affermato che “l’Alzheimer è probabilmente il risultato di numerose alterazioni in molti geni e proteine che, insieme, compromettono la salute del cervello”. Ha inoltre sottolineato come “ciò renda molto difficile lo sviluppo di farmaci, che tradizionalmente produce un farmaco per un singolo gene o proteina che causa la malattia”.
Per affrontare questa complessità, il team ha sfruttato dati pubblicamente disponibili provenienti da tre studi sul cervello di pazienti affetti da Alzheimer. Questi dati hanno permesso di misurare l’espressione genica a livello di singole cellule cerebrali di donatori deceduti, sia con che senza la malattia. Da queste analisi, sono state generate firme di espressione genica specifiche per l’Alzheimer nei neuroni e nella glia.
I ricercatori hanno quindi confrontato queste firme con quelle presenti nella Connectivity Map, un ampio database contenente i risultati di test sugli effetti di migliaia di farmaci sull’espressione genica nelle cellule umane. Su 1.300 farmaci analizzati, 86 hanno mostrato la capacità di invertire l’espressione genica dell’Alzheimer in un tipo di cellula, e 25 in diversi tipi di cellule cerebrali. Tuttavia, solo 10 di questi erano già stati approvati dalla FDA per l’uso nell’uomo.
Per raffinare ulteriormente la selezione, il gruppo ha esaminato attentamente milioni di cartelle cliniche elettroniche archiviate nell’UC Health Data Warehouse, un database che include informazioni sanitarie anonime di 1,4 milioni di persone con più di 65 anni. Attraverso questa analisi, hanno scoperto che molti dei farmaci identificati sembravano aver ridotto nel tempo il rischio di sviluppare il morbo di Alzheimer nei pazienti che li assumevano.
“Grazie a tutte queste fonti di dati esistenti, siamo passati da 1.300 farmaci a 86, a 10, a soli cinque”, ha spiegato Yaqiao Li, ex studente laureato dell’UCSF nel laboratorio di Sirota, ora ricercatore post-dottorato nel laboratorio di Huang a Gladstone e autore principale dello studio. “In particolare, i dati raccolti da tutti i centri sanitari dell’UC ci hanno indirizzato direttamente ai farmaci più promettenti. È un po’ come una simulazione di studio clinico.” Questo approccio basato sui dati ha permesso di accelerare notevolmente il processo di identificazione di potenziali terapie.
La terapia combinata: risultati sorprendenti
Yaqiao Li, Yadong Huang e Marina Sirota hanno selezionato due farmaci antitumorali tra i cinque candidati più promettenti per i test di laboratorio. Avevano ipotizzato che il letrozolo, comunemente usato per il cancro al seno, avrebbe agito sui neuroni, mentre l’irinotecan, impiegato per il cancro al colon e ai polmoni, avrebbe aiutato la glia.
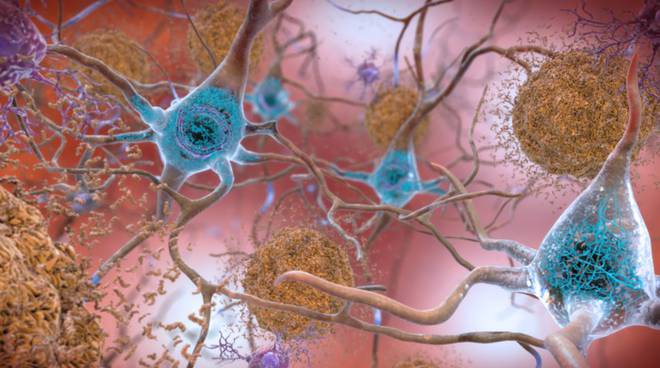
Il team ha utilizzato un modello murino aggressivo di Alzheimer, caratterizzato da molteplici mutazioni legate alla malattia. Man mano che i topi invecchiavano, sviluppavano sintomi simili all’Alzheimer e venivano trattati con uno o entrambi i farmaci. La combinazione dei due farmaci antitumorali ha prodotto risultati significativi, invertendo diversi aspetti dell’Alzheimer nel modello animale. Nello specifico, ha annullato le firme di espressione genica nei neuroni e nella glia che erano emerse con la progressione della malattia, ha ridotto sia la formazione di aggregati proteici tossici sia la degenerazione cerebrale e, aspetto cruciale, ha ripristinato la memoria nei topi.
“È davvero entusiasmante vedere la validazione dei dati computazionali in un modello murino di Alzheimer ampiamente utilizzato,” ha dichiarato Huang, che si aspetta che la ricerca possa presto avanzare verso una sperimentazione clinica per testare direttamente la terapia combinata sui pazienti. “Se fonti di dati completamente indipendenti, come i dati sull’espressione di singole cellule e le cartelle cliniche, ci guidano verso gli stessi percorsi e gli stessi farmaci, e poi risolvono l’Alzheimer in un modello genetico, allora forse siamo sulla buona strada,” ha aggiunto Sirota. Entrambi i ricercatori nutrono la speranza che questo approccio possa tradursi rapidamente in una soluzione concreta per i milioni di pazienti affetti dal morbo di Alzheimer.
Lo studio è stato pubblicato su Cell.