Un team di ricerca della Medical University of South Carolina (MUSC), guidato da Hongkuan Fan, professore associato presso il Dipartimento di Patologia e Medicina di Laboratorio, ha scoperto che bloccando o inibendo l’azione di Fli-1 in un modello murino con morbo di Alzheimer, la memoria dei topi subiva un miglioramento. La genesi di questa intuizione è dovuta allo studio dei pericoli, cellule che nel tessuto cerebrale di pazienti deceduti per l’Alzheimer, sino meno presenti.
Gli scienziati però, hanno anche riscontrato valori più elevati di Fli-1, una proteina che si trova più spesso nelle cellule del sangue e che si pensava ne governasse lo sviluppo. Da qui il tentativo di provare ad inibire la proteina che ha anche impedito alle cellule immunitarie di penetrare nel cervello e causare l’infiammazione che è un segno distintivo del morbo di Alzheimer. Il blocco di Fli-1 potrebbe essere un nuovo approccio promettente per il trattamento del morbo di Alzheimer e di altre demenze.
Il morbo di Alzheimer è un problema che nel tempo si sta aggravando, con l’invecchiamento della popolazione, raggiungerà cifre esponenziali. Secondo l’Alzheimer’s Association, più di 6 milioni di americani sono stati colpiti dal morbo di Alzheimer e 1 anziano su 3 ne morirà. Entro il 2050, il costo del morbo di Alzheimer, attualmente stimato in 355 miliardi di dollari, salirà a 1,1 trilioni di dollari.
I risultati della ricerca degli scienziati della Medical University of South Carolina sono stati pubblicati sulla rivista scientifica Molecular Therapy.
Inibire l’Fli-1: qualche approfondimento sulla ricerca
“Siamo davvero entusiasti di questi dati perché suggeriscono che Fli-1 potrebbe essere un nuovo bersaglio terapeutico per l’Alzheimer“, ha affermato il professore Hongkuan Fan, a capo della ricerca: “Sono urgentemente necessarie migliori terapie per il morbo di Alzheimer. La maggior parte delle terapie esistenti per l’Alzheimer trattano semplicemente i sintomi e fanno poco per affrontare le cause sottostanti“.
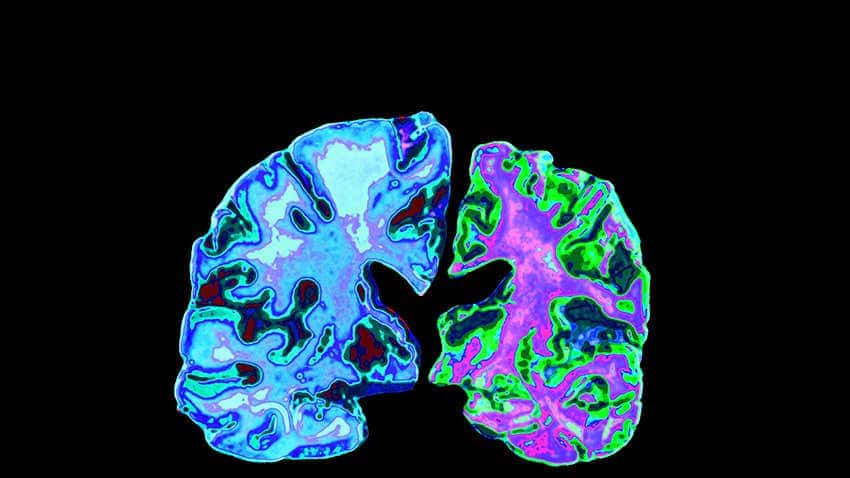
La comunità scientifica è da tempo consapevole che i soggetti con problemi vascolari, o problemi al cuore o ai vasi sanguigni, corrono un rischio maggiore di sviluppare il morbo di Alzheimer e altre demenze. Questi includono persone che hanno avuto un infarto o che hanno il diabete o la pressione alta o il colesterolo.
Questa informazione non dovrebbe meravigliare, poiché il cervello ha fame di ossigeno. Quando non ne riceve a sufficienza, perché il flusso di sangue è inadeguato, le sue cellule non funzionano bene e possono iniziare a morire. I pericoli che rivestono le pareti di minuscoli vasi sanguigni noti come capillari, assicurano che le richieste di energia e di eliminazione dei rifiuti del cervello siano soddisfatte.
“Il capillare è dove si trova tutta l’azione“, ha affermato Perry Halushka, MD, Ph.D., illustre professore universitario di farmacologia cellulare e molecolare. “È il luogo in cui tutti questi scambi avvengono davvero”.
I periciti aiutano anche a costituire la barriera ematoencefalica che impedisce alle impurità e alle cellule immunitarie del sangue di raggiungere il cervello. Aiutano anche a rimuovere l’amiloide-beta, noto per essere un colpevole del morbo di Alzheimer, dal cervello.
Quando i periciti vengono persi, le cellule immunitarie e le impurità iniziano a fuoriuscire nel cervello, provocandone l’infiammazione e portando infine alla morte cellulare e al declino della funzione mentale.
“I periciti possono svolgere un ruolo molto più importante nella demenza di quanto si pensasse inizialmente“, ha affermato Halushka. “Questo è particolarmente vero nella popolazione che invecchia, dove la demenza vascolare diventerà un problema più grande”.
Il team del MUSC ha esaminato il cervello delle persone morte di Alzheimer, servendosi delle risorse della banca del cervello del Carroll A. Campbell, Jr. Neuropathology Laboratory: “L’opportunità di studiare il cervello umano è una risorsa straordinaria per l’istituto e per lo studio di tutti i tipi di malattie del cervello, non solo del morbo di Alzheimer”, ha spiegato Halushka.
Il team del MUSC ha scoperto che i cervelli dei pazienti deceduti per l’Alzheimer avevano il 34% di periciti in meno rispetto ai cervelli sani nell’ippocampo, una parte del cervello associata all’apprendimento e alla memoria. I restanti periciti avevano livelli molto più elevati di Fli-1.
Il team ha quindi mostrato che un modello animale di Alzheimer mostrava anche perdita di periciti nell’ippocampo, aumento di Fli-1 e memoria compromessa. Il blocco di Fli-1 ha migliorato le prestazioni dei topi nei test comportamentali volti a valutare la memoria: “La scoperta più interessante è che l’inibitore Fli-1 ha effettivamente migliorato i deficit cognitivi nel modello animale perché, alla fine, è l’unica cosa che conta“, ha continuato Halushka.
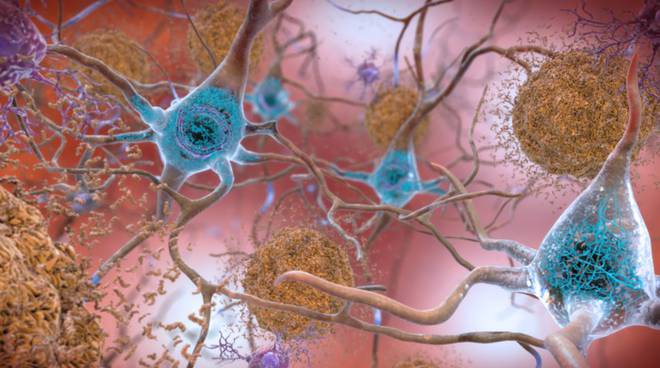
Il team di esperti ha anche rivelato che il blocco di Fli-1 nei topi ha aiutato a prevenire la perdita di periciti e a preservare l’integrità della barriera ematoencefalica, oltre a ridurre l’accumulo di beta-amiloide: “Non ci aspettavamo un effetto così profondo nei topi, ma con nostra sorpresa, l’inibitore ha funzionato davvero“, ha detto Fan.
Il prossimo passo per il team MUSC è sviluppare un RNA in grado di silenziare Fli-1 e quindi ridurre l’infiammazione cerebrale che porta alla morte cellulare nell’Alzheimer. L’obiettivo non sarebbe quello di eliminare Fli-1, poiché svolge ruoli importanti nel corpo, ma di mantenerlo a livelli sani.
“La cosa eccitante è che questo potrebbe essere un nuovo modo di pensare al trattamento dell’Alzheimer, a cui non si è mai pensato prima“, ha concluso Halushka. “Questa ricerca apre un’area completamente nuova per potenziali bersagli, non solo Fli-1 ma il pericito stesso”.