Qualcuno lo ha voluto paragonare alla forza rigeneratrice che possedeva Wolverine, ma l‘impianto osseo rigenerativo progettato dai ricercatori dell‘Università del Nebraska Medical Center e dell’Università del Nebraska-Lincoln potrebbe realmente aiutare a riparare i danni ossei in seguito a traumi fisici, interventi chirurgici o osteoporosi.
Lo studio è stato pubblicato sulla rivista scientifica Science Advances.
Impianto osseo rigenerativo: ecco di cosa si tratta
Il gruppo di esperti ha sviluppato un impianto o impalcatura biodegradabile, a base di nanofibre, il cui design potrebbe rigenerare meglio l’osso guidando efficacemente la migrazione delle cellule recuperative verso il sito della lesione. Quando l’impiantato osseo è stato introtto nello scheletro dei ratti con difetti ossei , lo scaffold cilindrico ha promosso la rigenerazione dell’osso che si è mostrato più denso, più voluminoso e più simile al tessuto circostante rispetto a quello ottenuto da molti altri progetti all’avanguardia.
L’impianto ha stimolato la rigenerazione anche senza l’ausilio di cellule staminali di origine esterna o cosiddetti fattori di crescita, che aiutano a promuovere la guarigione ma possono anche introdurre complicazioni regolatorie ed effetti collaterali che vanno dall’infiammazione alla formazione incontrollata di tessuto.
“Finora non abbiamo trovato scaffold in grado di funzionare meglio dei nostri”, ha affermato Jingwei Xie, professore di chirurgia presso UNMC e professore di ingegneria meccanica e dei materiali presso l‘Università del Nebraska-Lincoln. “La struttura è la chiave.” Quella struttura distintiva deriva da una recente scoperta ingegneristica, guidata da Xie, che ha trasformato un approccio bidimensionale promettente ma limitato in una meraviglia 3D.
“Prima di questo”, ha spiegato Xie, “molti laboratori stavano sviluppando impianti 2D realizzati con nanofibre allineate per formare i pori. Idealmente, si pensava, le cellule staminali del midollo osseo si sarebbero infiltrate in quei pori e alla fine avrebbero formato tessuti con un’architettura simile all’osso nativo adiacente. Ma gli ingegneri stavano spesso lottando per creare pori abbastanza grandi o organizzati da consentire alle cellule di passare costantemente attraverso e successivamente formare i viticci di tessuto che compongono l’osso”.
Lo scienziato, ispirato da un’idea proveniente dalla matematica del liceo, Xie ha deciso di fabbricare scaffold 3D con pori più grandi, meno casuali e più navigabili. Il concetto, denominato solido di rivoluzione, ha evidenziato come qualsiasi curva 2D (un rettangolo, un triangolo, un cerchio) può essere ruotata attorno a un asse per formare un solido matematico. Ruotando un rettangolo, ad esempio, si forma un cilindro, mentre un triangolo sviluppa un cono e un cerchio una sfera.
I collaboratori di Xie hanno applicato il principio prendendo un tappetino rettangolare in scala millimetrica di nanofibre impilate, usando il calore per fissare insieme un’estremità come il dorso di un libro, quindi immergendo il tappetino in una soluzione che ha espanso quelle fibre. Alla fine, l’estremità libera si è aperta a ventaglio per formare un cilindro le cui nanofibre e i relativi pori si irradiavano dal centro come i raggi di una ruota.
I ricercatori avevano intuito che la disposizione radiale avrebbe incoraggiato vari tipi di cellule da tutto il sito della lesione a migrare verso il suo centro, formando reti di tessuto nel processo. Per testarlo, hanno incorporato le impalcature radiali in cavità di osso mancante nella parte superiore del cranio dei ratti, valutando la ricrescita dopo quattro e otto settimane.
In entrambi i momenti, gli scaffold radiali avevano un osso rigenerato che copriva sostanzialmente più siti di lesione rispetto a un gruppo di controllo e un gruppo impiantato con spugne di collagene, un impianto comunemente usato.
“Abbiamo scoperto che le nanofibre allineate radialmente possono davvero migliorare la rigenerazione ossea in questo scenario, specialmente con l’osso cranico”, ha detto Xie. “Le prime quattro settimane, in particolare, abbiamo visto una differenza significativa. Può iniziare a promuovere la rigenerazione ossea in un lasso di tempo molto breve”.
L’osso rigenerato conteneva più minerali, come il calcio, essenziali per una sana formazione ossea. Era notevolmente più denso e spesso, il che significa che potrebbe aiutare ad affrontare i sintomi dell’osteoporosi. È cresciuto in un allineamento radiale molto simile a quello dell’impalcatura, suggerendo che le cellule stessero, in effetti, seguendo i pori. E quando i colleghi europei hanno eseguito simulazioni di stress meccanico basate sulla crescita risultante, il profilo dell’osso rigenerato era parallelo a quello dell’osso cranico sano, suggerendo che il primo potrebbe resistere a forze di compressione così come il secondo.
Oltre a tutto ciò, le cellule del midollo osseo che sono state coltivate sullo scaffold del team vantavano livelli naturalmente più elevati di molteplici fattori di crescita, tra cui la proteina morfogenetica ossea 2, o BMP-2, una forma della quale è stata utilizzata in combinazione con spugne di collagene per stimolare crescita ossea. Altri approcci rigenerativi emergenti – scaffold stampati in 3D, aerogel, idrogel iniettabili – spesso incorporano anche BMP-2 di origine esterna. Anche così, quelli messi alla prova sui ratti non sono riusciti a stimolare la crescita così come il design del team del Nebraska, ha detto Xie.
La promessa di un impianto biodegradabile in grado di stimolare tale crescita da solo, senza alcun agente biologico esterno, potrebbe facilitare il suo percorso verso l’eventuale approvazione della Food and Drug Administration statunitense. Anche lavorando a suo favore, il team ha fabbricato l’impianto da un poliestere già ampiamente utilizzato nei dispositivi biomedici approvati dalla FDA.
Se alla fine si tradurrà in un ambiente clinico, l’impianto potrebbe rivelarsi un’alternativa interessante agli approcci più tradizionali, ha affermato Xie. Questi includono gli alloinnesti, che consistono nell’impianto di frammenti ossei da donatori, e autoinnesti, che comportano la raccolta di un segmento di osso dal proprio corpo e il suo trapianto nel sito della lesione. Quest’ultimo richiede più interventi chirurgici e, tra gli altri problemi, può ridurre la funzionalità di qualunque osso venga prelevato.
Il recente esperimento del team potrebbe anticipare la prima applicazione diretta dell’impianto, ha detto Xie.
“Alla fine, l’idea è che forse possiamo generare un prodotto che è fondamentalmente solo l’impalcatura del cilindro, concentrandosi principalmente sulle applicazioni di neurochirurgia”, ha spiegato lo studioso. “Perché in un sacco di neurochirurgia, hanno bisogno di praticare un foro sul cranio prima di eseguire l’intervento. E dopo, hanno bisogno di riparare quel buco“.
Per aiutare a portare avanti il progetto, Xie e i suoi colleghi si stanno concentrando su prove ed esperimenti su animali di grandi dimensioni che coinvolgono il femore, la clavicola e simili, e stanno cercando di perfezionare ulteriormente ciò che già lo distingue: “Stiamo ancora cercando di ottimizzare la struttura”, ha detto Xie. “In questo momento, può migliorare la rigenerazione ossea, ma penso che possiamo ancora migliorarla in certi modi”.
Non solo impianto osseo in 3D ma un’impalcatura scheletrica che supporta le cellule ossee e i vasi sanguigni
L’impianto osseo rigenerativo in 3D è una grande promessa per le nuove tecnologie che verranno impiegate in campo ortopedico ma non è l’unica. La tecnologia biomedica infatti ha sviluppato gli scaffold di ingegneria tissutale costruiti attorno a peptidi ultracorti che forniscono una nuova piattaforma per lo studio della rigenerazione ossea in laboratorio. (1)
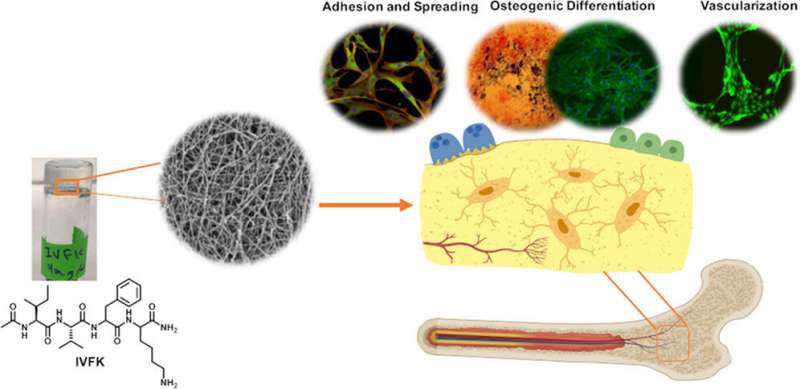
I peptidi creati presso KAUST si autoassemblano in un idrogel simile alla cartilagine che simula la matrice naturale che è alla base della formazione ossea nel nostro organismo. Le sue proprietà fisiologicamente rilevanti garantiscono a questo biomateriale favorevole alle cellule di supportare la crescita e lo sviluppo di cellule precursori del midollo osseo. Consente inoltre ai vasi sanguigni tubolari di prendere forma: questa funzione è una parte fondamentale della salute e della riparazione delle ossa.
“Il nostro sistema è un modello semplice, efficiente e robusto che ricorda da vicino la complessa architettura del tessuto osseo nativo”, ha affermato il ricercatore Salwa Alshehri. “Utilizzando questi idrogel a base di peptidi, ora possiamo costruire modelli di malattie 3D per l’ingegneria dei tessuti, la ricerca biomedica e i test sui farmaci”.
I ricercatori della KAUST, guidati dalla professoressa di bioingegneria Charlotte Hauser, avevano precedentemente dimostrato che i loro peptidi ultracorti potevano essere miscelati con le cellule nell’ugello di una stampante 3D per creare un tipo di bioinchiostro che, una volta espulso, si sarebbe solidificato istantaneamente nelle forme desiderate. Ma non era chiaro se il materiale sintetico potesse sostenere l’intera complessità dello sviluppo osseo, che include l’adesione, la diffusione e la differenziazione delle cellule staminali specifiche dell’osso, insieme all’incursione dei vasi sanguigni necessari per il trasferimento dei nutrienti e la rimozione dei rifiuti metabolici.
Alshehri ha messo alla prova la piattaforma. Lei e Hauser, insieme al ricercatore Hepi Hari Susapto, hanno sviluppato la rigidità dei loro idrogel alterando la concentrazione di peptidi nella loro miscela. Una volta ottenute le giuste proprietà meccaniche per la crescita ossea, gli studiosi hanno seminato gli scaffold con cellule staminali mesenchimali derivate dal midollo osseo. All’interno di questi costrutti 3D, le cellule hanno mantenuto la loro capacità di autorinnovarsi e, in condizioni appropriate convertirsi in cellule osteocitarie che formano l’osso.
Il team KAUST ha poi fatto un ulteriore passo avanti. I ricercatori hanno aggiunto cellule prelevate da vene ombelicali umane ai loro mini scaffold ossei e hanno scoperto che il materiale potrebbe supportare anche una fitta rete di formazione di vasi sanguigni. “Il nostro modello ha adattato con successo più di un tipo di cellula senza alcun compromesso sulla loro vitalità“, afferma Alshehri, che ora spera di sviluppare modelli di tessuto osseo ancora più sofisticati per la valutazione in modelli animali e, infine, come terapia rigenerativa per i pazienti con malattie ossee.
Alshehri, Hauser e i loro colleghi stanno anche cercando di estendere la piattaforma ad altre applicazioni mediche, non solo alla rigenerazione ossea . “Dal momento che i vasi sanguigni sono parte integrante dei tessuti nativi”, ha affermato Alshehri, “la coltura di successo delle cellule endoteliali in 3D all’interno di questi idrogel rappresenta una grande promessa per le applicazioni di ingegneria dei tessuti in generale”.
Ma qual è la funzione dei peptidi ultracorti?
La “biostampa“, la stampa 3D che incorpora cellule viventi, ha il potenziale per rivoluzionare l’ingegneria dei tessuti e la medicina rigenerativa. Gli scienziati hanno sperimentato “bioink” naturali e sintetici per stampare scaffold che tengono in posizione le cellule mentre crescono e formano un tessuto con una forma specifica. Ma ci sono sfide con la sopravvivenza cellulare. I bioinchiostri naturali, come la gelatina e il collagene, devono essere trattati con sostanze chimiche o luce ultravioletta per mantenere la loro forma, il che influisce sulla vitalità cellulare. Gli idrogel polimerici sintetici testati fino ad oggi richiedono anche l’uso di sostanze chimiche aggressive e condizioni che minacciano la sopravvivenza cellulare.
La bioingegnera di KAUST Charlotte Hauser ha guidato un team di ricercatori per sviluppare un processo di biostampa che utilizza pepridi ultracorti come base dell’inchiostro dell’impalcatura. Hanno progettato tre peptidi utilizzando diverse combinazioni degli amminoacidi isoleucina, lisina, fenilalanina e cicloesilalanina.
Per la stampa vera e propria, il team ha utilizzato un nuovo ugello a tripla entrata. Il bioinchiostro peptidico va in un ingresso, una soluzione tampone va in un altro e le cellule vengono aggiunte attraverso un terzo. Questo permette all’inchiostro peptidico di mescolarsi gradualmente con la soluzione tampone e quindi combinarsi con le cellule all’uscita dell’ugello. Una volta che l’inchiostro viene espulso, si solidifica istantaneamente, catturando le cellule all’interno della sua struttura.
I bioingegneri KAUST hanno sviluppato un processo di biostampa che utilizza peptidi ultracorti come base dell’inchiostro per impalcature. Credito: © 2021 KAUST: “È difficile trovare un biomateriale adatto alle cellule che supporti la sopravvivenza cellulare a lungo termine e sia anche stampabile”, afferma il ricercatore Hepi Hari Susapto. “I nostri bioink realizzati con idrogel peptidici ultracorti autoassemblanti affrontano in modo efficiente questa sfida”.
Il team è stato in grado di stampare cilindri alti fino a quattro centimetri, come nell’immagine sopra, e un naso simile a quello umano, che mantenevano bene le loro forme.
Fibroblasti umani, cellule staminali mesenchimali del midollo osseo umano e neuroni del cervello di topo sono sopravvissuti e hanno proliferato bene all’interno della matrice di idrogel. Gli scienziati hanno ulteriormente indotto le cellule staminali mesenchimali del midollo osseo a differenziarsi all’interno di un’impalcatura stampata in tessuto elastico simile alla cartilagine entro un periodo di quattro settimane.
Il team sta ora lavorando per cambiare la chimica di superficie dei loro bioinchiostri in modo che assomiglino più da vicino all’ambiente cellulare nel corpo umano: “Il nostro prossimo passo è bioprintare modelli di malattie 3D e organi in miniatura per lo screening e la diagnosi dei farmaci ad alto rendimento”, afferma Hauser. “Questi potrebbero aiutare a ridurre il tempo e il costo della ricerca di farmaci più efficaci e personalizzati“.
Perchè usate il verbo potrebbe? Sapete forse che lo studio è una cazzata oppure serve per beccare qualche click?
Caro Walter, il fenomeno del clickbaiting che lei chiama “acchiappa click” è riferito generalmente al titolo: se il titolo è accattivante, l’utente sarà invogliato a leggere l’articolo. La sua protesta invece riguarda la voce verbale “potrebbe” che non è presente né nel titolo né nel sottotitolo, bensì nell’attacco dell’articolo stesso (l’apertura): converrà con me che se lei lo ha letto, ha già cliccato sul link e il tanto disprezzato “potrebbe” è di conseguenza assolto per non aver commesso il fatto. Gentile Walter, se si è preso il disturbo di leggere l’articolo, avrà capito autonomamente che il supporto osseo in 3D è stato impiantato prima nei ratti e solo successivamente verranno sacrificati animali di taglie più grandi. Il “potrebbe” che tanto la disturba ha quindi la funzione di avvisare il lettore che si tratta di una ricerca sperimentale, particolare specificato sia nell’articolo stesso, sia nel link della ricerca dedicata. Concludo informandola che la redazione iCrewplay tech lavora con l’intenzione di informare su tutti i progressi della ricerca medica in modo gratuito: lei e tanti altri avete avuto accesso a questa informazione, frutto del lavoro e dello studio approfondito di un redattore senza dover pagare un centesimo. Capisce allora che ogni illazione sul clickbaiting evapora nel nulla, essendo il nostro intento molto più nobile di quanto alcuni riescano a cogliere. Non siamo tutti brutti, sporchi e cattivi. Saluti
Dénise Meloni