Un team di ricercatori del Massachusetts General Hospital (MGH) e del Brigham and Women’s Hospital (BWH) ha riprogrammato il microambiente tumorale del cancro al fegato utilizzando nanoparticelle di mRNA. Questa tecnologia, simile a quella utilizzata nei vaccini COVID-19, ha ripristinato la funzione del gene p53, un oncosoppressore mutato non solo nel fegato ma anche in altri tipi di cancro.
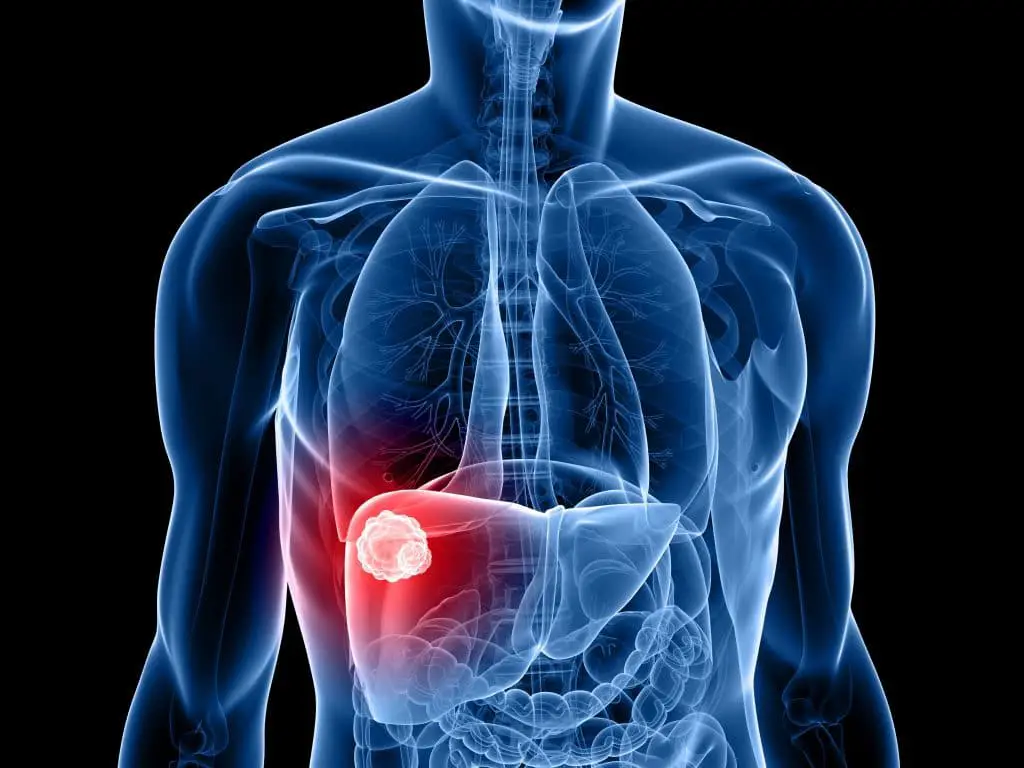
Se utilizzato in combinazione con il blocco del checkpoint immunitario (ICB), l’approccio con nanoparticelle di mRNA p53 non solo ha indotto la soppressione della crescita del tumore, ma ha anche aumentato significativamente le risposte immunitarie antitumorali nei modelli di laboratorio di carcinoma epatocellulare (HCC).
I risultati dello studio sono stati pubblicati sulla rivista scientifica Nature Communications.
Gene p53: come induce la soppressione del cancro al fegato
“La riprogrammazione delle componenti cellulari e molecolari del microambiente tumorale potrebbe essere un approccio trasformativo per il trattamento dell’HCC e di altri tumori“, afferma il co-autore senior Jinjun Shi, Ph.D., con il Center for Nanomedicine presso BWH, che ha sviluppato il piattaforma con il biologo del cancro al fegato MGH e co-autore senior Dan G. Duda, DMD, Ph.D.
“Utilizzando questo nuovo approccio, stiamo prendendo di mira percorsi specifici nelle cellule tumorali con nanoparticelle di mRNA. Queste minuscole particelle forniscono alle cellule le istruzioni per costruire proteine che, nel caso dell’HCC, ritardano la crescita del tumore e rendono il tumore più reattivo al trattamento con immunoterapia“, ha continuato Shi.
L’HCC è la forma più diffusa di cancro al fegato, caratterizzata da un alto tasso di mortalità e da una prognosi infausta per i pazienti. I bloccanti del checkpoint immunitario, una nuova classe rivoluzionaria di farmaci che consentono al sistema immunitario del corpo di riconoscere e attaccare le cellule tumorali, hanno mostrato efficacia nel trattamento dell’HCC, ma la maggior parte dei pazienti non ne trae beneficio.
Per superare questa resistenza, si stanno sviluppando molteplici strategie per migliorare gli ICB combinandoli con altre terapie esistenti, come i farmaci anti-VEGF e la radioterapia. Tuttavia, si prevede che anche questi approcci andranno a beneficio solo di un piccolo numero di pazienti, creando un urgente bisogno di nuove terapie combinate.
Incoraggiato dal successo dell’mRNA nei vaccini COVID-19, Shi ha deciso di applicare la tecnologia (con alcune modifiche) al targeting delle cellule tumorali. Ha collaborato con Duda, il cui laboratorio MGH aveva già creato sofisticati modelli animali per analizzare il microambiente dei tumori del fegato in risposta all’immunoterapia.
Gli scienziati hanno sviluppato e ottimizzato una strategia di nanoparticelle di mRNA per ripristinare la perdita di funzione di p53, un gene oncosoppressore la cui funzione è persa in più di un terzo dei casi di carcinoma epatocellulare. In tal modo, hanno scoperto prove che p53 regola il microambiente tumorale modulando l’interazione delle cellule tumorali con le cellule immunitarie come parte della terapia ICB.
“Nel nostro lavoro precedente avevamo sviluppato nanoparticelle per colpire CXCR4, un recettore per le chemochine espresso dalle cellule tumorali del fegato e per co-fornire selettivamente farmaci come gli inibitori della chinasi“, spiega Duda.
“Ora abbiamo adattato questa piattaforma per utilizzare CXCR4 come una sorta di codice postale per indirizzare selettivamente il tumore con nanoparticelle che incapsulano mRNA terapeutici. Quando abbiamo combinato questa nanomedicina con anticorpi anti-recettore della morte programmata 1 (PD-1), un’immunoterapia standard per i pazienti con carcinoma epatocellulare, ha indotto la riprogrammazione globale del microambiente tumorale e della risposta tumorale ripristinando l’espressione di p53 “.
Il prossimo passo per il team è trasferire la loro ricerca dai modelli animali ai pazienti in una sperimentazione clinica. “Gli scienziati hanno lottato per decenni per trovare un modo efficace per prendere di mira i percorsi oncosopressori “, sottolinea Shi. “Il nostro studio proof-of-concept è uno sviluppo entusiasmante che mostra chiaramente che le nanoparticelle di mRNA di p53 in combinazione con l’ICB non solo funzionano, ma potrebbero anche fare una grande differenza invertendo l’immunosoppressione nell’HCC e potenzialmente in altri tumori”.

Il cancro al fegato è molto più comune nei paesi dell’Africa subsahariana e del sud-est asiatico che negli Stati Uniti. In molti di questi paesi è il tipo più comune di cancro. Più di 800.000 persone vengono diagnosticate con questo cancro ogni anno in tutto il mondo. Il cancro al fegato è anche una delle principali cause di decessi per cancro in tutto il mondo, con oltre 700.000 decessi ogni anno.
Shi è professore associato di Anestesia presso la Harvard Medical School (HMS). Duda è professore associato di Oncologia delle radiazioni presso HMS e direttore della ricerca traslazionale in oncologia delle radiazioni gastrointestinali presso MGH. Yuling Xiao, Ph.D., e Jiang Chen, MD, Ph.D., sono gli autori principali dello studio e borsisti post-dottorato presso HMS.