La recente notizia della prossima disponibilità in Italia di Elacestrant, un farmaco orale rivoluzionario per il trattamento del tumore al seno metastatico, sviluppato grazie al contributo cruciale del polo farmaceutico di Menarini a Pisa, rappresenta ben più di un singolo successo scientifico. Essa incarna e celebra un modello virtuoso di sviluppo regionale che potremmo definire “La Toscana che cura il futuro”.
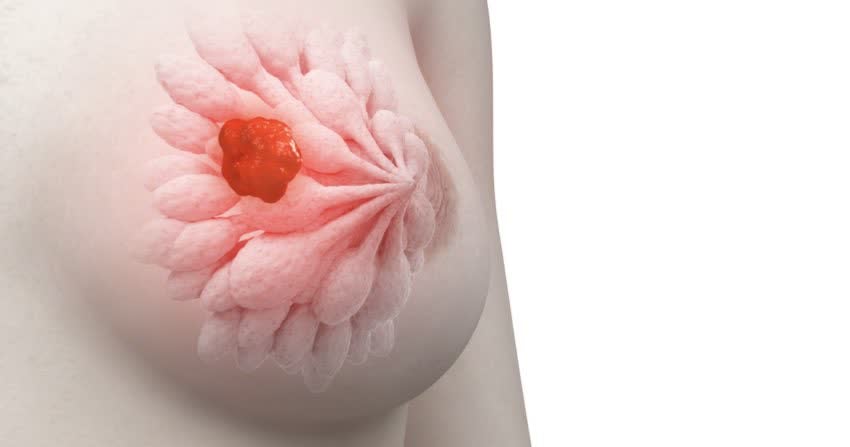
Un modello di sviluppo regionale sostenibile e proiettato al futuro
Questo concetto si fonda su una sinergia profondamente radicata e strategicamente coltivata tra diversi attori chiave: l’eccellenza della ricerca scientifica universitaria e dei centri di ricerca, la capacità innovativa e produttiva dell’industria farmaceutica e biotecnologica, un sistema sanitario regionale attento alle nuove frontiere della terapia e un tessuto sociale che riconosce il valore primario della conoscenza e della dignità umana.
Il contributo di Menarini a Pisa nello sviluppo di Elacestrant non è un evento isolato, ma si inserisce in una tradizione di eccellenza e di investimento nel settore farmaceutico che caratterizza la Toscana. La presenza di aziende come Menarini, capaci di integrare la ricerca di base con lo sviluppo traslazionale e la produzione su larga scala, costituisce un elemento fondamentale di questo ecosistema.
Queste realtà industriali non sono semplici esecutori di scoperte altrui, ma attori proattivi che investono in ricerca e sviluppo, attraggono talenti scientifici e creano un ambiente fertile per l’innovazione. La loro prossimità con le università e i centri di ricerca facilita lo scambio di conoscenze, la collaborazione su progetti specifici e la formazione di nuove generazioni di ricercatori e professionisti.
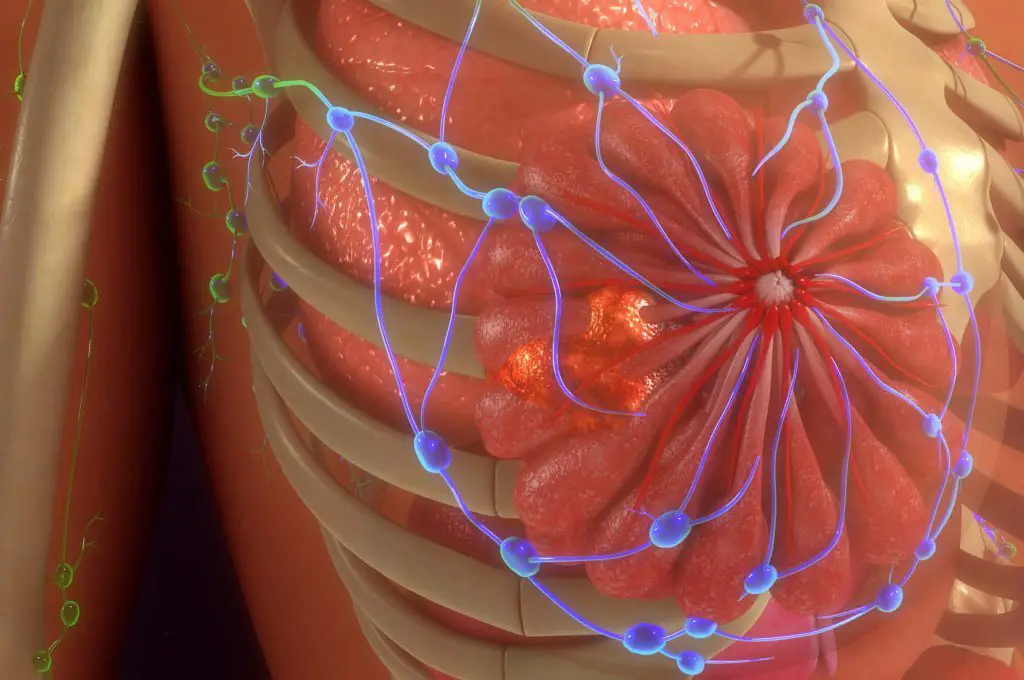
Il vero motore de “La Toscana che cura il futuro” risiede nella fitta rete di interconnessioni tra il mondo accademico, i centri di ricerca pubblici e privati e il tessuto industriale. Le università toscane, con i loro dipartimenti scientifici all’avanguardia e i loro laboratori di ricerca, rappresentano la fucina delle nuove idee e delle scoperte fondamentali.
I centri di ricerca, spesso specializzati in ambiti specifici come l’oncologia, la genetica o le biotecnologie, traducono queste scoperte in potenziali applicazioni terapeutiche. L’industria, a sua volta, raccoglie queste promesse scientifiche, investendo nelle fasi di sviluppo preclinico e clinico, superando le sfide regolatorie e portando infine i farmaci innovativi ai pazienti. Questo flusso bidirezionale di conoscenze, competenze e risorse è cruciale per accelerare il processo di innovazione e garantire che le scoperte scientifiche si traducano concretamente in benefici per la salute.
Un altro pilastro fondamentale di questo modello è rappresentato dal sistema sanitario regionale toscano, che dimostra una notevole apertura verso l’innovazione terapeutica e una forte attenzione alle esigenze dei pazienti. La disponibilità a integrare rapidamente nuove terapie efficaci, come Elacestrant, nei protocolli di trattamento e la capacità di collaborare con i centri di ricerca e l’industria per la conduzione di studi clinici sono elementi distintivi. Questa sinergia tra ricerca, industria e sanità garantisce che i progressi scientifici si traducano in un miglioramento concreto della qualità dell’assistenza sanitaria offerta ai cittadini toscani e, in questo caso specifico, ai pazienti affetti da tumore al seno metastatico.
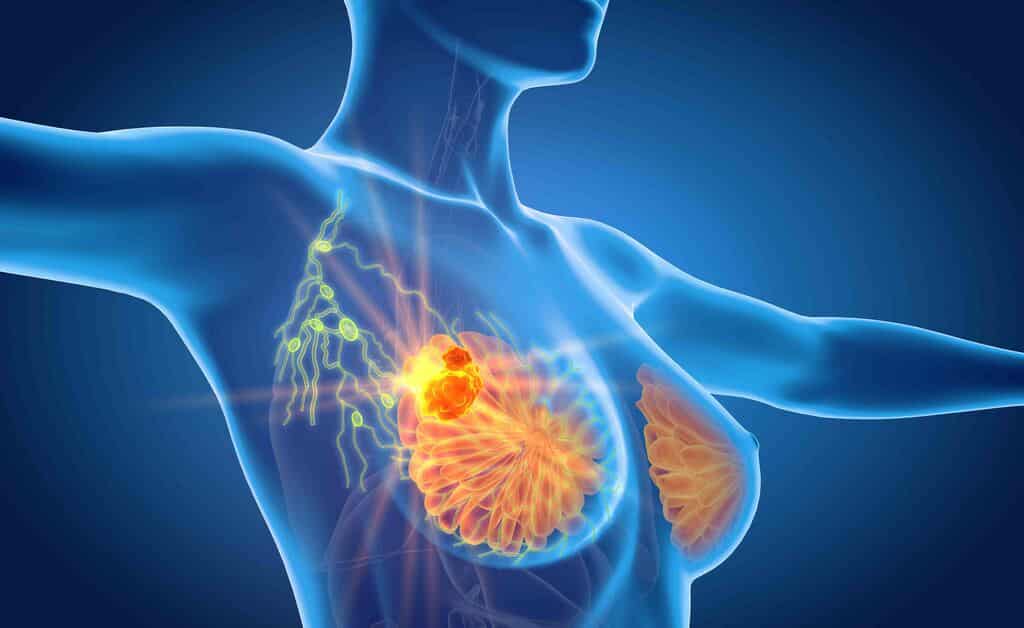
Alla base di questo ecosistema virtuoso si trova un profondo investimento nella conoscenza e nella dignità delle persone. La Toscana riconosce il valore intrinseco della ricerca scientifica come motore di progresso e di benessere collettivo. L’attenzione alla dignità dei pazienti si traduce in un impegno costante per sviluppare terapie più efficaci e meno invasive, che possano migliorare la loro qualità di vita anche nelle fasi più difficili della malattia. Elacestrant, con la sua somministrazione orale e la sua capacità di rallentare la progressione della malattia senza ricorrere alla chemioterapia, è un esempio tangibile di questo impegno.
“La Toscana che cura il futuro” non è solo uno slogan, ma un modello di sviluppo regionale che crea valore per l’intera comunità. L’innovazione nel settore farmaceutico e biotecnologico genera nuove opportunità economiche, attrae investimenti e talenti, e rafforza la reputazione della regione a livello nazionale e internazionale. Questo circolo virtuoso alimenta ulteriormente la ricerca e l’innovazione, creando un futuro in cui la Toscana può continuare a essere protagonista nella cura delle malattie e nel miglioramento della vita delle persone.
La storia di Elacestrant, un farmaco nato dalla collaborazione tra intelligenza scientifica, capacità industriale e attenzione al paziente in Toscana, è un faro che illumina la strada verso un futuro in cui la scienza e l’umanità si incontrano per affrontare le sfide più difficili.
Elacestrant: una speranza concreta nella terapia del tumore al seno metastatico
L’affermazione che Elacestrant “non guarisce, ma blocca le metastasi” racchiude in sé una profonda verità e una promessa significativa per le pazienti affette da tumore al seno metastatico. In uno scenario clinico spesso caratterizzato dalla progressione inesorabile della malattia nonostante i trattamenti disponibili, emerge come un’arma innovativa, capace di intervenire laddove altre terapie endocrine hanno perso la loro efficacia. La sua peculiarità di essere somministrato per via orale, sotto forma di una semplice compressa, rappresenta un ulteriore elemento di svolta, offrendo un’alternativa alla chemioterapia, notoriamente gravata da effetti collaterali debilitanti che impattano significativamente sulla qualità della vita delle pazienti.
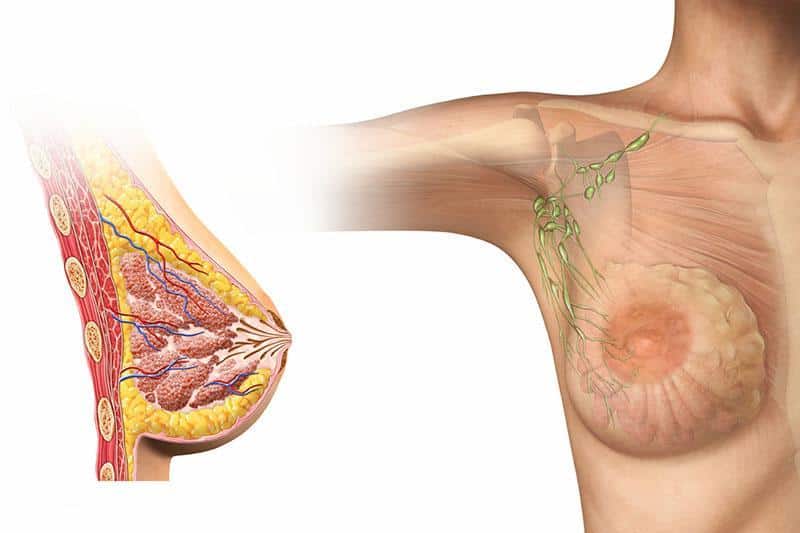
Per comprendere appieno il valore di Elacestrant, è fondamentale analizzarne il meccanismo d’azione. Questo farmaco appartiene alla categoria dei SERD (Selective Estrogen Receptor Degraders) orali. Nelle cellule tumorali del seno positive ai recettori degli estrogeni (ER+), la crescita è spesso alimentata dal legame degli estrogeni a tali recettori. Le terapie endocrine tradizionali mirano a bloccare questo legame o a ridurre la produzione di estrogeni.
Nel contesto del tumore al seno metastatico, le cellule tumorali possono sviluppare meccanismi di resistenza a queste terapie, spesso attraverso mutazioni nel gene ESR1 che codifica per il recettore degli estrogeni. Queste mutazioni rendono il recettore costitutivamente attivo, ovvero in grado di promuovere la crescita tumorale anche in assenza o in presenza di terapie endocrine standard.
Elacestrant agisce in modo differente. Non si limita a bloccare il recettore degli estrogeni, ma ne promuove attivamente la degradazione e la distruzione all’interno della cellula tumorale. Questo meccanismo d’azione “distruttivo” si dimostra efficace anche in presenza delle mutazioni ESR1, superando uno dei principali ostacoli alla terapia endocrina nel setting metastatico. In sostanza, Elacestrant priva le cellule tumorali del “carburante” ormonale di cui necessitano per proliferare, rallentando o bloccando la progressione della malattia, in particolare la formazione e la crescita di metastasi in sedi distanti.
Uno degli aspetti più significativi di è la sua somministrazione orale. Nel trattamento del tumore al seno metastatico, la chemioterapia rappresenta spesso una tappa inevitabile quando le terapie endocrine cessano di essere efficaci. Tuttavia, la chemioterapia è associata a una vasta gamma di effetti collaterali, tra cui nausea, vomito, affaticamento, perdita di capelli, mielosoppressione e neuropatia, che possono compromettere seriamente la qualità della vita delle pazienti in una fase già delicata della loro malattia.
Elacestrant, offrendo un’opzione terapeutica efficace per via orale, permette potenzialmente di ritardare o evitare il ricorso alla chemioterapia in alcune pazienti. Questo si traduce in un impatto positivo sulla loro qualità della vita, consentendo loro di mantenere una maggiore autonomia, di proseguire le proprie attività quotidiane con minori limitazioni e di preservare il proprio benessere fisico ed emotivo. La possibilità di assumere una compressa a domicilio, senza la necessità di recarsi periodicamente in ospedale per infusioni endovenose, rappresenta un ulteriore vantaggio in termini di praticità e di riduzione del carico assistenziale.
Elacestrant rappresenta un esempio emblematico di come la ricerca scientifica di eccellenza, quando integrata con una solida capacità industriale e un sistema sanitario attento alle esigenze dei pazienti, possa portare a innovazioni terapeutiche in grado di migliorare significativamente la qualità della vita e la prognosi di malattie gravi come il tumore al seno metastatico. La sua origine toscana è motivo di orgoglio per la regione e testimonia un modello di sviluppo basato sulla conoscenza, sulla collaborazione e sull’impegno per la salute e il benessere delle persone, con una risonanza che si estende ben oltre i confini regionali e nazionali.
Dagli studi preclinici all’approvazione regolatoria
L’annuncio della prossima disponibilità di Elacestrant in Italia non rappresenta l’improvvisa comparsa di una soluzione terapeutica, bensì il culmine di un lungo e meticoloso percorso di ricerca e sviluppo, costellato di studi clinici rigorosi e valutazioni da parte delle autorità regolatorie. Comprendere la cronologia di questo processo è fondamentale per apprezzare appieno il significato di questo traguardo e il contributo della scienza toscana in questo contesto.
Come per ogni farmaco innovativo, lo sviluppo ha avuto inizio con una fase preclinica, condotta in laboratori e su modelli animali. In questa fase, i ricercatori hanno studiato il meccanismo d’azione del composto, la sua capacità di interagire con il recettore degli estrogeni e di promuoverne la degradazione, nonché il suo profilo di sicurezza preliminare. I risultati promettenti ottenuti in questi studi hanno fornito la base scientifica per avanzare alla fase successiva: la sperimentazione clinica sull’uomo.
Il San Antonio Breast Cancer Symposium (SABCS) è uno dei congressi più importanti a livello mondiale nel campo della ricerca sul cancro al seno. La presentazione di risultati di studi clinici in questo contesto nel novembre 2024 ha rappresentato un momento cruciale. In questa sede, i ricercatori hanno condiviso dati aggiornati sull’efficacia e la sicurezza del farmaco in pazienti affette da carcinoma mammario ER+, HER2- avanzato o metastatico, con particolare attenzione al sottogruppo di pazienti con mutazioni ESR1.
È probabile che al SABCS 2024 siano stati presentati i risultati dello studio di fase III EMERALD, uno studio pivotal che ha confrontato Elacestrant con la terapia endocrina standard scelta dallo sperimentatore in pazienti che avevano già fallito una o due precedenti linee di terapia endocrina, inclusi inibitori di CDK4/6.
I dati presentati in questo contesto hanno verosimilmente dimostrato un beneficio significativo in termini di sopravvivenza libera da progressione (PFS) nel braccio trattato con Elacestrant, in particolare nel sottogruppo di pazienti con mutazioni ESR1, confermando il potenziale del farmaco nel superare la resistenza ormonale. La presentazione al SABCS ha permesso alla comunità scientifica internazionale di valutare l’impatto clinico di Elacestrant e di anticiparne il potenziale ruolo nella pratica clinica.
Un passaggio normativo cruciale nel percorso di Elacestrant verso la disponibilità per i pazienti è stata l’approvazione da parte dell’Agenzia Europea per i Medicinali (EMA) nel settembre 2023. L’EMA è l’autorità regolatoria responsabile della valutazione e dell’approvazione dei farmaci nell’Unione Europea. La sua decisione si basa su una rigorosa valutazione dei dati scientifici e clinici presentati dall’azienda farmaceutica, al fine di accertare il rapporto rischio-beneficio del farmaco per la specifica popolazione di pazienti target.
L’approvazione dell’EMA nel settembre 2023, specificamente per pazienti con carcinoma mammario ER+, HER2- localmente avanzato o metastatico con una mutazione attivante del gene ESR1 e che hanno avuto una progressione della malattia dopo almeno una linea di terapia endocrina, inclusi gli inibitori di CDK4/6, ha rappresentato un riconoscimento formale dell’efficacia e della sicurezza del farmaco in questa precisa categoria di pazienti. Questa approvazione ha aperto la strada alla successiva fase di negoziazione del prezzo e rimborso nei singoli stati membri dell’Unione Europea, inclusa l’Italia.
La notizia attuale della disponibilità di Elacestrant in Italia entro tre mesi fa seguito all’approvazione da parte dell’Agenzia Italiana del Farmaco (AIFA). L’AIFA è l’ente regolatorio nazionale che valuta e autorizza l’immissione in commercio dei farmaci in Italia, tenendo conto delle specificità del sistema sanitario nazionale e delle esigenze dei pazienti italiani. L’approvazione dell’AIFA e la successiva decisione sulla rimborsabilità sono passaggi essenziali per rendere un farmaco effettivamente accessibile ai pazienti.
L’annuncio della disponibilità entro tre mesi suggerisce che le procedure di negoziazione del prezzo e di definizione delle modalità di prescrizione e dispensazione sono state completate o sono in fase conclusiva. Questo rappresenta un risultato significativo, in quanto traduce l’approvazione regolatoria europea in una concreta opportunità terapeutica per le pazienti italiane affette da tumore al seno metastatico con le caratteristiche specifiche per cui Elacestrant ha dimostrato efficacia.
Trovi tutti gli studi clinici cliccando su National Cancer Institute (NCI).