La ricerca e lo sviluppo di isole pancreatiche derivate da cellule staminali rappresentano un campo di studio di grande interesse come potenziale fonte illimitata di cellule produttrici di insulina trapiantabili. Questa strategia terapeutica per il diabete di tipo 1 mira a superare la dipendenza dalla disponibilità di cellule pancreatiche ottenute da donatori deceduti, una risorsa intrinsecamente limitata.
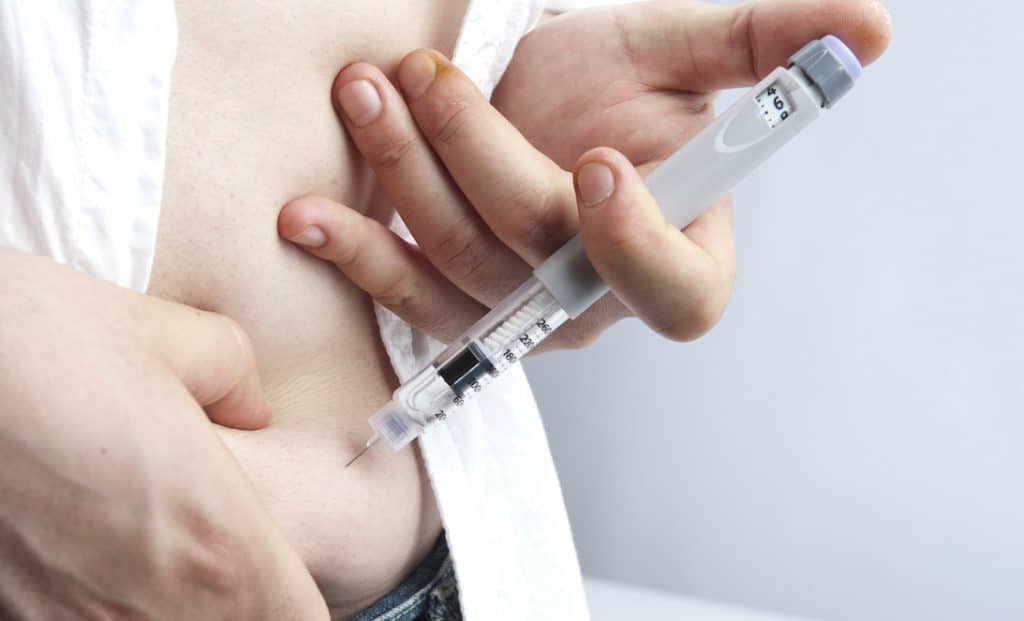
La promettente frontiera delle Isole pancreatiche da cellule staminali per la terapia del diabete di tipo 1
I primi tentativi di utilizzare il trapianto di cellule insulari come approccio curativo per il diabete di tipo 1 risalgono a circa mezzo secolo fa. Inizialmente, i medici si concentrarono sull’isolamento di tessuto pancreatico contenente isole di Langerhans, le strutture cellulari responsabili della produzione di insulina salvavita, da donatori deceduti. Grazie a significativi progressi scientifici e a tassi di successo sempre maggiori, il trapianto di cellule insulari ha ottenuto l’approvazione come terapia consolidata in Canada e in Europa. Negli Stati Uniti, tuttavia, la tecnica è ancora considerata di natura sperimentale.
Un team di endocrinologi e specialisti in medicina rigenerativa operanti nei Paesi Bassi ha compiuto notevoli passi avanti in questo campo. Attraverso una serie di innovativi sviluppi metodologici, sono stati messi a punto protocolli che migliorano significativamente l’efficienza della produzione di cellule staminali utilizzate per generare isole pancreatiche funzionali, capaci di secernere insulina in risposta agli stimoli fisiologici.
I ricercatori hanno inoltre sviluppato strategie efficaci per preservare l’integrità strutturale e funzionale (“architettura”) delle isole cellulari che emergono dai loro sofisticati processi di produzione in vitro. Nel complesso, questi recenti progressi suggeriscono la concreta possibilità di disporre in futuro di una fonte affidabile e “su richiesta” di isole pancreatiche derivate da cellule staminali, con un focus specifico sulle cellule beta, il tipo cellulare insulare primariamente responsabile della sintesi e del rilascio di insulina.

Come sottolinea il dottor Bahareh Rajaei, autore principale dello studio ed esperto di medicina rigenerativa presso il Centro medico dell’Università di Leida, la progressiva perdita delle cellule β pancreatiche rappresenta un segno distintivo del diabete di tipo 1. Questa patologia autoimmune è il risultato di una complessa interazione tra fattori genetici e ambientali che conduce alla distruzione selettiva delle cellule beta da parte del sistema immunitario dell’organismo.
La conseguente insufficiente massa di cellule β funzionali determina un aumento patologico della concentrazione di glucosio nel sangue, una condizione nota come iperglicemia. Se non adeguatamente trattata, l’iperglicemia può evolvere in gravi complicanze metaboliche, come la chetoacidosi diabetica, che può avere esiti fatali.
Il diabete di tipo 1 rappresenta una seria sfida per la salute pubblica a livello mondiale, una condizione cronica che accompagna le persone per tutta la vita e che affligge milioni di individui. Le stime dell’Organizzazione Mondiale della Sanità indicano che nel 2022, l’anno più recente per il quale sono disponibili statistiche complete, circa 8,75 milioni di persone convivevano con il diabete di tipo 1.

Bambini e giovani adulti costituiscono una porzione significativa di questa popolazione colpita, caratterizzata dall’incapacità intrinseca dell’organismo di produrre l’insulina necessaria per la sopravvivenza. Di conseguenza, le persone con diabete di tipo 1 necessitano di una somministrazione quotidiana di insulina esogena per mantenere sotto controllo i livelli di glucosio nel sangue e prevenire gravi complicanze.
All’interno del pancreas, le cellule insulari, sia di tipo alfa che beta, si organizzano in aggregati cellulari specializzati. Questi gruppi di cellule endocrine costituiscono le isole di Langerhans, microstrutture distinte immerse nel tessuto esocrino del pancreas. Le cellule alfa sono deputate alla produzione di glucagone, un ormone pancreatico che svolge un ruolo cruciale nella regolazione dei livelli di glucosio nel sangue, stimolando il fegato a rilasciare glicogeno (la forma di riserva del glucosio) nel circolo sanguigno, con conseguente aumento della glicemia.
Le cellule beta, al contrario, sono le responsabili della sintesi e del rilascio di insulina, l’ormone che agisce abbassando i livelli di glucosio nel sangue, facilitandone l’assorbimento da parte delle cellule e promuovendone la conversione in glicogeno per l’immagazzinamento. L’assenza o il grave danneggiamento delle cellule beta compromette irrimediabilmente il controllo fisiologico del glucosio, aprendo la strada all’insorgenza del diabete di tipo 1.
Le Isole beta da cellule Staminali: una speranza concreta
Endocrinologi ed esperti nel campo della medicina rigenerativa nutrono un crescente ottimismo riguardo al potenziale delle isole beta generate a partire da cellule staminali come terapia risolutiva per il diabete di tipo 1 in un futuro non lontano. L’attuale approccio terapeutico basato sul trapianto di cellule insulari provenienti da donatori deceduti presenta limitazioni significative e non si configura come un’opzione adatta a tutti i pazienti affetti da questa patologia autoimmune.

La terapia con cellule insulari da donatore richiede l’impiego di farmaci immunosoppressori per prevenire il rigetto, una necessità che implica un bilanciamento tra i benefici del trapianto e i rischi associati all’immunodepressione. Di conseguenza, i medici tendono a offrire questa forma di trapianto solo a quei pazienti per i quali i potenziali vantaggi superano i pericoli legati alla soppressione del sistema immunitario. È inoltre importante sottolineare che la ricezione di un trapianto non sempre esonera completamente i pazienti dalla necessità di assumere quotidianamente insulina esogena; in molti casi, si rende comunque necessario un supplemento giornaliero dell’ormone salvavita per mantenere un adeguato controllo glicemico.
Il settore ha compiuto progressi notevoli grazie al continuo affinamento delle conoscenze scientifiche da parte degli esperti di medicina rigenerativa e alla crescente focalizzazione sulle cellule staminali come fonte potenzialmente illimitata di cellule insulari funzionali. Negli Stati Uniti, dove il trapianto di cellule insulari è ancora considerato una procedura sperimentale, la Vertex Pharmaceuticals, con sede a South Boston, Massachusetts, è attivamente impegnata in attività di ricerca e in studi clinici volti a validare l’efficacia e la sicurezza di questa promettente strategia terapeutica. La collaborazione tra l’azienda e i centri medici specializzati ha già prodotto risultati incoraggianti nel campo del trapianto di isole pancreatiche derivate da cellule staminali.
Secondo il team di ricerca operante nei Paesi Bassi, la sfida attuale consiste nello sviluppo di protocolli e tecniche standardizzate che garantiscano una fornitura costante e affidabile di cellule staminali vitali e trapiantabili, in grado di soddisfare elevati standard qualitativi e di purezza, minimizzando la presenza di cellule indesiderate. In risposta a questa esigenza cruciale, il dottor Rajaei e il suo team di collaboratori hanno messo a punto una nuova e innovativa tecnica di purificazione cellulare.

Questo metodo avanzato è specificamente progettato per creare isolotti pancreatici funzionali a partire da cellule staminali, seguendo rigorose pratiche di produzione conformi agli standard clinici. L’obiettivo primario di questa ricerca è quello di rendere disponibile una terapia cellulare efficace e sicura per la cura del diabete di tipo 1, superando le limitazioni intrinseche legate alla disponibilità di cellule da donatore e riducendo la necessità di immunosoppressione a lungo termine.
Un potenziale illimitato per la terapia cellulare
La ricerca condotta nei laboratori di Leida ha fornito prove convincenti della funzionalità a lungo termine delle isole beta pancreatiche generate a partire da cellule staminali una volta trapiantate in modelli animali. La tecnologia alla base di questo promettente approccio terapeutico si fonda sull’utilizzo di cellule staminali pluripotenti, cellule dotate della straordinaria capacità di auto-rinnovarsi indefinitamente e di differenziarsi in un’ampia gamma di tipi cellulari specifici per i diversi tessuti dell’organismo.
Le cellule staminali pluripotenti possono essere concettualizzate come delle “tabule rase” biologiche, capaci di evolvere in qualsiasi tipo di cellula specializzata richiesta dall’organismo per la riparazione o la sostituzione di tessuti danneggiati. Il gruppo di ricerca guidato dal dottor Rajaei ha focalizzato il proprio lavoro sulle cellule staminali pluripotenti indotte (iPSC), una tipologia di cellule staminali ottenute riprogrammando cellule adulte mature in uno stato pluripotente.

Queste iPSC vengono successivamente differenziate in laboratorio, attraverso specifici protocolli di coltura, in cellule che mimano le caratteristiche funzionali delle isole pancreatiche native, prima di essere trapiantate nei modelli animali per valutarne l’efficacia. L’obiettivo primario dello studio è stato quello di tracciare il destino e la funzionalità di queste cellule trapiantate nel contesto biologico di un organismo vivente.
Come sottolineato dal dottor Rajaei nel suo lavoro, “il trapianto di isole pancreatiche derivate da cellule staminali pluripotenti umane rappresenta una promettente terapia di sostituzione delle cellule β per i pazienti affetti da diabete di tipo 1, offrendo una potenziale riserva cellulare illimitata, in grado di superare le limitazioni legate alla disponibilità di donatori”.
Il team ha evidenziato come alcune delle sfide precedentemente riscontrate nel settore includessero la mancanza di uniformità del prodotto cellulare finale e le fasi di purificazione, che spesso compromettevano l’integrità strutturale e funzionale degli isolotti. I nuovi protocolli sviluppati dal gruppo di ricerca sono riusciti a superare con successo questi ostacoli, aprendo la strada a una produzione più standardizzata e di alta qualità.
Guardando al futuro del settore della terapia cellulare, il dottor Rajaei e il suo team sostengono che le innovative tecniche di produzione da loro sviluppate potrebbero verosimilmente apportare benefici significativi anche ad altre patologie potenzialmente trattabili attraverso infusioni di cellule staminali. “Questo metodo potrebbe contribuire in modo sostanziale alla generazione di terapie cellulari migliorate per scopi di medicina rigenerativa che vanno ben oltre il campo specifico delle cellule staminali insulari, aprendo nuove frontiere nel trattamento di diverse patologie degenerative e lesioni tissutali”, ha concluso il dottor Rajaei, sottolineando la potenziale versatilità della loro piattaforma tecnologica.
Lo studio è stato pubblicato su Science Translational Medicine.