Una nuova ricerca ha confrontato la schizofrenia e la demenza frontotemporale, disturbi che situati entrambi nelle regioni del lobo frontale e temporale del cervello. Si tratta di un’intuizione che risale addirittura al 1899 per opera di Emil Kraepelin, che parlò di “dementia praecox” per descrivere il progressivo declino mentale ed emotivo dei giovani pazienti.
Il suo approccio è stato rapidamente messo in discussione, poiché solo il 25% delle persone colpite ha mostrato questa forma di progressione della malattia. Ma ora, con l’aiuto dell’imaging e dell’apprendimento automatico, gli scienziati hanno trovato le prime indicazioni valide di modelli neuroanatomici nel cervello che assomigliano alla firma dei pazienti con demenza frontotemporale.
I risultati dello studio sono stati pubblicati sulla rivista scientifica JAMA Psychiatry.
Schizofrenia e demenza frontotemporale: ecco che cosa ha rivelato la nuova ricerca
È raro che gli scienziati nella ricerca di base diano affidamento a scoperte apparentemente obsolete che hanno più di 120 anni. Nel caso di Nikolaos Koutsouleris e Matthias Schroeter, che sono ricercatori e medici, questa è stata addirittura un incentivo. Si tratta di Emil Kraepelin, fondatore del Max Planck Institute for Psychiatry (MPI) e dell’ospedale psichiatrico dell’Università Ludwig Maximilian di Monaco (LMU), e del suo termine “dementia praecox”, coniato nel 1899.
Questa è stata la sua definizione per i giovani adulti che si ritirano sempre più dalla realtà e cadono in uno stato irreversibile, simile alla demenza frontotemporale. Kraepelin è vissuto fino a vedere il suo concetto confutato. All’inizio del 20° secolo, gli esperti stavano iniziando a usare il termine “schizofrenia” per questi pazienti, poiché la malattia non ha un decorso così negativo in tutte le persone colpite.
Kraepelin ha pensato alla demenza frontotemporale, poiché ha ipotizzato che la ragione del decorso a volte debilitante dei pazienti si trovasse nelle aree del lobo frontale e temporale del cervello. È qui che la personalità, il comportamento sociale e l’empatia sono controllati: “Ma questa idea è andata perduta poiché nel cervello di questi pazienti non è stata trovata alcuna prova patologica per i processi neurodegenerativi osservati nel morbo di Alzheimer”, ha osservato Koutsouleris, che lavora nei luoghi di lavoro di Kraepelin, MPI e LMU.
“Sin da quando sono diventato uno psichiatra, ho voluto lavorare su questa domanda”. Quindici anni dopo con un set di informazioni sufficientemente grandi, tecniche di imaging e algoritmi, il Professore aveva gli strumenti a portata di mano per trovare potenzialmente risposte. Lo scienziato ha trovato il partner giusto in Matthias Schroeter, che studia le malattie neurodegenerative, in particolare le demenze frontotemporali, al Max Planck Institute for Human Cognitive and Brain Sciences.
La demenza frontotemporale (FTD), in particolare la variante comportamentale (bvFTD), è difficile da riconoscere nelle sue fasi iniziali perché è spesso confusa con la schizofrenia. Pertanto, le somiglianze sono ovvie: nei malati di entrambi i gruppi, si verificano cambiamenti nella personalità e nel comportamento. Si verifica uno sviluppo spesso drammatico per le persone affette e i parenti.
Poiché entrambi i disturbi si trovano nelle regioni frontale, temporale e insulare del cervello, è automatico anche confrontarli direttamente: “Sembrano essere su uno spettro di sintomi simile, quindi abbiamo voluto cercare segni o schemi comuni nel cervello”, dice Koutsouleris, descrivendo il suo piano.
Grazie ad una squadra di esperti internazionale, Koutsouleris e Schroeter hanno sfruttato l’intelligenza artificiale per addestrare i classificatori neuroanatomici di entrambi i disturbi, che hanno applicato ai dati cerebrali di diverse coorti. Il risultato, è stato che il 41% dei pazienti affetti da schizofrenia soddisfaceva i criteri di classificazione per demenza frontotemporale bvFTD.
“Quando abbiamo visto questo anche nei pazienti schizofrenici, ha suonato un campanello, indicando una somiglianza tra i due disturbi”, hanno raccontato Koutsouleris e Schroeter. Il gruppo di ricercatori ha rivelato che più alto era il punteggio bvFTD dei pazienti, che misurava la somiglianza tra i due disturbi, maggiore era la probabilità che avessero un fenotipo “simile a bvFTD” e meno probabile che migliorassero i loro sintomi nell’arco di due anni.
“Volevo solo sapere perché il mio paziente di 23 anni con sintomi di schizofrenia all’esordio, come allucinazioni, deliri e deficit cognitivi, non era migliorato affatto, anche dopo due anni, mentre un altro che aveva iniziato altrettanto male stava continuando la sua formazione e avendo trovato una ragazza. Più e più volte, ho visto questi giovani che non si sono ripresi affatto”, ha affermato Koutsouleris.
Quando i ricercatori hanno verificato le correlazioni anche in pazienti ad alto rischio come il 23enne, hanno trovato conferma a livello neuroanatomico di ciò che Kraepelin era stato il primo a descrivere con decisione: nessun miglioramento di sorta nelle condizioni di alcuni pazienti, piuttosto l’opposto.
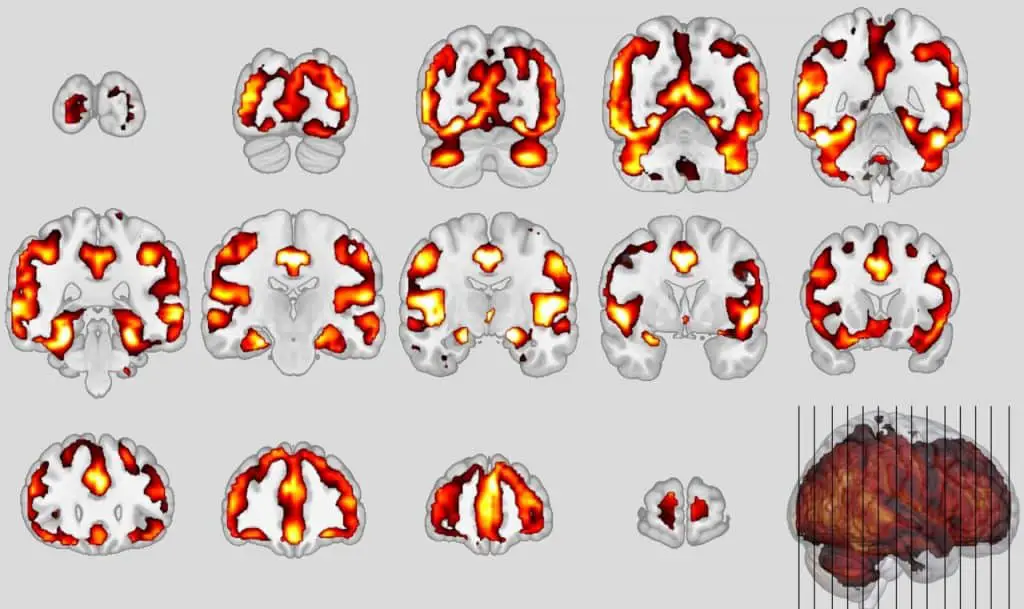
Strutture neuronali simili sono state colpite, in particolare la cosiddetta rete in modalità predefinita e la rete di salienza del cervello, responsabile del controllo dell’attenzione, dell’empatia e del comportamento sociale, ha mostrato diminuzioni di volume nell’area della materia grigia che ospita i neuroni. Nella demenza frontotemporale bvFTD, alcuni neuroni (neuroni von Economo) muoiono; nella schizofrenia, anche questi neuroni sono alterati.
Questo si rifletteva nel punteggio neuroanatomico: dopo un anno era raddoppiato in queste persone gravemente colpite. A titolo di confronto, gli scienziati avevano anche calcolato il punteggio di Alzheimer utilizzando un classificatore specifico e non vi hanno trovato questi effetti: “Ciò significa che il concetto di dementia praecox non può più essere completamente spazzato via; forniamo la prima prova valida che Kraepelin non aveva torto, almeno in alcuni dei pazienti”, ha spiegato Schroeter.
Oggi, o nel prossimo futuro, questo significa che gli esperti saranno in grado di prevedere a quale sottogruppo appartengono i pazienti. “Quindi un supporto terapeutico intensivo può essere avviato in una fase iniziale per sfruttare qualsiasi potenziale di recupero residuo”, ha concluso Koutsouleris. Inoltre, per questo sottogruppo potrebbero essere sviluppate nuove terapie personalizzate che promuovano una corretta maturazione e connettività dei neuroni colpiti e prevengano la loro progressiva distruzione come parte del processo patologico.