Una nuova ricerca condotta dall’Università dell’Arizona Health Sciences, suggerisce che la precedente vaccinazione contro il COVID-19 non ha impedito al sistema immunitario di sviluppare una risposta protettiva contro i ceppi Delta e Omicron. Tuttavia, la produzione di anticorpi specifici per le nuove mutazioni ha mostrato una leggera diminuzione.
Vaccinazione COVID-19 e risposta immunitaria alle varianti
Deepta Bhattacharya, Ph.D., direttore esecutivo inaugurale dell’U of A Health Sciences Center for Advanced Molecular and Immunological Therapies e professore di immunobiologia presso l’U of A College of Medicine–Tucson, ha spiegato il fulcro della ricerca: “Ciò che volevamo davvero affrontare è questa domanda fondamentale su come il sistema immunitario si adatta quando si è esposti a un virus e poi il virus cambia: è possibile generare nuove risposte contro queste nuove mutazioni?”.
I risultati indicano che, pur essendoci una leggera diminuzione delle risposte alle parti mutate del virus nelle persone vaccinate che contraggono l’infezione, la risposta protettiva complessiva è significativamente più elevata rispetto a chi non era vaccinato al momento dell’infezione.
Il team di ricerca ha esaminato le risposte anticorpali alle infezioni da varianti Delta e Omicron in individui che erano stati precedentemente vaccinati o meno contro il ceppo originale del SARS-CoV-2. È emerso che la produzione complessiva di anticorpi per le varianti Delta e Omicron era maggiore nelle persone che avevano ricevuto il vaccino originale contro il COVID-19 rispetto a quelle non vaccinate. Ciò nonostante, la produzione di anticorpi specifici per la variante Delta è risultata parzialmente soppressa nelle persone precedentemente vaccinate rispetto a quelle non vaccinate.
Oltre l’imprinting: nuove strategie per i vaccini
Il Dr. Deepta Bhattacharya ha chiarito che sebbene la vaccinazione contro il ceppo virale originale di SARS-CoV-2 offra una robusta risposta anticorpale protettiva generale contro le varianti successive come Delta, si osserva una leggera diminuzione nella produzione di anticorpi specifici per le parti mutate del virus rispetto agli individui non vaccinati. Egli ha sottolineato come, in ogni variante, esistano comunque porzioni del virus che rimangono invariate, e gli anticorpi diretti contro queste parti conservate si rivelano estremamente protettivi.
Questo suggerisce che, nonostante un certo “imprinting antigenico” – ovvero una soppressione della risposta immunitaria originale quando si incontra una versione leggermente diversa del virus – i cambiamenti immunitari indotti potrebbero essere troppo marginali per avere conseguenze funzionali significative per il SARS-CoV-2.
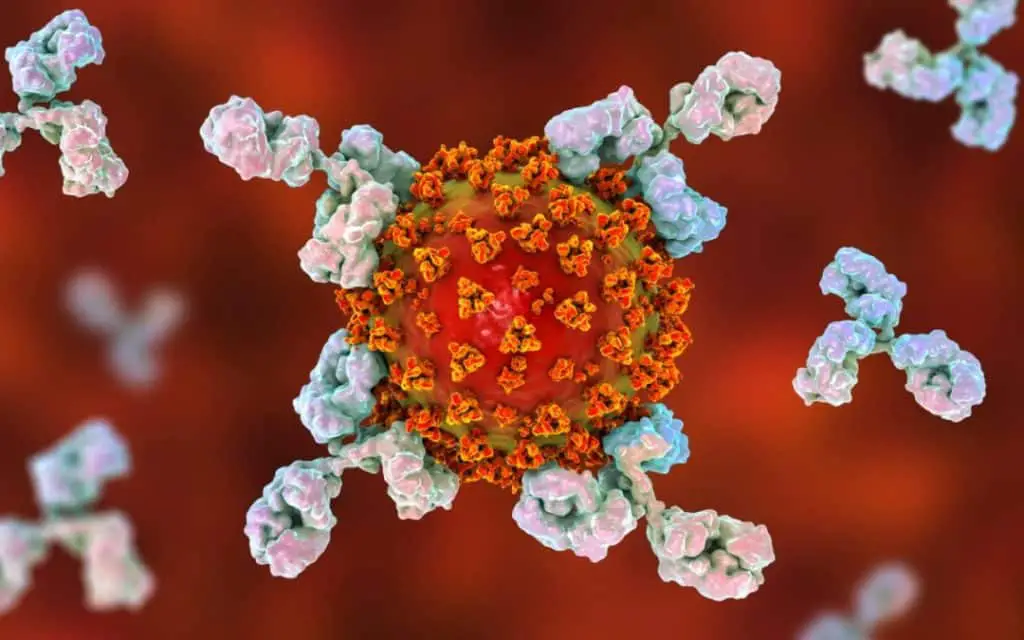
Un aspetto particolarmente intrigante emerso dallo studio è che persino gli individui la cui primissima esposizione al virus è stata con le varianti Delta o Omicron, e che quindi non avevano alcuna immunità pregressa, hanno mostrato risposte anticorpali molto deboli contro le porzioni mutate del virus. Questa osservazione, secondo Bhattacharya, membro del BIO5 Institute dell’università, evidenzia un’opportunità cruciale per lo sviluppo di vaccini con metodologie innovative, capaci di elicitare risposte immunitarie più ampie e robuste.
Se i ricercatori riusciranno a identificare con precisione quali parti del virus sono responsabili dell’elusione del sistema immunitario, sarà possibile progettare vaccini che assicurino un riconoscimento efficace dell’intero virus. Questo approccio è fondamentale per ampliare la risposta immunitaria e renderla più resiliente di fronte alle inevitabili mutazioni virali future, garantendo una protezione più completa e duratura.
L’imprinting antigenico e la progettazione dei vaccini futuri
Il Dottor Deepta Bhattacharya mira a esplorare in dettaglio le ragioni profonde alla base della soppressione delle risposte anticorpali de novo da parte dell’immunità preesistente, un fenomeno noto come imprinting antigenico. Comprendere appieno i meccanismi molecolari e cellulari attraverso i quali una precedente esposizione a un antigene (sia tramite infezione naturale che vaccinazione) modula o attenua la capacità del sistema immunitario di generare nuove risposte a varianti antigeniche successive è di cruciale importanza.
Questo implica un’analisi approfondita delle dinamiche dei linfociti B, in particolare come la memoria B-cellulare preesistente, altamente affine all’antigene originale, possa dominare la risposta, limitando l’espansione e la differenziazione di nuove popolazioni di linfociti B in grado di riconoscere efficacemente le mutazioni virali. Sarà necessario investigare se questa soppressione sia dovuta a competizione per risorse immunologiche, a segnali regolatori che inibiscono l’attivazione di linfociti B vergini, o a una combinazione complessa di questi fattori.
Le informazioni derivanti da questa ricerca potrebbero essere direttamente applicate allo sviluppo di schemi logici e ottimizzati per la somministrazione di vaccini e richiami. Attualmente, molte strategie vaccinali si basano su approcci empirici; tuttavia, una comprensione meccanicistica dell’imprinting antigenico permetterebbe una progettazione più razionale.
Questa profonda comprensione potrebbe guidare lo sviluppo di strategie di somministrazione vaccinale più intelligenti. Per esempio, potremmo modulare i tempi di somministrazione per trovare l’intervallo ideale tra le dosi iniziali e i richiami. Questo permetterebbe al sistema immunitario di sviluppare risposte anticorpali ampie e diverse prima che l’imprinting antigenico diventi troppo predominante.
Inoltre, una conoscenza più approfondita ci consentirebbe di sviluppare vaccini eterologhi o multivarianti. Se capiamo come l’immunità pregressa influenza le risposte alle nuove varianti, potremmo progettare richiami che presentano antigeni mutati in modi specifici, stimolando selettivamente nuove risposte e superando la dominanza di quelle preesistenti. Questo potrebbe tradursi nell’uso di diverse piattaforme vaccinali per i richiami o nell’incorporazione di epitopi specifici delle varianti in nuove formulazioni.
Un altro aspetto fondamentale è la possibilità di identificare marcatori predittivi. Riconoscere indicatori immunologici o genetici che predispongono un individuo a una maggiore suscettibilità all’imprinting antigenico ci permetterebbe di adottare approcci di vaccinazione personalizzati. Infine, sebbene gran parte della ricerca si concentri sugli anticorpi, è cruciale affrontare anche la risposta delle cellule T, sia citotossiche che helper. Comprendere come l’imprinting influenzi queste cellule è vitale, poiché esse svolgono un ruolo chiave nella rimozione virale e nella memoria immunitaria a lungo termine.
In sintesi, una comprensione dettagliata delle cause della soppressione delle nuove risposte anticorpali non solo amplierà la nostra conoscenza fondamentale dell’immunologia, ma ci fornirà anche gli strumenti per progettare interventi vaccinali più efficaci, resilienti e capaci di adattarsi contro patogeni in continua evoluzione, come i virus respiratori.
Lo studio è stato pubblicato su Nature Immunology.