Uno studio condotto da un team di ricercatori dell’Institute for Diabetes, Obesity and Metabolism presso la Perelman School of Medicine dell’Università della Pennsylvania, ha rivelato per la prima volta che durante lo sviluppo del diabete di tipo 1, quando le cellule produttrici di insulina nel pancreas sono attaccate dai linfociti T, le cellule pancreatiche si riprogrammano nel tentativo di sopprimere il T autoimmune.
I risultati della ricerca sono stati pubblicati sulla rivista scientifica Nature Metabolism.
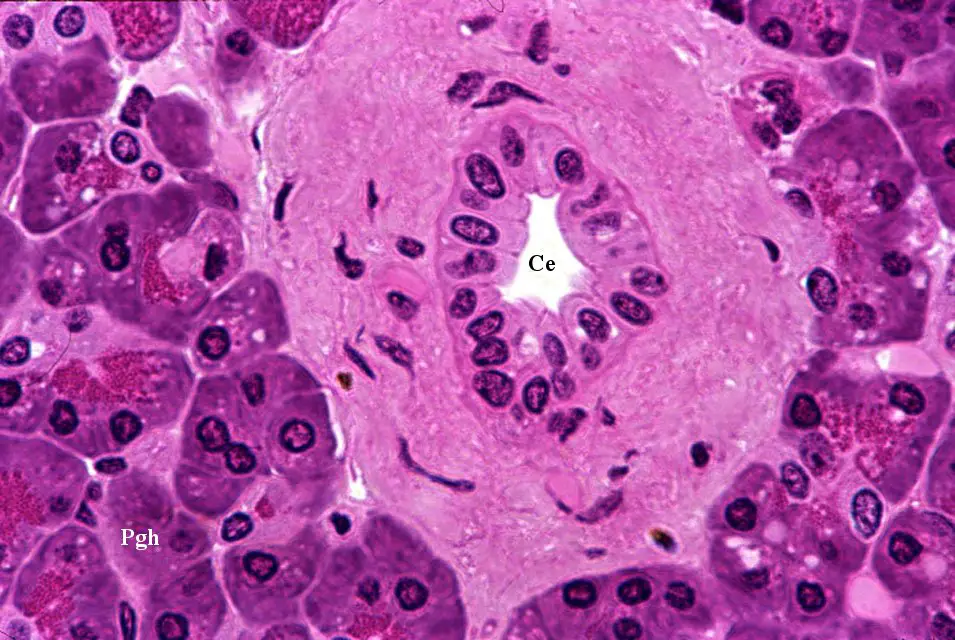
Cellule pancreatiche: ecco cosa succede quando si sta sviluppando il diabete di tipo 1
“I primi eventi che si verificano in un paziente che sta sviluppando il diabete di tipo 1, gli eventi che innescano l’autoimmunità, sono stati difficili da definire per i ricercatori a causa della nostra incapacità di praticare una biopsia al pancreas e dal fatto che la diagnosi clinica viene eseguita successivamente alla distruzione cellulare”, ha affermato l’autore senior Golnaz Vahedi, Ph.D., professore associato di genetica e membro dell’Institute for Diabetes, Obesity and Metabolism presso la Perelman School of Medicine dell’Università della Pennsylvania.
“Ecco perché è così importante sviluppare una migliore comprensione dei primi eventi molecolari nella patogenesi del diabete T1, in modo da poter scoprire di più sull’identificazione dei biomarcatori e sulla prevenzione delle malattie“, ha continuato Vahedi.
Le malattie autoimmuni, che colpiscono ben 23,5 milioni di americani, si verificano quando il sistema immunitario del corpo attacca e distrugge organi, tessuti e cellule sani. Esistono più di 80 tipi di malattie autoimmuni, tra cui l’artrite reumatoide, la malattia infiammatoria intestinale e il diabete di tipo 1. In quest’ultimo, le cellule immunitarie chiamate linfociti T attaccano e distruggono le celle beta pancreatiche che secernono insulina e il pancreas smette di produrre insulina, l’ormone che controlla i livelli di zucchero nel sangue.
“Anche se potrebbe essere un tentativo in definitiva fallito del pancreas di limitare la risposta adattativa dei linfociti T responsabile della distruzione delle cellule beta, questa scoperta che le cellule pancreatiche duttali sono in grado di svolgere questo ruolo soppressivo nei confronti delle risposte autoimmuni dei linfociti T non ha precedenti”, ha osservato il co- autore senior Klaus Kaestner, Ph.D., Thomas ed Evelyn Suor Butterworth Professore in Genetics.
“Il nostro studio mostra che queste cellule pancreatiche, che in precedenza non erano mai state collegate all’immunità, possono cambiare se stesse per proteggere il pancreas“, ha specificato Kaestner.
Istituito nel 2016, lo Human Pancreas Analysis Program (HPAP) è supportato da una sovvenzione di 28 milioni di dollari del National Institutes of Health con importanti contributi di Penn, University of Florida e Vanderbilt University. L’HPAP, che è co-diretto da Kaestner e Ali Naji MD, Ph.D., J. William White Professore di Surgical Research, ha iniziato a raccogliere tessuti pancreatici da centinaia di donatori di organi deceduti con diagnosi di diabete di tipo 1.
Poiché diversi individui con diabete di tipo 1 sono caratterizzati da autoanticorpi beta-cellulari chiamati decarbossilasi dell’acido glutammico (GAD) nel sangue anni prima della diagnosi clinica, HPAP raccoglie anche campioni da donatori autoanticorpi positivi, che sono a rischio di essere colpiti da diabete di tipo 1 ma non hanno avuto quella diagnosi.
“Il nostro studio ha preso quei campioni di tessuto di qualità e ha creato misurazioni ad alta risoluzione di milioni di cellule pancreatiche da pazienti in vari stadi della progressione del diabete di tipo 1, risultando in un atlante unicellulare di isole pancreatiche”, ha affermato il co-autore senior R. Babak Faryabi, Ph. .D., assistente professore di Patologia e Medicina di Laboratorio e membro principale dell’Epigenetics Institute di Penn.
Gli esami del sangue per verificare i livelli di GAD sono comuni per i soggetti che rischiano di riscontrare una diagnosi di diabete di tipo 1 e i medici lo usano come strumento diagnostico. Un’altra scoperta di questo studio è la nuova comprensione di ciò che sta accadendo a livello molecolare nel pancreas e di come è correlato ai risultati del test GAD.
“La nostra ricerca è la prima a dimostrare che anche quando una persona non è clinicamente considerata colpita da diabete T1, livelli elevati rilevati nel test GAD indicano un rimodellamento trascrizionale su larga scala delle loro cellulare beta“, ha spiegato Naji, co-autore senior dello studi: “Si rafforza l’esigenza per i medici di monitorare da vicino i pazienti con livelli crescenti di GAD, poiché ora sappiamo quali cambiamenti cellulari e molecolari sono in movimento in relazione a quei livelli”.
Sebbene i ricercatori non sappiano ancora se questi cambiamenti trascrizionali stiano contribuendo o siano conseguenze della patogenesi della malattia, la scoperta di cambiamenti fenotipici molecolari nelle cellule pancreatiche di individui positivi agli autoanticorpi fa avanzare la comprensione dei primi cambiamenti pancreatici che si verificano nel diabete T1 e pone le basi per continua ricerca in questo campo.