Un’équipe internazionale di scienziati, sotto la guida autorevole dell’Università di Medicina di Vienna, ha compiuto una scoperta di notevole importanza, portando alla luce sorprendenti analogie nei meccanismi biologici che sottendono patologie apparentemente distinte come il diabete e il cancro. In particolare, la ricerca ha evidenziato il ruolo cruciale della proteina PPARγ (recettore gamma attivato dal proliferatore dei perossisomi), un attore chiave nella complessa regolazione dei processi metabolici dell’organismo, nella modulazione della crescita delle cellule tumorali del cancro alla prostata. Questa rivelazione dischiude scenari inediti nella comprensione delle interconnessioni tra disturbi metabolici e proliferazione neoplastica.
Il PPARγ come anello di congiunzione tra diabete e cancro alla prostata
È ormai consolidata nella ricerca medica la conoscenza del PPARγ come target farmacologico primario per alcuni farmaci impiegati nel trattamento del diabete mellito di tipo 2. I risultati di questo innovativo studio ampliano significativamente la portata di tale conoscenza, suggerendo con forza che questi stessi farmaci, originariamente sviluppati per modulare la sensibilità insulinica, potrebbero rappresentare una strategia terapeutica promettente anche nel contesto del trattamento del cancro alla prostata. Questa convergenza di bersagli molecolari apre prospettive entusiasmanti per lo sviluppo di approcci terapeutici multifattoriali, capaci di agire simultaneamente su patologie con meccanismi patogenetici inattesi ma profondamente interconnessi.
Il PPARγ riveste da tempo un ruolo centrale nella ricerca sul diabete, essendo riconosciuto per la sua influenza determinante sulla sensibilità all’insulina, un aspetto cruciale nella patogenesi del diabete di tipo 2. Per oltre due decenni, questa proteina è stata il bersaglio di specifiche classi di farmaci, tra cui spiccano i tiazolidinedioni, come il pioglitazone, ampiamente utilizzati nella pratica clinica per la gestione del diabete.
Anche la ricerca oncologica, nella sua incessante esplorazione di nuove strategie terapeutiche mirate per contrastare la crescita tumorale, ha rivolto la propria attenzione a questa molecola negli ultimi anni. Il PPARγ, in quanto fattore di trascrizione nucleare, esercita un’azione pleiotropica, intervenendo in processi biologici fondamentali quali la regolazione del metabolismo energetico, la modulazione delle risposte infiammatorie e il controllo della crescita e della proliferazione cellulare, agendo come un vero e proprio interruttore genico.
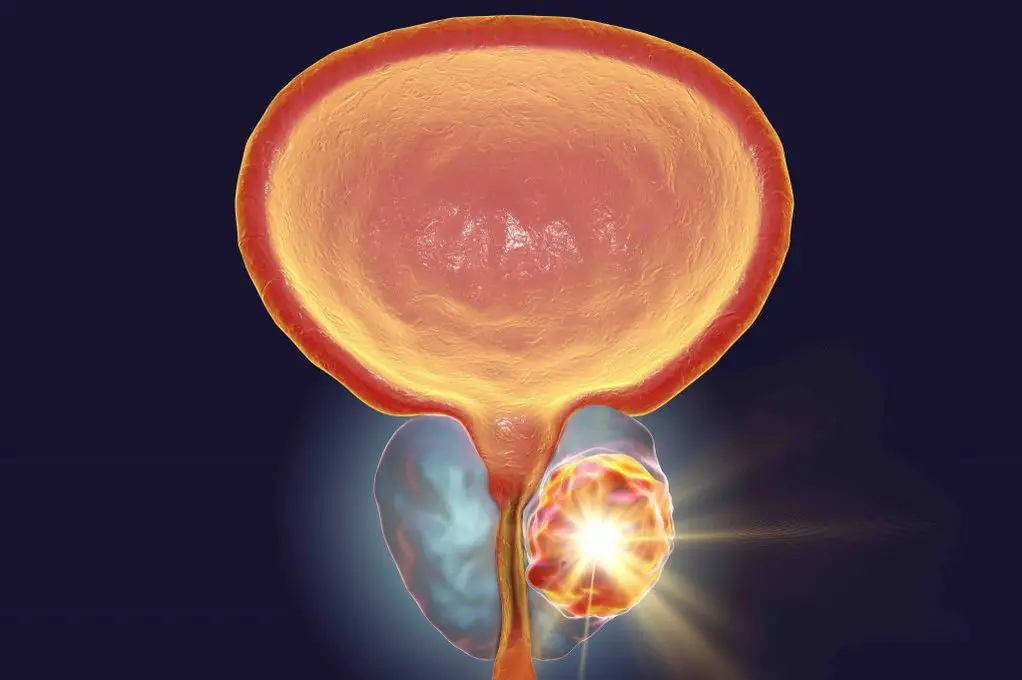
L’innovativo contributo del team di ricerca guidato dal professor Lukas Kenner, afferente al Dipartimento di Patologia Clinica presso l’Università di Medicina di Vienna, risiede nella dimostrazione inequivocabile del coinvolgimento del PPARγ anche nella dinamica di crescita del cancro alla prostata.
Questa scoperta stabilisce un legame molecolare diretto tra un regolatore metabolico chiave e un processo patologico di natura neoplastica, aprendo nuove e inaspettate vie per la comprensione e il trattamento di questa diffusa forma di tumore maschile. La capacità del PPARγ di influenzare sia il metabolismo che la proliferazione cellulare lo rende un bersaglio terapeutico di duplice interesse, potenzialmente in grado di agire sia sulle alterazioni metaboliche sottostanti che sulla crescita incontrollata delle cellule tumorali prostatiche.
Dalle colture cellulari ai dati clinici dei pazienti
I ricercatori hanno corroborato le loro innovative conclusioni attraverso un meticoloso esame condotto sia su colture cellulari in laboratorio che su campioni di tessuto biologico prelevati da specifiche coorti di pazienti affetti da cancro alla prostata. Questa duplice strategia di indagine, che spazia dall’analisi in vitro all’osservazione in vivo, ha permesso di delineare con precisione come i diversi stati di attivazione della proteina PPARγ esercitino la loro influenza a livello cellulare. Attraverso sofisticate tecniche di biologia molecolare e analisi istologiche, gli scienziati hanno potuto dissezionare i meccanismi attraverso i quali il PPARγ modula la crescita e il comportamento delle cellule tumorali prostatiche.
Un risultato particolarmente significativo emerso da questa approfondita indagine riguarda l’azione del pioglitazone, un farmaco ampiamente utilizzato nel trattamento del diabete mellito di tipo 2. “È stato dimostrato che il farmaco antidiabetico pioglitazone influenza l’attività del PPARγ e quindi inibisce la crescita e il metabolismo delle cellule tumorali”, spiega con chiarezza la prima autrice dello studio, Emine Atas, afferente al Dipartimento di Imaging Biomedico e Terapia Guidata dalle Immagini presso l’Università di Medicina di Vienna. Questa osservazione in vitro suggerisce un potenziale riposizionamento terapeutico del pioglitazone, aprendo la strada a nuove strategie di intervento farmacologico nel trattamento del cancro alla prostata.
Oltre alle promettenti evidenze ottenute in laboratorio, i ricercatori hanno riscontrato un dato clinico di notevole interesse analizzando le storie mediche dei pazienti. “Inoltre, i risultati iniziali hanno rivelato che i pazienti affetti da cancro alla prostata con diabete trattati con agonisti del PPARγ non avevano presentato recidive al momento della raccolta dei dati”, sottolinea Emine Atas. Questa osservazione preliminare, sebbene richieda ulteriori conferme su una casistica più ampia e con un follow-up più esteso, fornisce un indizio clinico concreto a sostegno dell’ipotesi che i farmaci in grado di modulare l’attività del PPARγ possano effettivamente esercitare un effetto protettivo contro la progressione del cancro.
Alla luce di questi risultati convergenti, che spaziano dalle evidenze molecolari in vitro alle promettenti osservazioni cliniche, il ricercatore principale Lukas Kenner esprime un cauto ma motivato ottimismo: “Ciò suggerisce che i farmaci che prendono di mira il PPARγ potrebbero rappresentare un nuovo approccio al trattamento del cancro alla prostata”.
La capacità di farmaci già in uso clinico per il trattamento del diabete di tipo 2 di interferire con la crescita tumorale prostatica e la potenziale associazione tra il loro utilizzo e una minore incidenza di recidive aprono scenari terapeutici innovativi e incoraggianti per la gestione di questa neoplasia maschile. Ulteriori ricerche saranno fondamentali per convalidare questi risultati preliminari e per esplorare appieno il potenziale terapeutico dei farmaci che modulano l’attività del PPARγ nel contesto del cancro.
L’impatto epidemiologico e la necessità di progressi terapeutici
Il cancro alla prostata si configura come una delle principali sfide sanitarie a livello globale, rappresentando la seconda neoplasia più frequentemente diagnosticata negli uomini in tutto il mondo. Nonostante gli straordinari progressi compiuti dalla medicina negli ultimi decenni nella comprensione e nel trattamento delle patologie oncologiche, questo specifico tipo di tumore continua a rappresentare una significativa causa di mortalità maschile. Basti pensare che, solo in Austria, il cancro alla prostata è ancora responsabile di un decesso maschile su otto correlato a una patologia neoplastica, evidenziando la persistente urgenza di sviluppare strategie terapeutiche più efficaci e mirate.
L’armamentario terapeutico attualmente disponibile per la gestione del cancro alla prostata comprende un ampio spettro di opzioni, che spaziano dagli interventi chirurgici volti all’asportazione della massa tumorale, alle tecniche di radioterapia per eradicare le cellule neoplastiche attraverso l’irradiazione, fino all’impiego di farmaci con diversi meccanismi d’azione.
La continua ricerca di nuove strategie terapeutiche è fondamentale per migliorare gli esiti clinici e la qualità di vita dei pazienti affetti da questa patologia. In questo contesto, l’identificazione e la comprensione di meccanismi molecolari precedentemente sconosciuti o sottovalutati rappresentano un passo cruciale per lo sviluppo di terapie sempre più selettive e personalizzate, in grado di colpire specificamente le cellule tumorali con maggiore efficacia e minori effetti collaterali.
In questo scenario di continua evoluzione della ricerca oncologica, la proteina PPARγ emerge come un potenziale regolatore chiave della crescita tumorale prostatica, aprendo prospettive terapeutiche di notevole interesse. La sua capacità di influenzare processi metabolici e proliferativi cellulari lo rende un bersaglio farmacologico promettente per lo sviluppo di nuove terapie mirate contro il cancro alla prostata. Le recenti scoperte scientifiche, che ne evidenziano il coinvolgimento nella biologia del tumore prostatico e la potenziale sensibilità a farmaci già utilizzati in ambito diabetologico, pongono le basi per ulteriori studi approfonditi.
Queste future indagini avranno l’obiettivo di elucidare compiutamente il ruolo del PPARγ nella patogenesi e nella progressione del cancro alla prostata, con la speranza di tradurre queste conoscenze in strategie terapeutiche innovative e più efficaci per contrastare questa diffusa e insidiosa malattia.
Lo studio è stato pubblicato su Molecular Cancer.