In quello che potrebbe rivelarsi un pezzo mancante nel puzzle del cancro al seno, i ricercatori della Harvard Medical School hanno identificato il fattore molecolare che causa la neoplasia.

I risultati della ricerca sono stati pubblicati sulla rivista scientifica Nature.
Cancro al seno qualche dettaglio sulla nuova ricerca
“Abbiamo identificato quello che crediamo sia l’innesco molecolare originale che avvia una cascata che culmina nello sviluppo del cancro al seno in un sottogruppo di tumori al seno che sono guidati dagli estrogeni”, ha detto il ricercatore senior dello studio Peter Park, professore di informatica biomedica presso l’Istituto Blavatnik presso HMS.

I ricercatori hanno affermato che fino a un terzo dei casi di cancro al seno può insorgere attraverso il meccanismo appena identificato. Lo studio mostra anche che l’ormone sessuale estrogeno è il colpevole di questa disfunzione molecolare perché altera direttamente il DNA di una cellula.
“Il nostro lavoro dimostra che gli estrogeni possono indurre direttamente riarrangiamenti genomici che portano al cancro, quindi il suo ruolo nello sviluppo del cancro al seno è sia quello di un catalizzatore che di una causa”, ha detto il primo autore dello studio Jake Lee, un ex ricercatore nel laboratorio del Parco che è ora borsista di oncologia medica presso il Memorial Sloan Kettering Cancer Center.
Molti tumori umani insorgono in questo modo durante la divisione cellulare, quando i cromosomi vengono riorganizzati e risvegliano i geni del cancro dormienti che possono innescare la crescita del tumore. Uno di questi scramble cromosomici può verificarsi quando un cromosoma si rompe e viene creata una seconda copia del cromosoma rotto prima che la rottura venga riparata.
Durante la successiva divisione cellulare, il cromosoma deforme viene allungato tra le due cellule figlie emergenti e il “ponte” cromosomico si rompe, lasciando dietro di sé frammenti frantumati che contengono i geni del cancro per moltiplicarsi e attivarsi.
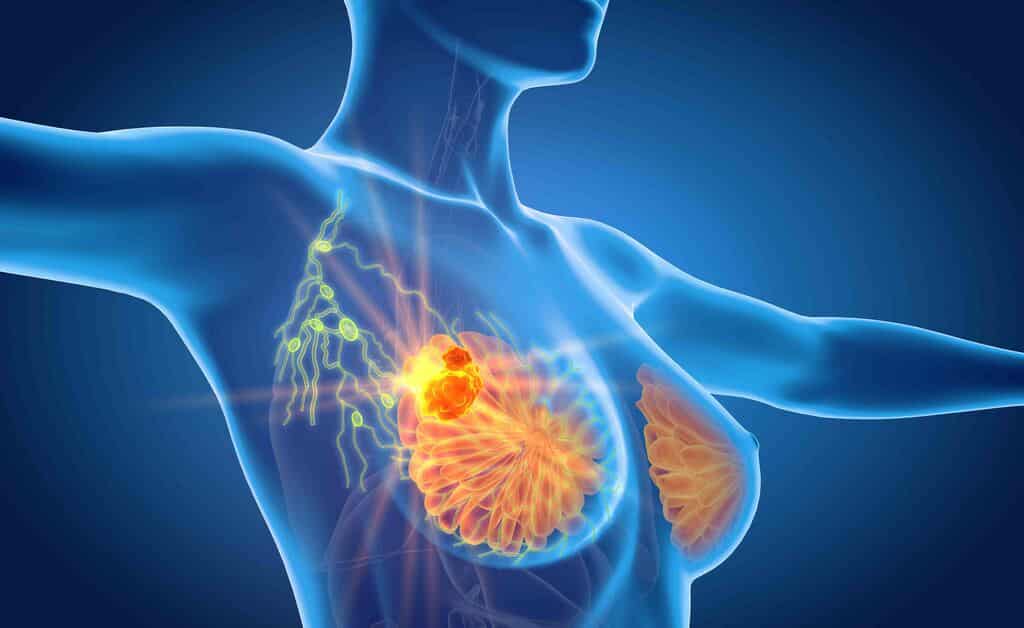
Questi erano i casi “freddi” che hanno incuriosito gli autori dello studio Park e Lee. Alla ricerca di risposte, hanno analizzato i genomi di 780 tumori al seno ottenuti da pazienti con diagnosi della malattia. Si aspettavano di trovare il classico disordine cromosomico nella maggior parte dei campioni tumorali, ma molte delle cellule tumorali non recavano traccia di questo classico schema molecolare.
Invece del classico cromosoma singolo deformato e rattoppato in modo improprio, hanno visto che due cromosomi si erano fusi, sospettosamente vicino a “punti caldi” dove si trovano i geni del cancro.
Proprio come nel modello di McClintock, questi cromosomi riorganizzati avevano formato dei ponti, tranne che in questo caso il ponte conteneva due cromosomi diversi. Questo modello distintivo era presente in un terzo (244) dei tumori nella loro analisi.
Lee e Park si sono resi conto di essersi imbattuti in un nuovo meccanismo mediante il quale un cromosoma “sfigurato” viene generato e poi fratturato per alimentare i misteriosi casi di cancro al seno.
Quando i ricercatori hanno ingrandito i punti caldi dell’attivazione del gene del cancro, hanno notato che queste aree erano curiosamente vicine alle aree di legame degli estrogeni sul DNA.
È noto che i recettori degli estrogeni si legano a determinate regioni del genoma quando una cellula viene stimolata dagli estrogeni. I ricercatori hanno scoperto che questi siti di legame degli estrogeni erano spesso vicini alle zone in cui si verificavano le prime rotture del DNA.
Ciò ha offerto un forte indizio che gli estrogeni potrebbero essere in qualche modo coinvolti nel rimescolamento genomico che ha dato origine all’attivazione del gene del cancro.
Lee e Park hanno seguito quell’indizio conducendo esperimenti con cellule di cancro al seno in un piatto. Hanno esposto le cellule agli estrogeni e poi hanno usato l’editing genico CRISPR per tagliare il DNA delle cellule.
Quando le cellule hanno riparato il loro DNA rotto, hanno avviato una catena di riparazione che ha portato allo stesso riarrangiamento genomico che Lee e Park avevano scoperto nelle loro analisi genomiche.
È già noto che gli estrogeni alimentano la crescita del cancro al seno promuovendo la proliferazione delle cellule del seno. Tuttavia, le nuove osservazioni gettano questo ormone sotto una luce diversa. La ricerca ha evidenziato che l’estrogeno è un personaggio più centrale nella genesi del cancro perché altera direttamente il modo in cui le cellule riparano il loro DNA.
I risultati suggeriscono che i farmaci che sopprimono gli estrogeni come il tamoxifene, spesso somministrati a pazienti con cancro al seno per prevenire la recidiva della malattia, agiscono in modo più diretto rispetto alla semplice riduzione della proliferazione delle cellule del seno.
Lo studio potrebbe portare a un miglioramento dei test sul cancro al seno . Ad esempio, rilevare l’impronta genomica del riarrangiamento cromosomico potrebbe allertare gli oncologi che la malattia di un paziente sta tornando, ha detto Lee.
In Italia, secondo il Ministero della Salute: “I numeri del cancro in Italia 2022 confermano che il carcinoma mammario è la neoplasia più diagnosticata nelle donne, in cui circa un tumore maligno ogni tre (30%) è un tumore mammario (I numeri del cancro in Italia 2020).
Il report 2022 stima in Italia per l’anno 2022 circa 55.700 nuove diagnosi di tumore nelle donne, con un incremento dello 0,5% rispetto al 2020.
La mortalità per il 2021 è stimata in 12.500 decessi. La sopravvivenza netta a 5 anni dalla diagnosi è stimata dal report dell’88%. La probabilità di vivere ulteriori 4 anni, condizionata ad aver superato il primo anno dopo la diagnosi, è indicata nel 91%.
Secondo i dati ISTAT nel 2018 il carcinoma mammario ha rappresentato, con 13.076 decessi, la prima causa di morte per tumore nelle donne.

Dalla fine degli anni novanta si osserva una continua tendenza alla diminuzione della mortalità per carcinoma mammario (-0,8%/anno), attribuibile a una maggiore diffusione dei programmi di diagnosi precoce (quindi all’anticipazione diagnostica) e anche ai progressi terapeutici”.