Indipendentemente dalle abitudini alimentari quotidiane, il pancreas opera instancabilmente come un fulcro biologico essenziale. Questo organo vitale è deputato non solo alla produzione di enzimi digestivi cruciali, ma anche alla sintesi di ormoni fondamentali per la regolazione del metabolismo. Ciononostante, quando anomalie patologiche, quali il cancro al pancreas, affliggono questa ghiandola, le ripercussioni possono rivelarsi estremamente gravi e sovente manifestarsi in maniera insidiosa.
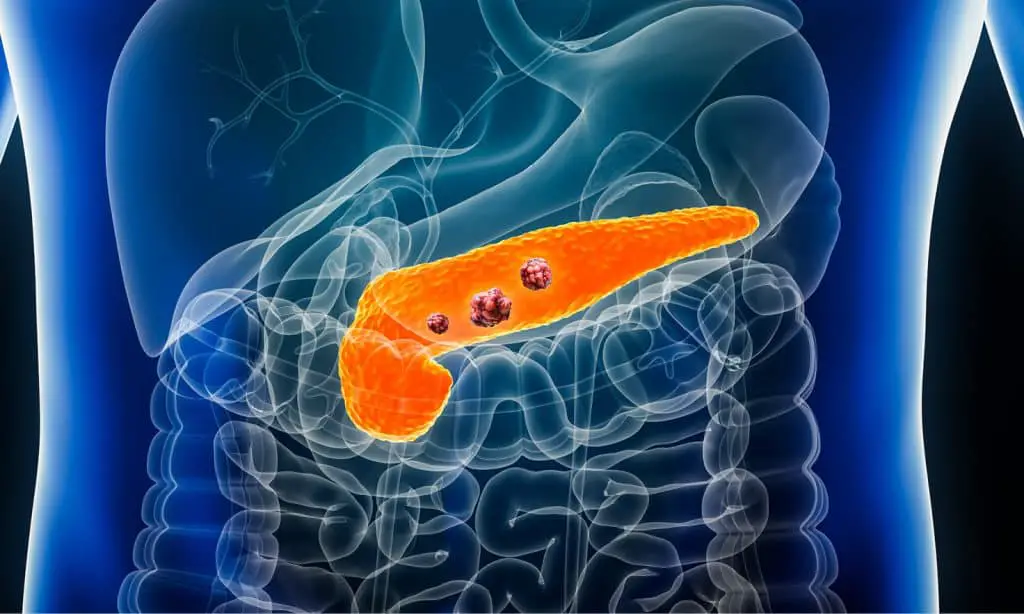
Cancro al pancreas: la nuova speranza arriva dall’intestino
Il cancro al pancreas si è tristemente guadagnato il soprannome di “killer silenzioso” con una ragione ben precisa. La maggior parte dei pazienti manifesta i sintomi solo quando la malattia ha già raggiunto uno stadio avanzato, limitando drasticamente le opzioni terapeutiche. Nel solo Regno Unito, tra il 2017 e il 2019, sono stati registrati oltre 10.700 nuovi casi e 9.500 decessi per cancro al pancreas, con tassi di incidenza in preoccupante aumento.
La forma più comune, l’adenocarcinoma duttale pancreatico (PDAC), si sviluppa nel dotto pancreatico, un condotto cruciale che collega il pancreas all’intestino tenue. Quando i tumori si formano in questa sede, possono bloccare il flusso degli enzimi digestivi, causando gravi problemi al metabolismo energetico. I pazienti spesso si sentono cronicamente stanchi e indisposti, ma questi sintomi sono purtroppo così subdoli che vengono facilmente ignorati o attribuiti ad altre condizioni meno gravi.
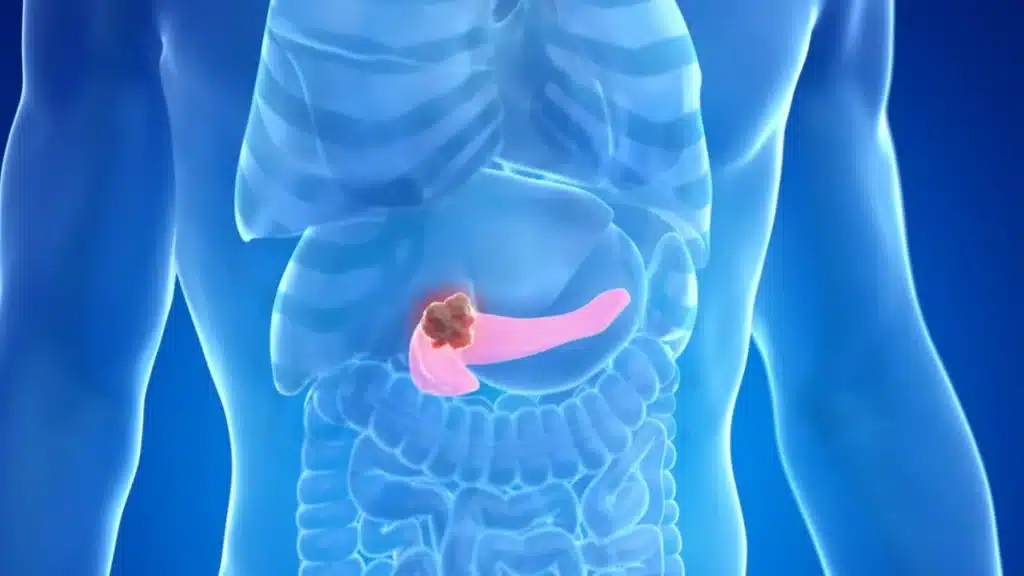
Ora, i ricercatori stanno rivolgendo la loro attenzione a una fonte inaspettata per la diagnosi precoce del PDAC: i campioni fecali. Sebbene l’analisi delle feci possa sembrare un approccio insolito per la diagnosi del cancro, gli scienziati stanno scoprendo che i nostri rifiuti biologici contengono una miniera di informazioni preziose sulla nostra salute.
Questo è dovuto al fatto che il nostro intestino ospita trilioni di batteri: le cellule batteriche nel tuo corpo superano in numero quelle umane di circa 40 a 30 trilioni. Questi microscopici abitanti formano comunità complesse che fungono da specchio del nostro stato di salute, inclusa la presenza di malattie. Poiché il PDAC si sviluppa tipicamente nella parte del pancreas connessa all’intestino e la maggior parte delle persone ha evacuazioni intestinali regolari, i campioni di feci offrono una finestra pratica e non invasiva su ciò che accade all’interno del corpo. Questo approccio innovativo potrebbe rivoluzionare la diagnosi del cancro al pancreas, permettendo un’individuazione molto più precoce e, di conseguenza, trattamenti più efficaci.
Decifrare il codice batterico: Il ruolo del sequenziamento del 16S rRNA
L’approccio innovativo che lega la salute dell’intestino alla diagnosi precoce del cancro al pancreas è stato convalidato da studi condotti in diverse nazioni, tra cui Giappone, Cina e Spagna. L’ultima e significativa svolta in questa direzione giunge da uno studio internazionale del 2025, frutto della collaborazione tra ricercatori in Finlandia e Iran. L’obiettivo primario di questa ricerca era esaminare la relazione tra la flora batterica intestinale e l’insorgenza del cancro al pancreas in diverse popolazioni, consolidando ulteriormente la rilevanza di questo campo di indagine.
Per condurre lo studio, i ricercatori hanno raccolto campioni di feci e hanno analizzato il DNA batterico utilizzando una tecnica chiamata sequenziamento dell’amplicone del gene 16S rRNA. Nonostante la complessità del nome, il principio alla base di questa metodologia è relativamente semplice: gli scienziati sequenziano e confrontano una specifica regione genetica presente nel genoma di ogni batterio. Questo permette loro di identificare e quantificare simultaneamente le diverse specie batteriche presenti nel campione, fornendo un’istantanea della composizione del microbioma intestinale.
I risultati di questo studio finlandese-iraniano sono stati a dir poco sorprendenti. I pazienti affetti da adenocarcinoma duttale pancreatico (PDAC) mostravano una ridotta diversità batterica intestinale, con alcune specie batteriche più abbondanti o meno presenti rispetto agli individui sani. Ancora più significativo è stato lo sviluppo da parte del team di un modello di intelligenza artificiale. Questo modello si è dimostrato capace di distinguere con elevata precisione tra pazienti oncologici e persone sane, basandosi esclusivamente sui loro profili batterici intestinali. Questa capacità diagnostica, derivata unicamente dall’analisi del microbioma, rappresenta un enorme passo avanti.
Il campo della ricerca sul microbioma sta vivendo una fase di rapida evoluzione. Sebbene lo studio qui menzionato abbia impiegato il sequenziamento di ampliconi, metodi più recenti e avanzati, come il “sequenziamento metagenomico shotgun”, stanno fornendo informazioni ancora più dettagliate e complete. Questa tecnica all’avanguardia cattura l’intero contenuto del genoma batterico, anziché focalizzarsi su un singolo gene. Ciò offre una risoluzione senza precedenti, che può persino rilevare se i batteri si sono recentemente trasferiti da un individuo all’altro, aprendo scenari impensabili fino a poco tempo fa.
Questi progressi tecnologici stanno innescando un cambiamento fondamentale nel nostro modo di concepire la salute e la malattia. Stiamo abbandonando una visione puramente antropocentrica per abbracciare una comprensione di noi stessi come “essere umano più microbioma”. Siamo, in realtà, ecosistemi complessi in cui i nostri partner batterici svolgono ruoli cruciali per il nostro benessere generale, influenzando non solo la digestione, ma potenzialmente anche la suscettibilità e la diagnosi di patologie gravi come il cancro.
Oltre il cancro al pancreas: Il microbioma rivoluziona la diagnosi e la ricerca
Le potenzialità dei batteri intestinali nella diagnosi precoce delle patologie si estendono ben oltre il cancro al pancreas. Al Quadram Institute, per esempio, i ricercatori stanno applicando metodologie simili per studiare il cancro del colon-retto. Hanno già analizzato oltre un migliaio di campioni fecali, impiegando sofisticati strumenti computazionali capaci di ricostruire genomi batterici e le loro funzioni a partire da DNA frammentato. Questo lavoro, ancora in corso, mira a svelare il comportamento specifico dei microbi intestinali in relazione al cancro del colon-retto, replicando il successo ottenuto da altri scienziati per l’adenocarcinoma duttale pancreatico (PDAC).
Le interazioni bidirezionali tra cancro e batteri sono un campo di studio particolarmente affascinante e complesso. Non solo specifici profili batterici possono indicare la presenza di una malattia, ma la malattia stessa può alterare la composizione del microbioma intestinale. Questa dinamica è stata precedentemente dimostrata nel contesto del morbo di Parkinson, evidenziando una complessa rete di causa ed effetto che i ricercatori stanno ancora cercando di decifrare.
Comprendere come i nostri “partner microbici” rispondono e influenzano le malattie ci sta fornendo intuizioni che potrebbero rivoluzionare sia la diagnosi che il trattamento. Sebbene le ricerche passate abbiano mostrato la complessità e la difficoltà di comprendere a fondo queste interazioni, i recenti sviluppi nella biotecnologia e nell’intelligenza artificiale stanno progressivamente aiutando gli scienziati a dare un senso a questo mondo microscopico.
Per i malati di cancro e le loro famiglie, questi progressi e altri sviluppi nella ricerca sul microbioma offrono una concreta speranza per una diagnosi precoce. Sebbene la traduzione di questi risultati nella pratica clinica sia ancora nelle fasi iniziali, la possibilità di individuare “il killer silenzioso” prima che diventi letale potrebbe trasformare radicalmente la prognosi per migliaia di pazienti. Tuttavia, ciò richiederà ulteriori ricerche attente e approfondite per garantire l’affidabilità e la scalabilità di queste metodologie.
La prospettiva microbica sulla salute non è più una remota curiosità scientifica; sta rapidamente diventando una realtà pratica con il potenziale di salvare vite umane. Mentre i ricercatori continuano a esplorare questa frontiera interna, stiamo scoprendo che la risposta ad alcuni dei nostri quesiti medici più complessi potrebbe essere nascosta in piena vista: nei rifiuti che scarichiamo ogni giorno.
Lo studio che ha aperto queste nuove prospettive è stato pubblicato su Gut Pathogens.