In una nuova ricerca sono state utilizzate le le cellule staminali dei pazienti e la biostampa 3D per produrre tessuto oculare che farà progredire la comprensione dei meccanismi delle malattie che causano la perdita della vista.
Il team di ricerca del National Eye Institute (NEI), parte del National Institutes of Health, ha stampato una combinazione di cellule che formano la barriera emato-retinica esterna, il tessuto oculare che supporta i fotorecettori sensibili alla luce della retina. La tecnica fornisce una fornitura teoricamente illimitata di tessuto derivato dal paziente per studiare le malattie degenerative della retina come la degenerazione maculare legata all’età (AMD).
I risultati dello studio sono stati pubblicati sulla rivista scientifica Nature Methods.
Biostampa 3D: ecco come ha creato il tessuto oculare
“Sappiamo che l’AMD inizia nella barriera emato-retinica esterna“, ha affermato Kapil Bharti, Ph.D., che dirige la sezione NEI sulla ricerca traslazionale sulle cellule staminali e oculari. “Tuttavia, i meccanismi dell’inizio e della progressione dell’AMD verso stadi asciutti e umidi avanzati rimangono poco conosciuti a causa della mancanza di modelli umani fisiologicamente rilevanti“.
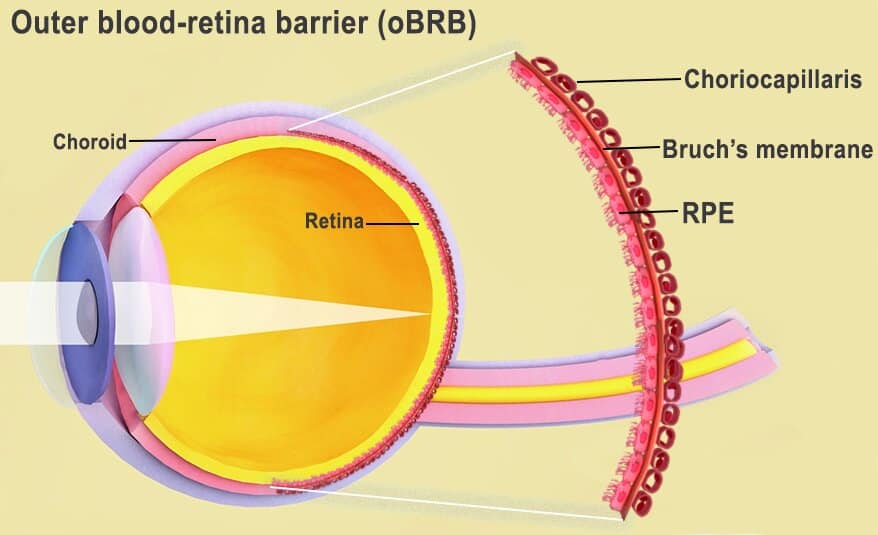
La barriera emato-retinica esterna è costituita dall’epitelio pigmentato retinico (RPE), separato dalla membrana di Bruch dal coriocapillare ricco di vasi sanguigni. La membrana di Bruch regola lo scambio di nutrienti e rifiuti tra il coriocapillare e l’RPE. Nell’AMD, depositi di lipoproteine chiamate drusen si formano all’esterno della membrana di Bruch, impedendone la funzione. Nel tempo, l’RPE si rompe portando alla degenerazione dei fotorecettori e alla perdita della vista.
Bharti e colleghi hanno combinato tre tipi di cellule coroideali immature in un idrogel: periciti e cellule endoteliali , che sono componenti chiave dei capillari; e fibroblasti, che danno struttura ai tessuti. Gli scienziati hanno quindi con la biostampa 3D hanno sviluppato il gel su un’impalcatura biodegradabile. In pochi giorni, le cellule hanno iniziato a maturare in una fitta rete capillare.
Il nono giorno, gli scienziati hanno seminato cellule epiteliali del pigmento retinico sul rovescio dell’impalcatura. Il tessuto ottenuto da biostampa 3D ha raggiunto la piena maturità il giorno 42. Le analisi del tessuto e i test genetici e funzionali hanno mostrato che il tessuto stampato aveva un aspetto e un comportamento simile alla barriera emato-retinica esterna nativa.
Sotto stress indotto, il tessuto ricavato da biostampa 3D ha mostrato modelli di AMD precoce come i depositi di drusen sotto l’RPE e la progressione verso lo stadio secco tardivo, dove è stata osservata la degradazione del tessuto. Aspetto simile all’AMD umida indotto da basso contenuto di ossigeno, con iperproliferazione dei vasi coroideali che sono migrati nella zona sub-RPE. I farmaci anti-VEGF, usati per trattare l’AMD, hanno soppresso la crescita eccessiva e la migrazione di questo vaso e ripristinato la morfologia dei tessuti.
“Stampando le cellule, stiamo facilitando lo scambio di segnali cellulari necessari per la normale anatomia della barriera emato-retinica esterna“, ha affermato Bharti. “Ad esempio, la presenza di cellule RPE induce cambiamenti nell’espressione genica nei fibroblasti che contribuiscono alla formazione della membrana di Bruch, qualcosa che è stato suggerito molti anni fa ma non è stato dimostrato fino al nostro modello“.
Tra le sfide tecniche che il team di Bharti ha affrontato stavano generando un’impalcatura biodegradabile adatta e ottenendo un modello di biostampa 3D coerente attraverso lo sviluppo di un idrogel sensibile alla temperatura che raggiungeva file distinte quando era freddo ma che si dissolveva quando il gel si riscaldava. Una buona consistenza delle righe ha consentito un sistema più preciso di quantificazione delle strutture tissutali. Hanno anche ottimizzato il rapporto di miscelazione cellulare di periciti, cellule endoteliali e fibroblasti.
Il coautore Marc Ferrer, Ph.D., direttore del 3D Tissue Bioprinting Laboratory presso il National Center for Advancing Translational Sciences del NIH, e il suo team hanno fornito competenze per la biofabbricazione dei tessuti della barriera emato-retinica esterna “in-a-well, ” insieme a misurazioni analitiche per consentire lo screening dei farmaci.
“I nostri sforzi di collaborazione hanno portato a modelli di tessuto retinico molto rilevanti di malattie degenerative degli occhi“, ha detto Ferrer. “Tali modelli di tessuto hanno molti potenziali usi nelle applicazioni traslazionali, incluso lo sviluppo terapeutico“.
Bharti e collaboratori stanno utilizzando modelli stampati di barriera emato-retinica per studiare l’AMD e stanno sperimentando l’aggiunta di ulteriori tipi di cellule al processo di stampa , come le cellule immunitarie, per ricapitolare meglio il tessuto nativo.