Una nuova ricerca sviluppata dalla professoressa Mara Mather della USC Leonard Davis School of Gerontology, ha rivelato un modo in cui gli adulti, giovani e meno giovani, possono ridurre i loro livelli di amiloide-beta: attraverso esercizi di respirazione che abbassano i livelli nel sangue di questi peptidi associati alla malattia di Alzheimer.
I risultati dello studio sono stati pubblicati sulla rivista scientifica Scientific Reports.
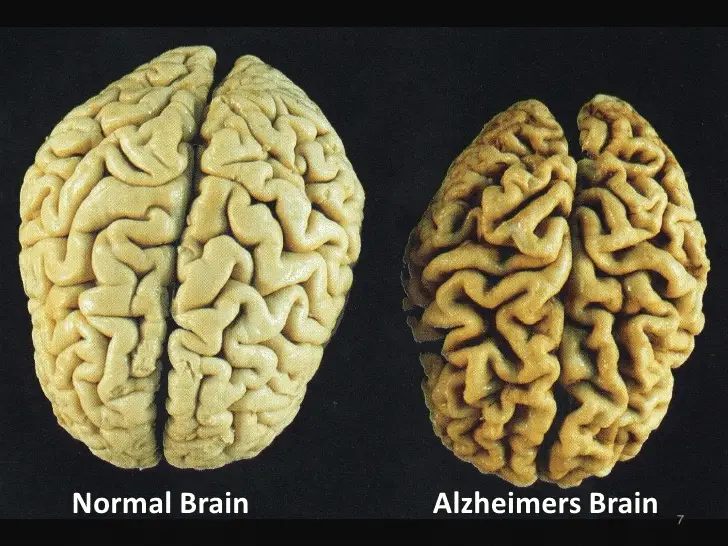
Alzheimer: ecco gli effetti degli esercizi di respirazione sulla salute cerebrale
L’esercizio era semplice: inspirare contando fino a cinque, poi espirare contando fino a cinque. Farlo per 20 minuti, due volte al giorno, per quattro settimane. Queste brevi sessioni di respirazione hanno avuto un impatto significativo: la variabilità della frequenza cardiaca dei volontari è aumentata durante ogni periodo di esercizio e i livelli di peptidi amiloide-beta circolanti nel loro sangue sono diminuiti durante le quattro settimane dell’esperimento.
Questo perché il modo in cui respiriamo influenza la nostra frequenza cardiaca, che a sua volta influenza il nostro sistema nervoso e il modo in cui il nostro cervello produce proteine e le elimina. Mentre siamo svegli e attivi, in genere utilizziamo il nostro sistema nervoso simpatico .
Questo è talvolta noto come il sistema “lotta o fuga”, ma lo usiamo anche per esercitare, focalizzare l’attenzione e persino per aiutare a creare ricordi duraturi. Mentre il sistema nervoso simpatico è attivato, non c’è molta variazione nel tempo tra ogni battito cardiaco. Al contrario, quando il sistema parasimpatico è attivato, la frequenza cardiaca aumenta durante l’inspirazione e diminuisce durante l’espirazione.
Quando siamo giovani, o più anziani, ma molto in forma, il nostro corpo scivola facilmente tra il sistema nervoso simpatico e il suo partner, il sistema nervoso parasimpatico. A volte noto come la parte “riposa e digerisci” del nostro sistema, il sistema nervoso parasimpatico ci consente di calmarci, digerire facilmente il cibo e dormire sonni tranquilli. Quando si verificano questi tipi di attività, la variazione tra i battiti cardiaci è maggiore.
Ma mentre invecchiamo, gli scienziati stanno imparando, la nostra capacità di accedere al nostro sistema nervoso parasimpatico e, quindi, la nostra variazione della frequenza cardiaca diminuisce drasticamente. Uno studio del 2020 che ha utilizzato orologi intelligenti ha rilevato che la variabilità della frequenza cardiaca diminuisce in media dell’80% tra i venti ei sessant’anni. Questa scoperta potrebbe in parte spiegare perché facciamo fatica a dormire profondamente mentre invecchiamo.
“Sappiamo che i sistemi simpatico e parasimpatico influenzano la produzione e l’eliminazione dei peptidi e delle proteine correlati all’Alzheimer”, ha affermato Mather, che dirige l’Emotion & Cognition Lab presso la Leonard Davis School of Gerontology. “Tuttavia, c’è stata pochissima ricerca su come questi cambiamenti fisiologici nell’invecchiamento potrebbero contribuire ai fattori che rendono favorevole lo sviluppo o meno dell’Alzheimer”.
Mather e colleghi ricercatori di USC, UC Irvine e UCLA hanno chiesto ai partecipanti di fare esercizi di biofeedback due volte al giorno, per 20 minuti alla volta. Tutti i partecipanti hanno agganciato un cardiofrequenzimetro all’orecchio; quel monitor era collegato a un laptop fornito dai ricercatori.
A metà del gruppo è stato chiesto di pensare a cose tranquille, come una scena sulla spiaggia o una passeggiata in un parco, o di ascoltare musica tranquilla. Nel frattempo, sono stati istruiti a tenere d’occhio la frequenza cardiaca visualizzata sullo schermo del laptop, assicurandosi che la linea della frequenza cardiaca rimanesse il più stabile possibile mentre meditavano.

All’altro gruppo è stato detto di regolare il ritmo della respirazione con un pacer sullo schermo del laptop: quando il quadrato si alzava, inspiravano e quando il quadrato scendeva, espiravano. Hanno anche monitorato le loro frequenze cardiache, che tendevano ad aumentare nei picchi mentre inspiravano e scendevano al basale mentre espiravano. Il loro obiettivo era aumentare le oscillazioni indotte dalla respirazione nella loro frequenza cardiaca.
I ricercatori hanno prelevato campioni di sangue prima che i partecipanti iniziassero l’esperimento e di nuovo, dopo quattro settimane di formazione sul biofeedback. Quindi i ricercatori hanno esaminato il plasma dei partecipanti di entrambi i gruppi, alla ricerca di peptidi beta amiloidi. In particolare, i ricercatori hanno esaminato due peptidi, l’amiloide beta 40 e 42.
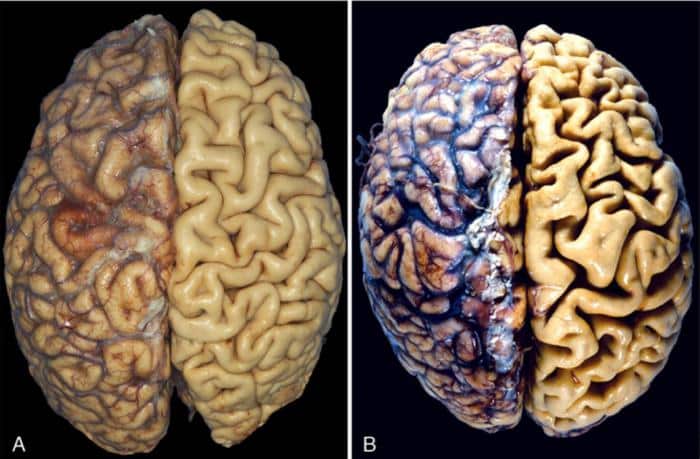
Si ritiene che l’accumulo di amiloide-beta nel cervello dovuto all’aumento della produzione e/o alla diminuzione della clearance inneschi il processo della malattia di Alzheimer. Negli adulti sani che non hanno ancora segni di accumulo di amiloide nel cervello, una meta-analisi mostra che livelli più alti di amiloide-beta 40 e 42 nel sangue circolante predice un maggior rischio di sviluppare l’Alzheimer.
Nello studio di Mather e colleghi, i livelli plasmatici di entrambi i peptidi sono diminuiti nel gruppo che respirava lentamente e cercava di aumentare la variabilità della frequenza cardiaca (HRV) aumentando le oscillazioni.
Ora i ricercatori vogliono capire perché i peptidi diminuiscono quando aumenta l’HRV, ha detto Jungwon Min, uno studente laureato in psicologia e autore principale dello studio. È perché vengono prodotti meno peptidi? O perché il corpo li elimina meglio? O una combinazione di entrambi? Lo studio attuale fornisce alcuni suggerimenti.
“Sulla base dei dati che abbiamo, sembra che la diminuzione della beta-amiloide sia dovuta più alla diminuzione della produzione”, ha detto. “Ma ciò non esclude la possibilità di una maggiore autorizzazione.”
Dei 108 partecipanti allo studio, metà erano giovani (dai 18 ai 30 anni) e metà erano anziani (dai 55 agli 80 anni). Gli adulti più giovani e più anziani hanno mostrato effetti simili degli interventi sui livelli plasmatici di amiloide-beta.
Lo studio sembra essere il primo a scoprire che gli interventi comportamentali possono ridurre il livello di peptidi beta-amiloide nel plasma. Precedenti ricerche hanno dimostrato che la privazione del sonno e lo stress possono aumentare i livelli di amiloide-beta, ma si è rivelato più difficile diminuire l’amiloide- beta con interventi comportamentali.
“Almeno fino ad oggi, gli interventi di esercizio fisico non hanno ridotto i livelli di Aβ [ beta amiloide ]”, ha affermato Mather. “Praticare regolarmente la respirazione a ritmo lento tramite il biofeedback dell’HRV può essere un modo economico e a basso rischio per ridurre i livelli plasmatici di Aβ e mantenerli bassi per tutta l’età adulta”.
Altri coautori dello studio sono stati Kaoru Nashiro, Hyun Joo Yoo, Shai Porat, Christine Cho e Junxiang Wan, della USC; Jeremy Rouanet, Allesandra Cadete Martini, Elizabeth Head, Daniel A. Nation e Julian F. Thayer, della UC Irvine; e Steve W. Cole dell’UCLA.
Per quanto invece riguarda la ricerca sul nuovo anticorpo monoclonale, secondo Silvia De Francia, professoressa di farmacologia all’università di Torino e divulgatrice scientifica sui temi della medicina e della farmacologia genere-specifica, i trial condotti su lecanemab mostrerebbero qualche carenza nell’interpretazione dei dati disaggregati per sesso.
“Il lecanemab è un anticorpo monoclonale e quindi come tale va a stimolare il sistema immunitario – ha spiegato la professoressa De Francia –: induce l’organismo a ridurre i livelli di protofibrille di beta-amiloide che è una delle proteine tossiche per il cervello, per i neuroni, recentemente identificata come uno dei marker di progressione di demenza di Alzheimer”.
“Nelle persone con malattia di Alzheimer precoce- si legge nella ricerca- lecanemab ha ridotto i livelli di amiloide cerebrale ed è stato associato a un declino moderatamente inferiore nelle misure cliniche della cognizione e della funzione rispetto al placebo a 18 mesi, ma è stato associato a eventi avversi. Sono necessari studi più lunghi per determinare l’efficacia e la sicurezza di lecanemab nella malattia di Alzheimer precoce”.
“Si è visto che lecanemab era in grado non tanto di curare la malattia – ha specificato Silvia De Francia –, quanto di rallentare l’avanzamento del declino cognitivo, la progressione della malattia, ma in modo non clinicamente significativo al momento. Il farmaco però ha anche degli effetti collaterali e una tossicità assolutamente non trascurabili, quali ad esempio accumulo di liquidi a livello cerebrale, emorragia cerebrale, edema”.
L’arruolamento c’è stato, anche perché si tratta di una patologia molto più frequente nel sesso femminile, quindi è molto più facile trovare donne con una diagnosi precoce di Alzheimer, che decidono di partecipare a uno studio di sperimentazione clinica.
In realtà però, a mio avviso, l’interpretazione dei dati disaggregati per sesso e per genere è ancora un po’ carente: nello studio (il trial clinico di fase 3, ndr) il 50% della popolazione arruolata è di sesso femminile, ma da ciò cosa si desume? Che cosa cambia negli uomini e nelle donne in termini di tossicità, in seguito alla somministrazione del farmaco?
Tali informazioni sono ancora un po’ carenti, ed è questa la cifra che ha accompagnato negli anni, e ancora oggi accompagna purtroppo, la sperimentazione clinica. Anche quelle più illuminate, che arrivano ad arruolare una buona parte di popolazione di sesso femminile, in realtà sono un po’ deficitarie nella interpretazione dei dati in modo sesso e genere specifico”.
“Bisogna riscrivere le linee guida per il trattamento della patologia che sappiamo essere molto più frequente nelle donne: su una popolazione considerata, due terzi dei pazienti affetti da demenza di Alzheimer sono di sesso femminile, e questo per diversi motivi che vanno dall’accezione biologica al costrutto del genere.
Innanzitutto, le donne hanno una maggior predisposizione allo sviluppo del declino cognitivo, perché per un certo periodo della loro vita sono protette dagli estrogeni, ma poi vanno incontro alla menopausa che spesso può anche essere precoce”.
E vanno considerati anche altri aspetti, come il numero di gravidanze, i livelli di pressione arteriosa. “Dal punto di vista biologico, c’è una maggior frequenza di una determinata mutazione su un gene detto ApoE, l’allele 4 muta più frequentemente nelle donne e quindi la popolazione femminile è più esposta allo sviluppo della malattia”.
In generale a livello mondiale le donne fanno mediamente un lavoro meno stimolante, hanno un livello di istruzione decisamente inferiore, e quindi per questo motivo sono meno abituate all’esercizio mentale e più esposte nel mondo ovviamente a una patologia di questo tipo.
La ricerca farmacologica negli ultimi anni non ha tenuto in debita considerazione tutte queste differenze che tracciano due organismi profondamente diversi in termini di aspettativa di vita, di anni che si trascorrono in disabilità e in termini di risposta al trattamento farmacologico impostato ad esempio per una donna o per un uomo che a 60-65 anni comincino a dimostrare i primi segni e sintomi di malattia”.
“Negli ultimi anni è possibile diagnosticare l’Alzheimer quando la persona è ancora in vita, poiché esistono dei marcatori che indicano la presenza della malattia e hanno un valore predittivo. La ricerca scientifica ha fatto molti passi avanti, dunque, ma non ancora purtroppo in ottica sesso e genere specifiche. E questo – ha concluso Silvia De Francia – dovrà essere l’obiettivo del futuro”.
Il Prof. Paolo Maria Rossini, Direttore del Dipartimento Neuroscienze e Neuroriabilitazione dell’IRCCS San Raffaele, sempre a proposito del Lecanemab, ha dichiarato: “Rispetto a tre anni fa insieme rappresentano due armi in più all’interno di un armamentario desolante”.
“Fino ad oggi avevamo solamente farmaci sintomatici, capaci cioè di ridurre i sintomi della malattia, dall’agitazione al disorientamento, senza però interferire con la malattia sottostante. Questi invece sono i primi che modificano la curva di peggioramento naturale della malattia. Su una persona di 70 anni con una malattia progressiva che toglie l’autonomia come l’Alzheimer, lecanemab potrebbe ridurre il costo personale e sociale della sua gestione e garantire una buona qualità di vita per un periodo di tempo più lungo”.