Una squadra di ricercatori delle università di Kaunas, in Lituania, hanno sviluppato un algoritmo basato sull’apprendimento profondo in grado di prevedere la possibile insorgenza della malattia di Alzheimer dalle immagini del cervello con una precisione superiore al 99%. Il metodo è stato sviluppato durante l’analisi di immagini MRI funzionali ottenute da 138 soggetti e ha ottenuto risultati migliori in termini di accuratezza, sensibilità e specificità rispetto ai metodi tradizionali.

La ricerca è stata pubblicata sulla rivista scientifica Diagnostica.
Algoritmo prevede Alzheimer: ecco cosa dice la ricerca
Secondo l’Organizzazione Mondiale della Sanità, il morbo di Alzheimer è la causa più frequente di demenza, contribuendo fino al 70% dei casi di demenza in totale. Nel mondo ne sono colpite circa 24 milioni di individui e si prevede che questo numero raddoppierà ogni 20 anni. A causa dell’invecchiamento della società, la malattia diventerà un onere in termini economici per il sistema sanitario pubblico.
“I professionisti medici di tutto il mondo cercano di aumentare la consapevolezza di una diagnosi precoce di Alzheimer, che offre alle persone colpite una migliore possibilità di beneficiare del trattamento. Questa è stata una delle questioni più importanti per la scelta di un argomento per Modupe Odusami, un dottorato di ricerca studente dalla Nigeria”, afferma Rytis Maskeliūnas, ricercatore presso il Dipartimento di Ingegneria Multimediale, Facoltà di Informatica, Kaunas University of Technology (KTU), Ph.D. di Odusami, supervisore.
Uno dei possibili primi segni di Alzheimer è il detoriamento cognitivo breve (MCI), che è lo stadio tra il previsto declino cognitivo del normale invecchiamento e la demenza. Sulla base di una ricerca precedente, la risonanza magnetica funzionale (fMRI) può essere sfruttata per individuare le regioni del cervello che possono essere associate all’insorgenza della malattia di Alzheimer, secondo Maskeliūnas. Le prime fasi dell’MCI spesso non hanno sintomi chiari, ma in alcuni casi possono essere rilevate dal neuroimaging.
Questo procedimento in linea teorica è possibile ma l’analisi manuale delle immagini fMRI che tentano di identificare i cambiamenti associati all’Alzheimer non solo richiede conoscenze specifiche, ma richiede anche molto tempo: l’applicazione del Deep learning e di altri metodi di intelligenza artificiale può accelerare questo con un significativo margine di tempo. Trovare le caratteristiche dell’MCI non significa necessariamente la presenza di una malattia, in quanto può anche essere un sintomo di altre malattie correlate, ma è più un indicatore e un possibile aiuto per orientarsi verso una valutazione da parte di un medico.
“La moderna elaborazione del segnale consente di delegare l’elaborazione delle immagini alla macchina, che può completarla in modo abbastanza veloce e accurato. Naturalmente, non osiamo suggerire che un professionista medico dovrebbe mai fare affidamento su un algoritmo al cento per cento. Pensa a una macchina come un robot in grado di svolgere il compito più noioso di ordinare i dati e ricercare le caratteristiche.In questo scenario, dopo che l’algoritmo del computer ha selezionato i casi potenzialmente interessati, lo specialista può esaminarli più da vicino e alla fine tutti ne beneficiano poiché la diagnosi e il trattamento raggiungono il paziente molto più velocemente”, afferma Maskeliūnas, che ha supervisionato il team che lavorava sul modello.
Il modello basato sul deep learning è stato sviluppato come una proficua collaborazione dei principali ricercatori lituani nel settore dell’intelligenza artificiale, utilizzando una modifica della ben nota ResNet 18 (rete neurale residua) per classificare le immagini MRI funzionali ottenute da 138 soggetti. Le immagini rientravano in sei diverse categorie: dal sano allo spettro del deterioramento cognitivo lieve (MCI) al morbo di Alzheimer. In totale, sono state selezionate 51.443 e 27.310 immagini dal set di dati fMRI dell’Alzheimer’s Disease Neuroimaging Initiative per la formazione e la convalida.
Il modello è stato in grado di trovare efficacemente le caratteristiche dell’MCI nel dato set di dati, ottenendo la migliore precisione di classificazione del 99,99%, 99,95% e 99,95% per MCI precoce rispetto a AD, MCI tardivo rispetto a AD e MCI rispetto a MCI precoce, rispettivamente.
“Anche se questo non è stato il primo tentativo di diagnosticare l’insorgenza precoce dell’Alzheimer da dati simili, la nostra scoperta principale è l’accuratezza dell’algoritmo. Ovviamente, numeri così alti non sono indicatori di prestazioni reali nella vita reale, ma stiamo lavorando con istituzioni mediche per ottenere più dati”, afferma Maskeliūnas.
Secondo lo studioso, l’algoritmo potrebbe essere sviluppato in un software, che analizzerebbe i dati raccolti dai gruppu vulnerabilu (quelli di età superiore ai 65 anni, con una storia di lesioni cerebrali, ipertensione, ecc.) e notificherebbe al personale medico le anomalie relative alla l’esordio precoce dell’Alzheimer.
“Dobbiamo sfruttare al massimo i dati”, afferma Maskeliūnas, “Ecco perché il nostro gruppo di ricerca si concentra sul principio europeo della scienza aperta, in modo che chiunque possa utilizzare le nostre conoscenze e svilupparle ulteriormente. Credo che questo principio contribuisca notevolmente al progresso della società”.
Il capo ricercatore, la cui area principale è focalizzata sull’applicazione dei moderni metodi di intelligenza artificiale sull’elaborazione del segnale e sulle interfacce multimodali, afferma che il modello sopra descritto può essere integrato in un sistema più complesso, analizzando diversi parametri, ad esempio, anche monitoraggio del tracciamento dei movimenti oculari, lettura del viso, analisi della voce, ecc. Tale tecnologia potrebbe quindi essere utilizzata per l’autocontrollo e l’avviso per chiedere una consulenza professionale se qualcosa causa preoccupazione.
“Le tecnologie possono rendere la medicina più accessibile ed economica. Sebbene non sostituiranno mai (o almeno non presto) veramente il medico, le tecnologie possono incoraggiare la ricerca di diagnosi e aiuto tempestivi“, afferma Maskeliūnas.
Algoritmo prevede Alzheimer: l’intelligenza artificiale si basa anche sulla fMRI
La risonanza magnetica funzionale (fMRI) è una tecnica diagnostica non invasiva per i disturbi cerebrali. Misura i minimi cambiamenti nei livelli di ossigeno nel sangue all’interno del cervello nel tempo, fornendo informazioni sull’attività locale dei neuroni. Nonostante i suoi vantaggi, la fMRI non è stata ampiamente utilizzata nella diagnosi clinica. Il motivo è duplice. Innanzitutto, i cambiamenti nei segnali fMRI sono così piccoli da essere eccessivamente suscettibili al rumore, che può annullare i risultati. In secondo luogo, i dati fMRI sono complessi da analizzare. È qui che entrano in gioco gli algoritmi di deep learning.
Lo studio è stato pubblicato sulla rivista scientifica Journal of Medical Imaging.
Per poter portare avanti la loro ricerca, gli scienziati della Texas Tech University hanno utilizzato un algoritmo di apprendimento automatico per classificare i dati fMRI. Gli studiosi hanno sviluppato un tipo di algoritmo di apprendimento profondo noto come rete neurale convoluzionale (CNN) in grado di differenziare i segnali fMRI di persone sane, persone con decadimento cognitivo lieve e persone con AD.
Le CNN possono estrarre autonomamente caratteristiche dai dati di input che sono nascosti agli osservatori umani. Ottengono queste caratteristiche attraverso l’addestramento, per il quale è necessaria una grande quantità di dati preclassificati. Le CNN sono utilizzate principalmente per la classificazione delle immagini 2-D, il che significa che i dati fMRI quadridimensionali (tre spaziali e uno temporale) rappresentano una sfida. I dati fMRI sono incompatibili con la maggior parte dei progetti CNN esistenti.
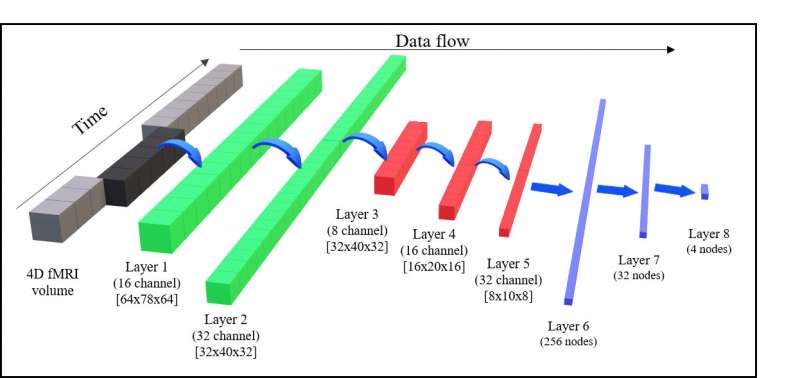
Per superare questo problema, i ricercatori hanno sviluppato un’architettura della CNN in grado di gestire in modo appropriato i dati fMRI con passaggi di pre-elaborazione minimi. I primi due livelli della rete si concentrano sull’estrazione di caratteristiche dai dati esclusivamente in base a cambiamenti temporali, senza riguardo per le proprietà strutturali 3D. Quindi, i tre strati successivi estraggono le caratteristiche spaziali a scale diverse dalle caratteristiche temporali estratte in precedenza. Ciò produce una serie di caratteristiche spazio-temporali che gli strati finali utilizzano per classificare i dati fMRI di input da un soggetto sano, uno con decadimento cognitivo lieve precoce o tardivo o uno con AD.
Questa strategia offre molti vantaggi rispetto ai precedenti tentativi di combinare l’apprendimento automatico con l’fMRI per la diagnosi di AD. Harshit Parmar, dottorando alla Texas Tech University e autore principale dello studio, spiega che l’aspetto più importante del loro lavoro risiede nelle qualità della loro architettura della CNN. Il nuovo design è semplice ma efficace per la gestione di dati fMRI complessi, che possono essere inviati come input alla CNN senza alcuna manipolazione o modifica significativa della struttura dei dati. A sua volta, questo riduce le risorse computazionali necessarie e consente all’algoritmo di effettuare previsioni più velocemente.
I metodi di deep learning possono migliorare il campo del rilevamento e della diagnosi di AD? Parmar la pensa così. “Le CNN di deep learning potrebbero essere utilizzate per estrarre biomarcatori funzionali correlati all’AD, che potrebbero essere utili nella diagnosi precoce della demenza correlata all’AD”.
I ricercatori hanno addestrato e testato la loro CNN con dati fMRI da un database pubblico e i risultati iniziali erano promettenti: l’accuratezza della classificazione del loro algoritmo era pari o superiore a quella di altri metodi.
Se questi risultati valgono per set di dati più grandi, le loro implicazioni cliniche potrebbero essere enormi. “L’Alzheimer non ha ancora una cura. Sebbene il danno cerebrale non possa essere invertito, la progressione della malattia può essere ridotta e controllata con i farmaci”, secondo gli autori. “Il nostro classificatore può identificare con precisione le fasi di un lieve detoriamento cognitivo che forniscono un avvertimento precoce prima della progressione nell’AD”.